סימפוניה של ננו-חומרים ואימונותרפיה המבוססת על מחזור החיסוניות הסרטנית
Sep 13, 2023
תַקצִיר
מערכת החיסון מעורבת בהתחלה והתקדמות של סרטן. מחקר על סרטן וחסינות תרם לפיתוח של מספר טיפולים אימונותרפיים מוצלחים מבחינה קלינית. אימונותרפיות אלו פועלות לעתים קרובות על שלב בודד של מחזור החסינות לסרטן. בשנים האחרונות, הגילוי של ננו-חומרים חדשים הרחיב באופן דרמטי את הפונקציות והיישומים הפוטנציאליים של ננו-חומרים. בנוסף לפעולה כפלטפורמות למתן תרופות, ננו-חומרים מסוימים יכולים לגרום למוות של תאים אימונוגניים (ICD) של תאים סרטניים או לווסת את הפרופיל וחוזק התגובה החיסונית בתור אימונומודולטורים. בהתבסס על הרבגוניות שלהם, ננו-חומרים עשויים לשמש פלטפורמה משולבת למספר תרופות או אסטרטגיות טיפוליות, תוך מיקוד בו-זמנית למספר שלבים של מחזור החסינות לסרטן כדי לשפר את התוצאה של התגובה החיסונית האנטי-סרטנית. כדי להמחיש את התפקידים הקריטיים של ננו-חומרים באימונותרפיה לסרטן המבוססת על מחזור החסינות לסרטן, סקירה זו תתאר באופן מקיף את ההצלבה בין מערכת החיסון לסרטן, ואת היישומים הנוכחיים של ננו-חומרים, כולל נשאי תרופות, מעוררי ICD ואימונומודולטורים. יתרה מכך, סקירה זו תספק דיון מפורט בידע בנוגע לפיתוח אימונותרפיות משולבות לסרטן המבוססות על מחזור חסינות הסרטן, בתקווה למקסם את היעילות של טיפולים אלו בסיוע ננו-חומרים.

תוסף תוסף cistanche-הגברת חסינות
1. הקדמה
סרטן, אחת המחלות הקטלניות ביותר, מאיימת על חייהם של כ-20 מיליון אנשים ברחבי העולם כיום1. באופן מסורתי, ניתוח, כימותרפיה והקרנות היו התרופות העיקריות לחולים עם סרטן. עם זאת, רעילות מערכתית, הישנות סרטן וגרורות משפיעות על הפרוגנוזה של החולים2. ככל שגדלה ההבנה שלנו לגבי האינטראקציה בין אונקולוגיה ואימונולוגיה, הפך אפשרי לנצל את מערכת החיסון של החולים כדי להתגונן מפני סרטן. טיפולים אימונותרפיים לסרטן שיכולים לעורר זיכרון אימונולוגי הוכיחו השפעה מעכבת מתמשכת על גדילת סרטן, הישנות וגרורות 3. טיפולים אימונותרפיים לסרטן, כגון חסימת מחסום חיסונית (ICB)4e7 וטיפול בתאי אנטיגן כימרי T (CAR-T)8e10, שיפרו את ההישרדות הכוללת בתת-קבוצה של חולים, במיוחד באלה עם סרטן המטולוגי. עם זאת, טיפולים אלו גורמים לתגובות מוגבלות בגידולים מוצקים11 וקשורים לדלקת מערכתית12. לאחר ההצלחה הקלינית של טיפול ICB ו-CAR-T, פותחו תרופות אימונותרפיות ואסטרטגיות קומבינטוריות רבות. אימונותרפיה מגדירה מחדש את הטיפולים בסרטן ואינה מוגבלת לטיפול בסוגי סרטן באתר או קיימים. עם זאת, ידע אימונולוגי לא שלם כמו גם מגבלות טכניות עדיין מגבילים את הפיתוח של אימונותרפיות יעילות יותר לסרטן. מטרות אימונולוגיות חדשות, שיטות מתן תרופות וטיפולים סינרגיסטים עשויים להוביל לפריצות דרך בתחום האימונותרפיה בסרטן.
לאחרונה, גילויים באימונולוגיה של סרטן הרחיבו את אופק האימונותרפיה בסרטן. ניאואנטיגנים, שמקורם במוטציות המתעוררות במהלך התפשטות מהירה של תאים סרטניים, מגבירים באופן משמעותי את האימונוגניות של אנטיגנים של גידול13. הוכח כי חיסוני Neoantigen מפעילים תאי T ציטוטוקסיים (CD8þ T)14. בנוסף, עומס גבוה של מוטציות סרטן הוא אינדיקטור פרוגנוסטי חשוב של אימונותרפיה בסרטן15,16. במהלך טיפול ICB, כמות תאי T CD8þ חודרים לגידול מקושרת ישירות להשפעה הטיפולית17. "גידולים חמים", עם מספר גבוה יותר של תאי T-CD8þ חודרים כנגד אנטיגנים של גידול, מציגים תגובה גדולה יותר לטיפול ICB18. בנוסף להפעלת תגובה חיסונית נגד תאים סרטניים, יש צורך גם בוויסות של המיקרו-סביבה המדכאת את מערכת החיסון של הגידול. ציטוקינים ותאי חיסון שונים מעורבים בפיתוח ובתחזוקה של מיקרו-סביבות מדכאות חיסון של הגידול. אלה כוללים אינטרלויקין (IL)-10, גורם גדילה משתנה (TGF)-b, נקודות ביקורת חיסוניות המובעות יתר על המידה על פני השטח של תאים סרטניים, תאי T רגולטורים (Treg) ומקרופאגים הקשורים לגידול מסוג M2- (TAMs)19. לאחרונה עלה מחזור החסינות לסרטן שמתאר את האינטראקציה של רקמות הסרטן ומערכת החיסון, והמושג הזה מתעדכן ומשתפר כל הזמן. המחזור החיסוני של הסרטן מתאר את התהליך של האופן שבו אנטיגנים של גידולים המשתחררים מתאי סרטן פגועים נלכדים על ידי תאי APC ומודרכים לתאי T CD8þ, וכיצד תאי T CD8þ חודרים לרקמות סרטניות והורגים תאי סרטן. עבור אימונותרפיה בסרטן, יש לשקול היטב כל שלב במחזור החסינות לסרטן. יתרה מכך, אופטימיזציה של ההפעלה הזמנית והמרחבית של התגובה החיסונית היא הבסיס להשגת אפקט אנטי סרטני בטוח ומתמשך20.
אימונותרפיה נגד סרטן ניתנת בדרך כלל באופן מערכתי כדי להבטיח שהוא מגיע לכל הגידולים הפוטנציאליים. עם זאת, זה יכול להיות מלווה בתופעות לוואי חמורות הקשורות למערכת החיסון, כגון קוליטיס, שלשולים ואנדוקרינופתיה23,24. לכן, מיקוד והפעלה ספציפית של תאי חיסון הקשורים לסרטן הם קריטיים.
בשל המאמצים המשותפים של קלינאים, ביולוגים, כימאים ומדעני חומר, ננו-חומרים ממלאים כעת תפקידים חשובים ומגוונים באימונותרפיה של סרטן25e28. ניתן להעשיר ננו-חומרים ברקמות סרטן בהשוואה לתרופות מולקולריות קטנות חופשיות, מה שנקרא אפקט חדירות ושימור (EPR) מוגברת29. במקור האמינו כי אפקט ה-EPR נובע מכלי הדם החדירים של הגידול ופגיעה בניקוז הלימפה30. דיווחים אחרונים העלו שרוב הננו-חומרים נכנסים לרקמות הגידול דרך מסלולים טרנס-אנדותליאליים פעילים31,32. מחקר מפורט יותר של מנגנון ה-EPR יאפשר לבצע אופטימיזציה של ננו-חומרים להעשרה יעילה יותר בתוך רקמות סרטן. כפלטפורמה אידיאלית, ננו-חומרים יכולים לשלב מספר תרופות לאסטרטגיות טיפול משולבות או סינרגטיות33,34, בינתיים, לחלק מהם יש את הפונקציונליות שלהם, כולל יכולות פוטותרמיות35, פוטודינמיות36 ויכולות תגובה מגנטית37. בנוסף, חלק מהננו-חומרים יכולים לעורר את המערכת החיסונית, חלקית על ידי גרימת ספיגת אנטיגן והצגה על ידי APCs38. תכונות אלו של ננו-חומרים מאפשרות להפעיל בו-זמנית מספר שלבים במחזור החסינות לסרטן בדיוק מרחבי וזמני, מה שעוזר בשליטה על אירועים חריגים הקשורים למערכת החיסון ומגביר ביעילות את התגובה החיסונית האנטי-סרטנית על ידי הפעלה סינרגטית של שלבים שונים של תהליך החיסון. יישומים נוכחיים של ננו-חומרים באימונותרפיה של סרטן כוללים שימוש כנשאי תרופות (מסירה של מעורר אפופטוזיס, אימונוסטימולנטים, מולקולות פוטותרמיות או פוטודינמיות, נוגדני ICB), חומרים פונקציונליים (אינדוקציה של תהליכים פוטותרמיים או פוטודינמיים), ואימונומודולטורים. סקירה זו סיכמה את המנגנונים החיסונים והידע על מחזור החסינות לסרטן, ובינתיים דנה בפירוט ביישום של ננו-חומרים לקידום אימונותרפיה של סרטן המבוססת על מחזור החסינות לסרטן. לבסוף, אנו מקווים לזהות פריצת דרך לקידום השילוב והיישום של ננו-חומרים באימונותרפיה של סרטן.
2. משחק בין סרטן לחסינות
טיפול אימונותרפי בסרטן הוא תחום בינתחומי מסובך, הכולל אינטראקציה ודיבור בין גידולים למערכת החיסון בשלבים שונים של התפתחות הסרטן. בתחילה האמינו שאין קשר ברור בין תהליכים חיסוניים והתפתחות סרטן. בעשורים האחרונים פורסמה כמות הולכת וגוברת של ראיות התומכות במעורבות של תהליכים חיסוניים בסרטן39,40. בנוסף, הוכח כי סרטן משפיע על תהליכים חיסוניים ומוביל לבריחה חיסונית או דיכוי חיסוני41. בהתבסס על תגליות אלו, מחקרים רבים התמקדו בהפעלת מערכת החיסון של חולים או אימוץ תאי חיסון רבי עוצמה כדי לנטר, לעכב ולהפוך את צמיחת הסרטן. עם זאת, ההשפעות של אימונותרפיה נגד סרטן כנגד מרכיב בודד בתהליך החיסון עלולות להיפגע על ידי חסימת חלקים אחרים של התהליך החיסוני המושרה על ידי סרטן. לכן, יש צורך דחוף להבהיר הבנה מפורטת של התגובות החיסוניות הקשורות להתפתחות וטיפול בסרטן.
2.1. מחזור חיסוני של סרטן
מחזור הסרטן-חסינות סוכם לראשונה על ידי Chen et al.20 בשנת 2013. הוא מתאר את תהליך החסינות התאית נגד רקמות סרטניות. הוא כולל מספר שלבים. שלב 1, אנטיגנים של גידול משתחררים מתאי סרטן פגומים ונלכדים על ידי תאים דנדריטים (DCs) לעיבוד; שלב 2, DCs מציגים אנטיגנים של גידול למולקולות MHCI ו- MHCII על תאי T; שלב 3, הכנה והפעלה של תגובת תאי ה-T המשפיעים; שלב 4, תאי T effector מסתובבים לגידולים; שלב 5, תאי אפקטור T חודרים לרקמות הגידול; שלב 6, תאי T אפקטור מזהים תאים סרטניים על ידי TCR ו-MHC I קומפלקס; שלב 7, תאי T אפקטור הורגים תאים סרטניים. השלב האחרון של הריגת תאים סרטניים תורם לשחרור אנטיגנים של גידול כדי להתחיל סבב חדש של מחזור חסינות הסרטן. לכן, מחזור חסינות הסרטן יכול להתקיים מעצמו עם התחלתו. מחזור החסינות המקורי לסרטן מדגיש את התפקוד הקריטי של חסינות תאית בטיפול בסרטן. עם זאת, ראיות רבות מוכיחות שחסינות הומורלית וחסינות מולדת ממלאות תפקידים חשובים בעיכוב התפתחות סרטן43. כמתואר באיור 1, אנטיגנים של הגידול מתאי סרטן נלכדים על ידי APC. כאנטיגנים אקסוגניים, אנטיגנים של הגידול עוברים אנדוציטוזה לאנדו בלבד, כך שמערכות מסוימות קושרות בדרך כלל מולקולות MHC II העשירות באנדוזום, מה שמעורר עוד יותר את ההתחלה וההפעלה של תאי T CD4þ. מסלול זה הוא חסינות הומורלית קלאסית, אשר הורגת תאי סרטן על ידי משקעים משותפים של נוגדן-אנטיגן או ציטוטוקסיות מתווכת תאים תלוית נוגדנים (ADCC) המתווכת על ידי תאי NK. עם זאת, DCs ספציפיים, כמו CD8aþ DCs44, או נסיבות מיוחדות, כמו דליפת אנדוזום של אנטיגנים גידולים45, מעוררים הצגה צולבת של אנטיגנים של גידול. במצב של הצגה צולבת, אנטיגנים גידוליים הקיימים בציטופלזמה מועברים על ידי הטרנספורטר של פפטידים אנטיגנים (TAP) לרשת האנדופלזמית (ER), וקשורים למולקולות MHC I שזה עתה הורכבו. הצגת הקומפלקס MHC I/antigen מובילה בסופו של דבר להפעלה של תאי T CD8þ. לכן, ארגנו מחדש והגברנו את התוכן של מחזור חסינות הסרטן בסקירה זו (איור 2). תיארנו את מחזור חסינות הסרטן כשלבים הבאים. (1) שחרור אנטיגנים של גידול מתאי סרטן פגומים או גוססים; (2) ספיגה והצגת אנטיגנים של גידול על ידי APC; (3) הכנה והפעלה של תאי T CD4þ ו-CD8þ להפעלת חסינות הומורלית ותאית אנטי סרטנית; (4) סחר בתאי NK, נוגדנים ספציפיים לאנטיגן לגידול ותאי T CD8þ; (5) הסתננות והעשרה של תאי NK, נוגדנים ספציפיים לאנטיגן לגידול ותאי T CD8þ לרקמות סרטניות; (6) הכרה ומיגור של תאי סרטן באמצעות ציטוטוקסיות של תאי T CD8þ והשפעת ADCC המתווכת על ידי תאי NK.
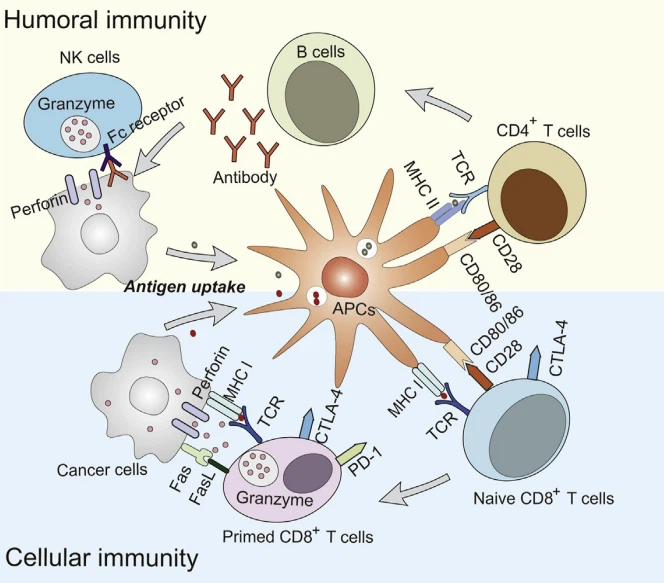
איור 1 איור 1 חסינות מסתגלת בטיפול בסרטן. חסינות הומורלית: APCs קולטים ומציגים אנטיגנים על ידי מולקולות MHC II כדי להפעיל תאי CD 4þ T; תאי T CD4þ מציגים אנטיגנים לתאי B, וכתוצאה מכך הפרשת נוגדנים ספציפיים לאנטיגן; נוגדנים נקשרים לאנטיגנים ומצמצמים יחד לעיכול על ידי מקרופאגים או מעוררים אפקט ADCC המתווך על ידי תאי NK. חסינות סלולרית: תאי סרטן נבלעים על ידי APC; APCs מצליבים אנטיגנים לתאי T CD8þ נטולי על ידי מולקולות MHC I, המלווה בביטוי CTLA-4 על תאי T CD8þ מודרכים; תאי T עם CD8þ דרוכים מזהים תאים סרטניים באמצעות קומפלקס MHC I/antigen והורגים תאים באמצעות מסלול ה-perforin, granzyme ו-Fas/FasL; עם זאת, החיבור של CTLA-4 או PD-1 עם הליגנדים שלהם יכול לגרום לחוסר תפקוד של תאי T עם CD8þ.
2.2. בריחה חיסונית ודיכוי חיסוני ברקמות סרטן
הקשר בין סרטן לחסינות הוא מסובך ביותר. מחקרים אחרונים העלו כי דלקת כרונית תורמת להתחלה ולגדילה של סרטן. מוטציות גנים או וריאציות מטבוליטים מתרחשות בתאי סרטן במהלך הגידול. תאי T CD8þ מזהים והורסים תאים סרטניים על ידי ניטור האנטיגנים החריגים שמוצגים על ידי מולקולות MHC I על תאים סרטניים, מה שמבטיח שכיחות נמוכה של סרטן בהתחשב בכך שמוטציות מתרחשות בכ-107 תאים אנושיים מדי יום. בדרך כלל, תהליך ההרג של תאי T CD8þ על תאי סרטן יכול להפעיל את מחזור החסינות לסרטן ולעכב ביעילות את התרחשות הסרטן. עם זאת, תאי T CD8þ לפעמים עיוורים לתת-קבוצה של תאים שעברו מוטציה, מה שמכונה בריחה חיסונית של תאים סרטניים46. יתרה מכך, הסביבה המדכאת את מערכת החיסון של הגידול מעכבת גם את פעולת מחזור החסינות לסרטן. הסיבות העיקריות לבריחה חיסונית ודיכוי חיסוני מסוכמות כדלקמן (איור 3).
(1) בחירה חיסונית מאפשרת לגידולים בעלי אימונוגניות חלשה יחסית לחמוק ממעקב חיסוני ולהתרבות באופן סלקטיבי47. סרטן המושרה על ידי וירוסים אונקוגניים וחומרים מסרטנים כימיים הם אימונוגניים ביותר ומתנקים בקלות על ידי המערכת החיסונית, בעוד שסרטנים ספונטניים של בעלי חיים נושאים אימונוגניות חלשה ונוטים להישמר48. (2) חסימת אנטיגן או הטמנה על פני השטח של תאים סרטניים משפיעה על זיהוי והתקפה של תאי חיסון49. חלק מתאי הסרטן מביאים לידי ביטוי יתר של mucopolysaccharides50, כגון sialic acid51 או glycoproteins52, ומונעים מתאי CD8þ לזהות אנטיגנים המוצגים על ידי MHC I. ניקוי חומצה סיאלית נמצא כמשפר את התגובה החיסונית האנטי סרטנית53,54. (3) ביטוי מופחת של מולקולות MHC I על פני השטח של תאים סרטניים יכול להגביל את זיהוי תאי T מסוג CD8þ. עם זאת, מולקולות MHC I מעכבות גם תאי NK על ידי קשירת קולטנים מעכבי תאי רוצח (KIR) על תאי NK. מחסור במולקולות MHC I מפעיל את תאי NK כדי לתווך את התמוגגות או אפופטוזיס של תאים סרטניים57. לכן, תאי סרטן מבטאים מולקולות MHC I שאינן קלאסיות (HLA-E ו-HLA-G) כדי להתחבר ל-KIR ולעכב את הפעילות של תאי NK58. (4) ביטוי Fas מופרע על פני השטח של תאי סרטן מגביל את היכולת של תאי T CD8þ לעורר אפופטוזיס של תאי סרטן באמצעות מסלול Fas/FasL59. יתרה מכך, סוגי סרטן מסוימים מבטאים יתר על המידה ומפרישים FasL כדי לקשור מולקולות Fas על תאי T ולגרום למוות של תאי T60. (5) תאי סרטן מפרישים גורמים מעכבים, כגון IL-10 ו-TGF-b כדי לדכא את התגובה החיסונית של המארח61,62. מולקולות מעכבות אלו מצטברות ברקמות סרטניות, ויוצרות מיקרו-סביבה חזקה מדכאת חיסון, אשר משביתה והורגת תאי חיסון חודרים63. בנוסף, ברקמות סרטניות, תאי סטרומה מפרישים אינדולאמין-2,3- דיאוקסיגנאז (IDO) כדי לעכב את התפשטות תאי T64. IDO הוא האנזים המגביל את הקצב למטבוליזם של טריפטופן ומוציא את הטריפטופן במיקרו-סביבה כדי לעכב את התפשטות תאי ה-T 65. ציטוקינים נפוצים הקשורים לסרטן מפורטים בטבלה 1 66e77. (6) תאי חיסון מדכאים קיימים ברקמות הגידול, כולל פיברובלסטים הקשורים לסרטן (CAF), תאי T רגולטורים (Treg), תאים מדכאים (MDSCs) ומקרופאגים מסוג M2-(TAM) ). סרטן, אשר יכול להיחשב כפצע שאינו מרפא, יכול לגרום לתגובה דמוית פציעה, לרבות המשך ההפעלה של פיברובלסטים. במהלך התקדמות הסרטן, תאים סרטניים מפרישים גורם גדילה אנדותל כלי דם (VEGF) ומגייסים פיפי-פיברובלסטים, תאי אנדותל ותאי דלקת.

איור 2 מחזור סרטן-חסינות. (1) שחרור אנטיגנים של גידול מתאי סרטן פגומים או גוססים; (2) ספיגה והצגת אנטיגנים של גידול על ידי APC; (3) הכנה והפעלה של תאי T CD4þ ו-CD8þ להפעלת חסינות הומורלית ותאית אנטי סרטנית; (4) סחר בתאי NK, נוגדנים ספציפיים לאנטיגן לגידול ותאי T CD8þ; (5) הסתננות והעשרה של תאי NK, נוגדנים ספציפיים לאנטיגן לגידול ותאי T CD8þ לרקמות סרטניות; (6) הכרה ומיגור של תאים סרטניים באמצעות ציטוטוקסיות של תאי T CD8þ וציטוטוקסיות תלוית נוגדנים (ADCC) המתווכת על ידי תאי NK. העיצוב של איור 2 נוצר בהשראת איור 1 של Ref. 20 עם אישור זכויות יוצרים. זכויות יוצרים ª 2013 Elsevier Inc. פיברובלסטים ותאי דלקת הם המשאבים העיקריים של VEGF שמקורו במארח, היוצר מעגל אוטוקריני ברקמות סרטן78. עם זאת, הפחתת פעילות הפיברובלסט והתאים הדלקתיים הנצפית לאחר ריפוי פצעים אינה מתרחשת בסרטן. (7) מחסומים חיסוניים
הפעלת תאי T דורשת קישור של מולקולות MHC I הקשורות לאנטיגן ל-TCRs ומווסתת על ידי אותות קוסטימולטורי או מעכבים, או נקודת ביקורת חסינות (טבלה 2). צמדי מחסומים חיסוניים הם אסטרטגיות חשובות להשגת סובלנות עצמית ולמנוע ממערכת החיסון לפגוע ברקמה הרגילה שמסביב במהלך חסינות אנטי-פתוגנית. נקודות ביקורת חיסוניות משדרות אותות "עצמי" ו"אל תאכל אותי" לתאי T. תאי סרטן נמלטים ממעקב חיסוני על ידי הגברת אותות של נקודת ביקורת חיסונית. אסטרטגיות ICB מספקות טיפולים רבי עוצמה כדי להקל על חסינות אנטי סרטנית. CTLA-4 מתבטא באופן דומיננטי בתאי T עם דריכה CD8þ ומשתף את הליגנד B7 עם CD28. הקשר של B7 עם CD28, מלווה בהצגת אנטיגן, מפעיל תאי T נאים. לעומת זאת, הקישור של B7 ל-CTLA מונע הפעלה של תאי T. הרגולציה העליונה של CTLA-4 על תאי T עם הכנה CD8þ מונעת פעולת יתר של חסינות תאית79. למרות ש-CTLA-4 מתבטא בעיקר על תאי T עם CD8þ מודרכים, הוא נמצא גם בתאי Th ו-Treg80. המעורבות של CTLA-4 בתאי Th מפחיתה את פעילות Th, בעוד שהביטוי של CTLA-4 בתאי Treg משפר את השפעתם המדכאת את החיסון81. התפקיד העיקרי של PD-1 הוא להגביל את פעילות תאי T ברקמות היקפיות בתגובה הדלקתית האנטי-פתוגנית. עם זאת, יש לו פונקציה מדכאת חיסונית במהלך התקדמות הסרטן. PD-1 מתבטא בלימפוציטים רבים החודרים לגידול (TIL), כולל CD8þ T, Treg, B ו-NK cells82. הליגנדים הנפוצים של PD-1 הם PD-L1 ו-PD-L2, שבדרך כלל סובלים מביטוי יתר בתאי סרטן83. הקשר בין PD-1 והליגנדים שלו יכול לגרום לחוסר תפקוד של תאי CD8þ T ו-NK. עם זאת, PD-1 משפר את השגשוג של תאי Treg בנוכחות ליגנדים 84. בסרטן מוצק, PD-L1 הוא הליגנד העיקרי של PD-1. עם זאת, רמת הביטוי של PD-L1 היא הטרוגנית בסוגי סרטן שונים, מה שעשוי להיות חשוב כאשר בוחנים את ההיתכנות של אסטרטגיות טיפוליות נגד PD-1 ו-PD-L1. ההשפעות האנטי-סרטניות של חסימת CTLA-4 או PD-1 נובעות מההשפעה הסינרגטית של הפעלת תאי CD8þ ו-NK ועיכוב תאי Treg.

איור 3 איור 3 דיכוי חיסוני ברקמות סרטן.
טבלה 1 ציטוקינים הקשורים לסרטן.

2.3. אימונותרפיה לסרטן משחזרת מחזור חסינות לסרטן
תפקידה של מערכת החיסון במהלך התחלת סרטן, התפתחות וגרורות זכה לתשומת לב גוברת. הזיהוי של מחזור חסינות הסרטן המעורב בסרטן תמך בשימוש באימונותרפיות בחולים. ככל שהטיפולים האימונותרפיים הפכו ממוקדים יותר, התוצאות הקליניות של חולים המקבלים אימונותרפיות אנטי סרטניות משתפרות בהדרגה, ובינתיים, פרופיל הבטיחות משתפר. בדרך כלל, טיפולים אימונותרפיים לסרטן המחזירים ישירות את מחזור החסינות לסרטן או מקלות על ההשפעה המדכאת את מערכת החיסון על מחזור החסינות לסרטן, מראים פוטנציאל רב למיגור הסרטן. מכיוון שמחזור החסינות לסרטן יכול להתקיים מעצמו, כל טיפול אימונותרפי המקדם כל שלבי מחזורי חסינות הסרטן עשוי להשיג השפעות אנטי סרטניות מוגברות. טיפולים אימונותרפיים לסרטן בשימוש כיום המשחזרים את מחזור החסינות לסרטן כוללים אימונותרפיה לא ספציפית, טיפול בנוגדנים חד שבטיים, טיפול בתאים מאמצים (ACT) וטיפול בחיסון נגד גידולים.
2.3.1. אימונותרפיה לא ספציפית (ציטוקינים וחומרים אימונוסטימולנטים)
אימונותרפיה לא ספציפית, הכוללת בעיקר ציטוקינים וחומרים אימונוסטימולנטים, מפעילה בדרך כלל באופן שיטתי תגובות חיסוניות נגד תאים סרטניים. אימונותרפיה לא ספציפית כוללת בדרך כלל מנגנונים מגוונים לקידום מחזור החסינות לסרטן, כולל גרימת ספיגת אנטיגן הגידול של APCs, קידום הפעלה של תאי CD8þ, והקלה על הסביבה המדכאת את מערכת החיסון של הגידול על ידי גירוי ציטוקינים. Coley85 נתן לראשונה תמציות חיידקים (הרעלים של קולי) כעזרים בחולים עם סרטן בסוף המאה התשע-עשרה. הרעלים של קולי שינו את רמות הציטוקינים והובילו לפינוי הגידול בחלק מהחולים. לאחר מכן, ציטוקינים רבים הוכחו כבעלי השפעות אנטי סרטניות, כולל IL-2, IFN-g ו-GM-CSF86. IL-2 ו-IFN-g הוכיחו פוטנציאל אנטי סרטני מבטיח. עם זאת, היישום הקליני של IL-2 ו-IFN-g מעוכב על ידי רעילות חמורה בעקבות מתן מערכתי 87. הוכח כי מיזוג ציטוקינים עם חלבוני מיקוד מגביר את ההצטברות בגידולים ומשפר את התוצאות הבאות תוך הפחתת רעילות שיטתית88. עם זאת, לאסטרטגיות היתוך יש השפעות ברורות על ציטוקינים שונים. השילוב של טכנולוגיית טרנסגנים וציטוקינים מספק אסטרטגיית טיפול חדשה. תאים סרטניים ששונו עם גנים של ציטוקינים הוערכו על סמך ההשפעה המגנה מפני אתגרים שלאחר מכן עם תאים סרטניים מסוג פרא89,90. למעט ציטוקינים מעוררים, מוטציות אימונוסטיות, כגון אגוניסטים של TLRs או STING חלבון, נמצאים בשימוש נרחב כדי להפעיל את הפונקציה של APCs91e93.

הטבות תוספי cistanche
2.3.2. נוגדנים מונוקלונליים (mAbs)
באימונותרפיה של סרטן, נוגדנים חד שבטיים (mAbs) מהווים חלק ניכר מהתרופות המאושרות על ידי מינהל המזון והתרופות האמריקאי (FDA). mAbs מתקשרים ליעדים בעלי זיקה גבוהה, מה שמבטיח את הדיוק והיעילות של סוכנים אלה. יתר על כן, mAbs יכולים לתווך ADCC של תאי NK, מה שתומך עוד יותר בהשפעות האנטי-סרטניות של mAbs. ה-mAbs המכוונים למחזורי חסינות סרטן מחולקים בעיקר לשתי קטגוריות: מעכבי נקודת ביקורת חיסונית להקלה על דיכוי החיסון במחזור החסינות לסרטן ותכשירי נוגדנים-תרופות (ADCs) להשראת מוות ושחרור אנטיגן של תאים סרטניים. קיומם של נקודות ביקורת חיסוניות על תאים סרטניים מגביל באופן משמעותי את יעילות הטיפול האימונותרפי בסרטן. כדי לשחזר את תפקודם של תאי T עם CD8þ מודרכים, נוגדנים המעכבים את הקשר של CTLA-4 או PD-1 עם ליגנדים בהתאמה נחקרו בהרחבה. נתונים קליניים מקדמים את הסוציאליזציה של mAbs נגד CTLA-4 (ipilimumab), PD- (nivolumab, pembrolizumab) ו-PD-L1 (אכלו zolizumab)94. בהשוואה ל-CTLA-4 ו-PD-1 mAbs, PD-L1 mAbs הוכיחו רעילות נמוכה יותר. לאחרונה, ADCs משכו תשומת לב, ושלושה סוגים של ADCs ממוסחרים מאז 2019. לתרופות כימיות מסורתיות אין סלקטיביות ודורשות מינון גבוה יחסית כדי להשיג השפעות מרפאות. נוגדנים בעלי זיקה גבוהה יכולים להיות קשורים במדויק למטרות שלהם. ADCs, המורכבים מ"ראש נפץ" של נוגדן, מקשר הניתן לפירוק ותרופה ציטוטוקסית, משלבים את היתרונות של נוגדנים ותרופות כימיות. ADCs המאושרים כיום ממקדים לסמנים ביולוגיים המבוטאים יתר על המידה על תאים סרטניים, כגון HER-2, CD30, CD33 ו-CD2295. פיתוח טכנולוגיות ADC הרחיב את האינדיקציות לטיפולים אלו מלוקמיה לממאירות מוצקה. Enhertu, ADC חדש יותר, שימש בחולים עם סרטן שד, קיבה וסרטן ריאות חיובי HER-2, עם שיעור תגובה אובייקטיבי (ORR) של כ-60%96. ה-ADC המאושרים על ידי ה-FDA מסוכמים בטבלה 3.
2.3.3. פעולה
ACT כרוך בהפעלה והרחבה של תאי חיסון עצמיים במבחנה, אשר לאחר מכן מוחדרים למטופל כדי לשפר את היכולת האנטי סרטנית של מערכת החיסון. ACT מבצעת ישירות את הזיהוי וההרג של תאים סרטניים ומניעה מחדש את מחזור החסינות לסרטן על ידי אספקת מספר רב של אנטיגנים לגידולים. התאים המשפיעים של ACT הם בעיקר תאי רוצח מופעל על ידי לימפוקין (LAK)97, תאי רוצח המושרה על ידי ציטוקינים (CIK)98 לימפוציטים חודרים לגידול (TIL), DC, NK, TCR-T ו-CAR-T99. בטיפול לא ספציפי ב-ACT, תאי החיסון המשפיעים, כולל LAK, CIK, DC ו-NK, אינם מזהים אנטיגנים ספציפיים של גידול ואין להם הגבלה של MHC I. למרות שטיפול לא ספציפי ב-ACT הוכיח פעילות אנטי-סרטנית מצוינת נגד תאים סרטניים החסרים מולקולות MHC I, לא ניתן להתעלם מהרעילות הפוטנציאלית לרקמה תקינה. תאי החיסון המשפיעים בטיפול ספציפי ב-ACT, כולל TIL ו-TCR-T, יכולים לזהות אנטיגנים של גידול. ההכרה והאפקט הקטלני שלאחר מכן בתאים סרטניים תלויים במולקולות MHC I. בשל ההגבלה של MHC I, טיפולי ACT ספציפיים מבוססי TIL ו-TCR-T אינם יעילים נגד תאים סרטניים חסרי MHC I. עם זאת, CAR-T משתמש במודל זיהוי נוגדנים-אנטיגן כדי להחליף את הקשר של TCR-CD3 עם MHC I /antigen complex, אשר נמנע מהגבלה של MHC I. עם זאת, CAR-T יכול לכוון רק לתאים סרטניים עם אנטיגנים על פני השטח, ולא לאלה עם אנטיגנים פנימיים. טיפולי CAR-T שאושרו על ידי ה-FDA, כגון קימריה ויסקרטה, מכוונים בעיקר ללימפומות. היישום של CAR-T על גידולים מוצקים נותר מאתגר. זיהוי סמנים ביולוגיים טובים יותר לסרטן והעיצוב הרציונלי של CAR הם הגורמים העיקריים להצלחת הטיפול ב-CAR-T. יתרה מכך, טכנולוגיות דומות נוצלו בתאי CAR-NK, אשר נוצלו במחקרים פרה-קליניים רבים. לחולים הנושאים סרטן יש לרוב מערכת חיסונית חלשה, עם מגבלות במספר ובפעילות של לימפוציטים עצמיים. לכן, התפתחות לימפוציטים ממקורות אחרים נחשבת לפריצת דרך. לאחרונה, טכנולוגיית תאי גזע פלוריפוטנטיים (iPSC) הרחיבה את המקורות והמינונים של לימפוציטים ראשוניים. אולי בגלל זיכרון אפיגנטי, בהשוואה לתאים סומטיים, iPSCs מדם טבורי או לימפוציטים מדם היקפי מגבירים את היעילות של ייצור לימפוציטים CD4þ CD8þ101. טיפולי CAR-T או CAR-NK המבוססים על iPSCs הוכיחו השפעות מרפאות משמעותיות בחולים עם גידולים ממאירים של תאי B וסרטן שחלות102. יתר על כן, CAR-T אוניברסלי מתגבר על המגבלות הקשורות למקור התא, ומספק ACT ישים נרחב ללא התאמת HLA. לפיכך, מולקולות MHC I, MHC II ו-TCR מבוטלות כדי למנוע דחיית שתל או תגובות שתל מול מארח באמצעות עריכת גנים בוגרים. יתר על כן, HLA-E או HLA-G i הוכנסו כדי למנוע התקפות חיסוניות על ידי תאי NK של חולים103. ניסויים קליניים שחוקרים טיפולי ACT או CAR אוניברסליים שמקורם ב-iPSC נמשכים כעת.
2.3.4. חיסונים נגד סרטן
התחלת והתקדמות הגידול מלווים בדרך כלל במוטציות גנטיות, היוצרות אנטיגנים ייחודיים השונים מאלה בתאים אוטולוגיים רגילים. שחרור אנטיגנים של גידול אמור להתחיל את מחזור החסינות לסרטן. עם זאת, חוסר היכולת של APCs במיקרו-סביבת הגידול או האימונוגניות הנמוכה של אנטיגנים של הגידול מונעים את לכידה והצגתם של אנטיגנים של הגידול. חיסונים לסרטן, המורכבים מאנטיגנים ואדג'ובנטים של הגידול, שואפים להתגבר על הסביבה המדכאת את מערכת החיסון של הגידול, להגביר את האימונוגניות של אנטיגנים של הגידול, להפעיל חסינות תאית או הומורלית עצמית, ובכך לשלוט או לחסל סוגי סרטן104. באופן מסורתי, חיסונים לסרטן כללו תאים שלמים (חיסונים לתאי סרטן וחיסוני DC), חיסוני פפטיד וחומצות גרעין. עם ההתפתחויות האחרונות בריצוף גנים וביואינפורמטיקה, ניתן לזהות במהירות ניאו-אנטיגנים מותאמים אישית של גידולים105. יחסית לאנטיגנים הקשורים לגידול, ניאו אנטיגנים נגזרים ממוטציות בתאי סרטן ולכן הם אנטיגנים חדשים לחלוטין. ניאו-אנטיגנים אלו הם בדרך כלל שברי פוליפפטיד בעלי יכולת קשירה מסוימת עם HLA; עם זאת, האימונוגניות שלהם אינה ודאית ויש לקבוע בניסויים vivo. חיסוני פפטיד וחיסוני mRNA המבוססים על ניאו אנטיגנים יכולים לגרום לחסינות הומוראלית ותאית אנטי סרטנית14,106. מחקר מעמיק של מוות תאי סרטן מצא שחלק מתאי הסרטן עלולים לגרום לתגובה חיסונית לאחר מוות, הנקראת מוות תאי אימונוגני (ICD). כאשר תאים סרטניים מתים כרגיל, האנטיגנים והרכיבים האימונוסטימולטוריים שלהם מתכלים דרך מסלול האפופטוזיס. במהלך ICD, תאים סרטניים חושפים את האנטיגנים שלהם ומשחררים דפוסים מולקולריים הקשורים לנזק (DAMPs), כולל ATP, חלבון קבוצתי 1 עם ניידות גבוהה (HMGB1) ו-calreticulin107. DMAPs אלו מעוררים קליטה והצגת אנטיגנים של גידול על ידי תאי APC, ובכך מייצרים השפעות אנטי סרטניות. חיסונים לסרטן באתרו המבוססים על תהליך ICD חשפו מנגנונים אנטי סרטניים חדשים של תרופות כימותרפיות מסורתיות, כגון דוקסורוביצין (DOX)109. יתר על כן, מספר טיפולי סרטן חיצוניים, כגון טיפול פוטותרמי, טיפול פוטודינמי והקרנות, הוכחו כמעוררים ICDs בתאים סרטניים. עם זאת, ההשפעה של אסטרטגיית החיסון במקום אינה מובטחת, והיא תלויה ישירות באימונוגניות של אנטיגנים של הגידול. סרטן עם עומס מוטציות גדול יותר מציגים תגובה גדולה יותר לחיסונים במקום. יתרה מכך, לחיסונים לסרטן המפעילים חסינות תאית יש תוצאות טובות נגד סרטן. ההצטלבות של APCs עבור אנטיגנים גידולים אקסוגניים היא קריטית להפעלת חסינות תאית. חיסוני הסרטן שיכולים לכוון ל-CD8aþ DCs בבלוטות הלימפה או לשחרר אנטיגנים של גידולים מהאנדו בלבד, כך שמערכת כלשהי לציטופלזמה, מעוררים הצגה צולבת של APCs וחסינות תאית אנטי-סרטנית טובה יותר.
טבלה 3 ADCs מאושרים על ידי ה-FDA לטיפול בסרטן.

3. ננו-חומרים המעוררים מחזור חיסוני לסרטן
לננו-חומרים יש יתרונות מגוונים, כגון גודל ניתן לשליטה, תאימות ביולוגית גבוהה ויכולת עומס מעולה. ככל שהמנגנונים העומדים בבסיס האימונולוגיה של הסרטן מובהרים בהדרגה, לננו-חומרים צפויים להיות פוטנציאל לייעל היבטים רבים של אימונותרפיה של סרטן בהתבסס על מחזור חסינות הסרטן. יכולת המיקוד של ננו-חומרים יכולה להבטיח שהשלבים השונים של מחזור חסינות הסרטן יופעלו בדיוק זמני ומרחבי, מה שממזער את תופעות הלוואי תוך הבטחת תגובה חיסונית אנטי-גידולית. הזיהוי של השפעות EPR הופך את הננו-חומרים (20e200 ננומטר) לשותף מתאים לאספקת תרופות ממוקדות סרטן110. יישום ננו-חומרים כנשאים עשוי להעשיר תרכובות מווסתות של מערכת החיסון ברקמות הסרטן כדי לשפר את התגובה החיסונית ולהפחית רעילות מערכתית. בנוסף, ננו-חומרים בגודל של כ-25 ננומטר נוטים יותר להתמקד בבלוטות הלימפה, וכתוצאה מכך הפעלה חיסונית חזקה המושרה על ידי חיסוני סרטן111,112. בנוסף להשתתפות בטיפול אימונותרפי בסרטן כנשאי תרופות, מספר הולך וגדל של ננו-חומרים מצוינים לתווך טיפולים אנטי-סרטניים חיצוניים, כולל טיפולים פוטותרמיים ופוטודינמיים, אשר גורמים ל-ICD בתאי סרטן ליצור חיסון אנטי-סרטני במקום ולהניע מחדש את מחזור החסינות לסרטן. בנוסף, ננו-חומרים חלקיים הוכיחו השפעות אדג'ובנטיות ייחודיות, שיכולות לעורר את הגוף לייצר תגובה חיסונית חזקה יותר ולהקל על דיכוי מחזור חסינות הסרטן. להלן יציג בפירוט כיצד ננו-חומרים כנשאי תרופות, מעוררי ICD ותוספים חיסוניים משפרים טיפול אימונותרפי בסרטן המבוסס על חסינות סרטנית. התפקודים הרב-תכליתי של ננו-חומרים מעלים את האפשרות לפתח אימונותרפיה סרטנית קומבינטורית למיקוד בו-זמנית במספר שלבים של מחזור חסינות הסרטן כדי להשיג תוצאה אנטי-סרטנית חזקה יותר (איור 4).

יתרונות תוסף cistanche-איך לחזק את המערכת החיסונית
3.1. פלטפורמת משלוח תרופות
באימונותרפיה של סרטן, נעשה שימוש נרחב בננו-חומרים כדי למקד ולהעשיר תרכובות מעוררות מערכת החיסון או חיסונים לסרטן ברקמות סרטן או רקמות חיסוניות (כגון בלוטות לימפה). התרופות המועשרות משפרות את הפעלת המערכת החיסונית בגלל הריכוז המוגבר וגם מגבילות את הנזק לרקמה תקינה הנגרמת מתגובה חיסונית מערכתית. ניתן לחלק ננו-חומרים המתמקדים ברקמות סרטניות ובלוטות לימפה לסוכני מיקוד פסיביים ופעילים, בהתאם למנגנון המשמש. מיקוד פסיבי מסתמך על קליטת ננו-חומרים בגודל ספציפי על ידי רקמות סרטניות או בלוטות לימפה, בעוד מיקוד פעיל מסתמך בעיקר על ביטוי יתר של מולקולות קולטן. לדוגמה, קולטני av-integrin או folate מתבטאים יתר על המידה בכמה רקמות סרטניות, וניתן לשנות את הליגנד av-integrin (iRGD) או חומצה פולית על פני השטח של ננו-חומרים כדי להשיג מיקוד פעיל. קולטני מנוז באים לידי ביטוי יתר על פני השטח של APCs בבלוטות הלימפה. לכן, ניתן לשנות מנוז בננו-חומרים כדי למקד באופן פעיל ל-APC. ננו-חומרים ממוקדים לסרטן עמוסים בדרך כלל במפעילים חיסוניים שיכולים להתגבר על המיקרו-סביבה המדכאת את מערכת החיסון, כולל ציטוקינים, ממריצים חיסוניים ונוגדני ICB. ננו-חומרים המכוונים לבלוטות לימפה עמוסים בדרך כלל באנטיגנים של גידול כדי לקדם את העיבוד וההצגה של אנטיגנים על ידי DCs, וכדי להפעיל תאי CD8þ ספציפיים לסרטן בבלוטות הלימפה. הזיהוי והפיתוח של מעוררי ICD הובילו לשימוש בננו-חומרים כדי להעביר חומרים אלה לרקמות סרטניות. בנוסף, השילוב הרציונלי של אימונומודולטורים שונים בננו-חומרים ישפר עוד יותר את היעילות של אימונותרפיה בסרטן.
3.1.1. ציטוקינים וחומרים חיסוניים
מתן מערכתי של ציטוקינים חופשיים וחומרים אימונוסטימולנטים מוביל לסערה חיסונית בלתי נשלטת. ננו חומרים ממוקדי סרטן יכולים להגביל את ההפעלה החיסונית המתרחשת בתוך רקמות סרטן. לאחר הרכבה של פולי אתילן-אימין בעל משקל מולקולרי נמוך (600 דאה), הוכח כי קישור עם b-cyclodextrin והגן IL-2 וקשר עם פולאט, ננו-חלקיקים פולימריים בקוטר של כ-100 ננומטר, גורמים להפעלה של CD4þ תאי T, CD 8þ תאי T ותאי NK, וכתוצאה מכך נסיגה של שתלי מלנומה B16eF1113. שילוב של הגן IL-2, גן IL-12, שומנים מתפצלים אנדוזומלית ופפטיד RGD הניתן לפירוק אנדוזומלית יצרו ננו-חלקיקים בגודל של כ-100 ננומטר, מה שהוביל להגברת חדירת לויקוציטים ואזורים סרטניים נמקיים114. בנוסף, טעינת חלבוני Fc מאוחדים IL-2-ונוגדן CD137 אגוניסטי על ליפוזומים יכולה לשמור על ההשפעות האנטי-סרטניות החזקות של IL-2 ושל נוגדן CD137 אגוניסטי, תוך הפחתת רעילות מערכתית הנגרמת על ידי לויקוציטים במחזור115 (איור .5). מלבד ציטוקינים, ננו-חומרים בשילוב עם אימונוסטימולנטים מבטיחים הפעלה מקומית של לויקוציטים חודרים לגידול. הוכח כי מתן תוך ורידי של שומנים קטיוניים טעוני מחזורי-di GMP מעורר ביעילות את הייצור של אינטרפרון (IFN) והפעלה של תאי NK, אשר עיכבו גרורות בריאות במודל B16-F10 xenograft עכבר116. בנוסף, לננו-חומרים טעוני אימונומודולטור יש פוטנציאל לכוון ללוקוציטים הקשורים לסרטן. לדוגמה, ננו-חלקיקים הטעונים באגוניסט TLR7/8 כוונו ספציפית ל-DCs ברקמות סרטניות ובלוטות לימפה סחוטות באמצעות מיקוד פסיבי עקב השפעות הגודל. ננו-חומרים פולימריים של PLGA-PEG הקשורים לנוגדן אנטי-PD-1 (aPD1) או נוגדן CD8 הוכחו כנקשרים ספציפית לתאי T CD8þ חיוביים ל-PD-1. ננו-חומרים פולימריים PLGA-PEG אלה הוכחו כמספקים מעכבי TGF-b, והופכים את ההשפעה המדכאת של TGFb על תאי T CD 8þ118. ננו-חלקיקים דומים המעוטרים ב-aPD1 שימשו כדי לספק מעכב NF-kB ל-TIs חיוביים ל-PD-1 כדי להפחית את הייצור של IL-10 ו-TGF-b, ובכך להקל על התנאים המדכאים את מערכת החיסון119.
3.1.2. mAbs
ICB, הטיפול המוצלח ביותר ב-mAb המשמש באימונותרפיה של סרטן, פועל הן על TIL והן על לויקוציטים במחזור הדם, אשר גורמים להשפעות אנטי-סרטניות יחד עם דלקת אוטואימונית. ננו-חומרים יכולים להעביר נוגדני ICB לרקמות סרטן ולשפר את הרעילות. הוכח כי מיקרו-מחטים מתכלות עצמיות עוטפות aPD1 משחררות aPD1 לרקמות המלנומה ומעכבות באופן משמעותי את התקדמות הסרטן. בנוסף לשחרור מבוקר, ננו-חומרים גם מעניקים לנוגדני ICB השפעות רב ערכיות, מה שמחזק את האינטראקציה בין הנוגדנים למטרותיהם. בניית נוגדן רב-ערכי אנטי-PD-L1 (aPD-L1) על ידי צימוד aPD-L1 עם דנדרמרים פולי-(אמידואמין) מסועפים יתר על המידה, הגברה את תאוות הקישור עם PD-L1 פי שישה בהשוואה ל-aPD-L1121 חופשי. יתר על כן, מיזוג של scFv רקומביננטי של aPD1 עם פוליפפטיד דמוי אלסטין סובלני חיסוני (iTEP) הביא להרכבה עצמית של ננו-חלקיקי aPD1, שחסמו את נקודת הבידוק החיסונית של PD-1 במבחנה וב-vivo122. יתר על כן, ננו-חלקיקים שנטענו יחד עם mAbs שונים, כגון aPD1 ו-anti-OX40 נוגדן (aOX40) הפגינו תוצאות סינרגטיות ומשופרות נגד סרטן בהשוואה לשני הנוגדנים החופשיים123 (איור 6).
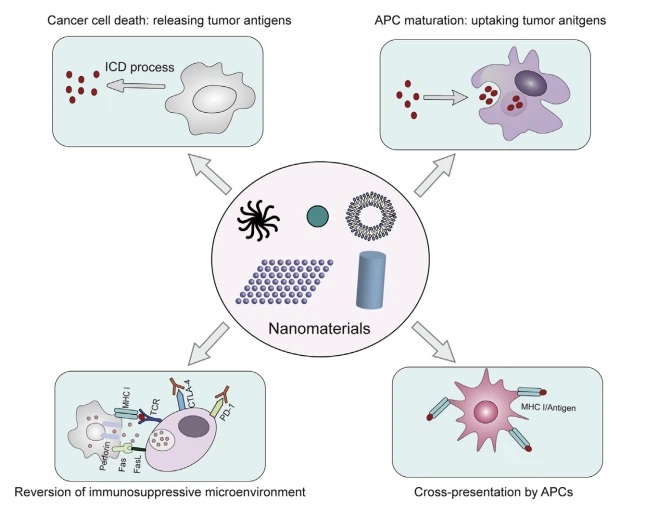
איור 4 ננו-חומרים מכוונים לשלבים שונים של מחזור חסינות הסרטן בנפרד או בו-זמנית. ננו-חומרים הנמצאים בשימוש כיום גורמים בעיקר ל-ICD של תאים סרטניים, מקדמים את ספיגת האנטיגן והבשלת ה-APC, משפרים את ההצגה ההולכת של APC, ומווסתים את המיקרו-סביבה המדכאת את מערכת החיסון של רקמות סרטן.
3.1.3. חיסונים לסרטן
אנטיגנים ואדג'ובנטים לגידול נדרשים עבור חיסונים לסרטן. מרכיבי עזר, כגון אימונוסטימולנטים, יכולים לשפר עוד יותר את האימונוגניות של חיסוני סרטן. ננו-חומרים הם פלטפורמות רב-תכליתיות המספקות יתרונות מגוונים לבניית חיסוני סרטן, כדלקמן124,125: (1) היכולת לספק בו-זמנית רכיבי חיסון שונים לאותם APC כדי להגביר תגובה חיסונית ספציפית; (2) להעשיר חיסונים לסרטן לנגמ"שים בבלוטות לימפה או ברקמות סרטן על ידי מיקוד פסיבי או אקטיבי; (3) לתווך השפעות גודל ורב-ערכיות של חיסוני סרטן כדי לעורר תגובה חיסונית חזקה; (4) שחרור מבוקר ובר-קיימא של אנטיגנים גידוליים המבטיח הפעלה ארוכת טווח של מערכת החיסון; (5) אספקה ציטוזולית של אנטיגנים של גידול כדי לקדם הצגה צולבת של APCs כדי לקדם ביעילות תאי T CD8þ נאי. אנטיגנים הקשורים לגידול (TAA) ואנטיגנים למודל נוצלו באופן נרחב לזיהוי ופיתוח ראשוניים של חיסוני סרטן מאחר וזיהוי של אנטיגנים ספציפיים לגידול הוא קשה יחסית. בהתבסס על TAAs ואנטיגנים מודלים (כגון אולבומין ו-OVA), נעשה שימוש במספר ננו-חלקיקים לפיתוח חיסוני ננו לסרטן. לדוגמה, חלקיקי PLGA126 מתכלים, (LCP) ננו-חלקיקים127, ננו-חלקיקי organosilica mesoporous mesoporous128, וננו-חלקיקי חלבון129, הטעינו בהצלחה TAAs ואנטיגנים מודלים, והוכחו כמתווכים חסינות ספציפית לאנטיגן לגידול. בעקבות הגילוי ש-DCs ממלאים תפקידים חשובים בקליטה ובטיפול בחיסוני סרטן, מספר גדל והולך של חיסוני ננו לסרטן תוכננו למקד את DCs130. לדוגמה, ננו-חלקיקים מוזהבים בגודל של כ-14 ננומטר שימשו לטעינת חלבון פלורסנט אדום (RFP) כאנטיגן מודל ו-CPG-ODN כעזרים. הניסוח הביא להעשרה של ננו-חלקיקים בבלוטות הלימפה המנקזות, לטיטר גבוה של נוגדן אנטי-RFP ולנסיגה של גידולי B16-F10131 המבטאים RFP. בנוסף, מולקולות מכוונות DC, כגון מנוז או נוגדנים CD40, עוברות שינויים בדרך כלל על ננו-חלקיקים כדי לספק חיסונים ננו לסרטן ל-DCs. לדוגמה, חלקיקי PLGA-ננו המכילים Pam3CSK4, Poly (I: C) ו-OVA, היו קשורים לנוגדנים נגד CD40, מה שהביא לאספקת חיסון יעילה ל-DCs ולהפעלה חזקה של תאי T CD8þ132. בנסיבות רגילות, DCs מציגים אנטיגנים לתאי T CD4þ כדי לעורר חסינות הומורלית לאחר בליעת אנטיגנים אקסוגניים. עם זאת, חסינות תאית המאפשרת הצגה צולבת של DCs בעזרת מולקולות MHC I מייצגת תגובה חיסונית אנטי סרטנית יעילה יותר. ננו-חומרים בעלי יכולת להעביר אנטיגנים של גידול לתוך הציטופלזמה משפרים מאוד את ההסתברות והיעילות של הצגה צולבת. ננו-חומרים טעונים חיובית, כגון פוליאתילן-אימין (PEI) וננו-גליונות ננו-כיטוזן/סידן פוספט, הוכחו כגורמים לבריחה אנדוזומלית של מטענים באמצעות אפקט ספוג פרוטון45,133. ננו-חומרים עמוסים בחומרים משבשי אנדוזום, כגון פפטידים יוצרי נקבוביות, יכולים לתווך בריחת מטען שנמסר בשיתוף פעולה. לדוגמה, Kong and Liu et al.134 בנו חיסונים ננו על ידי העמסת PLGA עם OVA והידרוקסיכלורוקין (HCQ). HCQ גרם לחדירת ממברנה של האנדוזום והקל על שחרור OVA. בהשוואה לננו-חלקיקים PLGA/OVA, חיסוני ננו הגבירו את הביטוי של MHC-I ואת המולקולה הקוסטימולטורית CD86 של BMDCs, העלו את התדירות של תאי IFN-gþ CD8þ T, IFN-gþ CD4þ תאי T וזיכרון מרכזי תאי T, וקידם את הרגרסיה המשמעותית של גידולים. בשנת 2019, Xu et al.135 בנו חיסון ננו נוסף המאפשר הצגה צולבת על ידי העמסת OVA ו-CpG-ODN על דנדרמר דופמין פוליאמיד שעבר שינוי בחומצה גואנידינו בנזואית (DGBA). חיסון ננו זה גרם לחסינות תאית חזקה ספציפית לאנטיגן ומנע את האתגר מחדש של מלנומה B16-OVA. יתרה מכך, חיסון ננו זה הוכיח יעילות אנטי-סרטנית חזקה נגד מלנומות B16-OVA בשילוב עם אסטרטגיית ICB של aPD-1. בעקבות הבשלת טכנולוגיית הזיהוי של ניאו אנטיגנים, ניאו אנטיגנים לסרטן משמשים כעת לניסוח חיסוני ננו לסרטן. ננו-דיסקים מצופים בניאו-אנטיגן ו-CPG-ODN הוכחו כמועשרים באיברים לימפואידים ומושרים עד פי 47-יותר CTLs ספציפיים לניאו-אנטיגן מאשר חיסונים מסיסים136. בנוסף, השימוש בבקטריופאג'ים T7 כננו-נשאים לביטוי של ניאו-אנטיגנים יכול להשיג חיסוני ננו המכילים ניאו-אנטיגנים מגוונים. חיסוני ננו אלה העלו טיטרים גבוהים של נוגדנים אנטי-ניאונטיגנים ותגובות תאי B.

איור 5 ליפוזומים המעגנים את IL-2-התמזגו Fc ונוגדן CD137 אגוניסטי הביאו לחסינות אנטי סרטנית ללא רעילות מערכתית. (א) תמונת Cryo-TEM של IL-2-Fc-ליפוזום (ליפוזומים נגד CD137 היו דומים). (ב) ספירת תאי T CD8þ נקבעה בעקבות טיפול בתאי T רב שבטיים מעכברי C57Bl/6 עם IL-2-Fc מסיס או ליפוזומלי (10 ng/mL של חלבון). (ג) נותח IFN-g המופרש ולאחר מכן הודגרו תאי T משופעלים עם אנטי-CD137 או Lipo-aCD137 מסיס (ריכוז aCD137 האחרון: 10 מ"ג/מ"ל). (ד) קטעים קפואים של הגידול לאחר הזרקות של Alexa-568-מסומנים aCD137 ו-IL-2-Fc ו-Lipo-aCD137 þ Lipo-IL2-Fc. (E) גדלי גידול בעכברי C57Bl/6 לאחר טיפול ב-aCD137 þ IL-2-Fc, Lipo-aCD137 þ Lipo-IL-2-Fc, או Lipo-IgG. (ו) תמונות ביולוגיות של עכברי C57BL/6 הנושאים גידולי B16F10 המבטאים לוציפראז, לאחר טיפול ב-Lipo-aCD137 þ Lipo-IL-2-Fc או Lipo-IgG. נדפס מחדש באישור מ-Ref. 115. זכויות יוצרים ª 2019 Nature Publishing Group.

איור 6 ננו-חלקיק אימונותרפי כפול המכוון ל-PD-1 ו-OX40 שיפרו את החסינות האנטי-סרטנית. (א) סכימה של שיפור בסיוע DINP של אימונותרפיה משולבת. (ב) תמונות של ננו-חלקיקים לפני ואחרי צימוד נוגדנים (סרגל קנה מידה: 100 ננומטר). (ג) גודל גידול ועקומות הישרדות של עכברי C57BL/6 עם גידולי B16F10 בעקבות טיפול בתרופות שונות. (ד) תמונות אימונופלואורסצנטיות של גידולים לאחר טיפול בתרופות שונות. נדפס מחדש באישור מ-Ref. 123. זכויות יוצרים ª 2018 WILEY-VCH Publishing Group.
3.2. חומר פונקציונלי כמשרה ICD
הסוגים והתפקודים של ננו-חומרים מגוונים. הם יכולים לשמש כנשאי תרופות (כגון ליפוזומים, סיליקון מזופורי ופולימרים), ויש להם גם פונקציות שונות, כגון השפעות פוטותרמיות, השפעות פוטודינמיות, השפעות קינטיות כימיות, השפעות מגנטו-תרמיות והשפעות שיפור קרינה. חלק מננו-חומרים בעלי פונקציות אלה הוכח כגורם ל-ICD בתאים סרטניים, ובכך משחרר אנטיגנים של גידול ו-DMAPs151. השילוב של ננו-חומרים אלה עם אימונותרפיה מסורתית, כגון אימונוסטימולנטים וטיפול בנקודת ביקורת חיסונית, יש לו פוטנציאל לקדם ביעילות מספר שלבים של מחזור החסינות לסרטן ובסופו של דבר להשיג אפקט אנטי-סרטני טוב יותר. החלק הבא של סקירה זו יציג ננו-חומרים פוטותרמיים, פוטודינמיים, רדיותרפיים, המודינמיים ואחרים פונקציונליים, וידון ביישומם באימונותרפיה של סרטן על בסיס מחזור החסינות לסרטן.

יתרונות cistanche לגברים - מחזקים את המערכת החיסונית
3.2.1. ננו-חומר פוטררמי
סוכנים פוטותרמיים (PTAs) הופכים אנרגיית אור לאנרגיה תרמית. ננו-חומרי PTA מחולקים בדרך כלל לחומרים אנאורגניים על בסיס מתכת, חומרים אנאורגניים על בסיס פחמן, חומרים על בסיס זרחן, סוכנים פולימריים ו-PTAs חדשים אחרים152e154. PTAs אנאורגניים מבוססי מתכת כוללים חומרי מתכת אצילים קונבנציונליים (כולל Au, Ag, Pd ו-Pt) וחומרים מוליכים למחצה (המכילים CuS, MoS2 ו-WS2). PTAs אנאורגניים מבוססי מתכת מסונתזים בקלות עם גדלים וצורות מתכווננים אך יש להם חסרונות כמו קצב חילוף חומרים איטי ופרופילי רעילות לטווח ארוך לא ברורים. PTAs אנאורגניים מבוססי פחמן מורכבים בעיקר מגרפן, ננו-צינוריות פחמן ופולרן. בעוד PTAs אנאורגניים מבוססי פחמן יש יעילות ויציבות המרה פוטו-תרמית גבוהים, יש להם פוטנציאל לגרום לדלקת ריאות וקשה לייצר אותם בקנה מידה גדול. PTAs מבוססי זרחן, ננו-חומרים שפותחו לאחרונה, מכילים זרחן שחור דו מימדי ונקודות קוונטיות זרחניות שחורות. ל-PTAs מבוססי זרחן יש יעילות המרה פוטו-תרמית גבוהה ותכונות פירוק ביולוגי מצוינות. עם זאת, נותרו לפתור בעיות עם יציבות, ייצור בקנה מידה גדול ויכולת אחסון. יתר על כן, הרעילות החריפה וההשפעות החיסוניות הקשורות ל-PTAs מבוססי זרחן עדיין לא ברורות. PTAs פולימריים, כולל פוליפירול (PPy) ופולידופמין (PDA), מסונתזים בקלות עם משקלים מולקולריים מתכווננים. לגבי PTAs חדשניים אחרים, נוצרו מספר חומרים דו-ממדיים עם יעילות המרה פוטו-תרמית גבוהה, כגון C3N4 ו-MXenes עם הנוסחה הכללית Mnþ1Xn. ב-Mnþ1Xn, M מציין מתכת מעבר (Ti, V, Ta, Nb, Mo ו-Zr) ו-X מייצג C או N. ה-PTAs המתאימים ל-PTT באימונותרפיה של סרטן צריכים לעמוד בדרישות הבאות: (1) המרה פוטו-תרמית גבוהה יחסית יעילות כדי למנוע נזק לייזר לרקמה רגילה; (2) תאימות ביולוגית מעולה ופירוק ביולוגי כדי למנוע רעילות מערכתית; ו-(3) קליטת אור באזור ה-NIR, שהיא אופטימלית בחלון ה-NIR השני (NIR-II) (1000e1350 ננומטר). עד כה, טיפולים פוטותרמיים מתפקדים כשני מודלים: PTT בטמפרטורה גבוהה ו-PTT בטמפרטורה נמוכה. עבור PTT בטמפרטורה גבוהה, רקמות סרטן מובטלות בטמפרטורות העולה על 50 C155. טמפרטורה גבוהה והעברת חום עלולים לפגוע ברקמה נורמלית סמוכה156. בדרך כלל, תאי יונקים מגיבים להלם חום על ידי ביטוי יתר של חלבוני הלם חום (HSPs), כגון HSP70 ו-HSP90. לכן, המחקר התמקד ברגישות של תאים סרטניים ל-PTT בטמפרטורה נמוכה על ידי עיכוב הביטוי והפעילות של HSPs157. מחקרים אחרונים אישרו כי PTT יכול לגרום ל-ICD בתאי סרטן144. הטמפרטורה הגבוהה יותר שנגרמה על ידי הקרנה הביאה למוות תאים יעיל יותר. עם זאת, סמנים ביולוגיים של ICD לא עלו עם עליית הטמפרטורה. סמני ICD, כגון שחרור ATP, שחרור HMGB1 וביטוי קלרטיקולין, הופיעו בתדירות גבוהה יותר ב-63.3e66.4 C מאשר בטמפרטורות גבוהות יותר (83.0e83.5 C) ונמוכות יותר (50.7e52.7 C). יתרה מכך, חיסון לאחר מכן עם נוירובלסטומות שונות שטופלו ב-PTT אישר את הממצאים במבחנה. אתגר עכברים מחוסנים עם תאי נוירובלסט טומא בתוך חלון טמפרטורה אופטימלי הביא לשיפור ההישרדות לטווח ארוך בהשוואה לקבוצות טמפרטורה גבוהות או נמוכות יותר. עם זאת, קשה לעורר תגובה חיסונית חזקה אנטי סרטנית רק בהתאם לאימוגניות של אנטיגן הנובעת מ-ICD המושרה על ידי PTT. לכן, ננו-חומרי PTA משולבים לעתים קרובות עם אסטרטגיות חיסוניות מסורתיות אחרות כדי לשפר את התוצאות של אימונותרפיה בסרטן. ניצול של ננו-צינוריות פחמן כ-PTA, בשילוב עם מתן סיסטמי של נוגדן אנטי-CTLA-4 עיכב ביעילות סרטן רחוק וגרורות סרטן תחת הקרנה159. ננו-חלקיקי CuS חלולים המצופים בצ'יטוזן וב-CpG-ODN נמצאו כמפעילים תאי NK ו-DCs ברקמות סרטניות ומנקזים בלוטות לימפה, מה שמוביל לעיכוב של סרטן מקומי ומרוחק160. לאחרונה, תאים יונקים נוצלו ליצירת באתרו של PTAs, Au nanoparticles (AuNPs). טיפול בתאי B16F10 עם HAuCl4 גרם ליצירה תוך תאית של AuNPs. לאחר אקסוציטוזיס, AuNPs הוכנסו לממברנות B16F10 המכילות אנטיגנים מגוונים של גידול. לאחר מכן, התאים AuNP@B16F10 הודגרו עם תאי DC2.4 כדי לקשט עוד יותר את קרום DC וליצור AuNP@DCB16F10. מתן AuNP@DCB16F10 לעכברים הנושאים B16F10- עיכב באופן משמעותי את התפתחות הסרטן והפעיל תאי DC ו-CD8þ לאחר הקרנה161 (איור 8). למרות ש-PTT מתווכת ננו-חומר נעשה שימוש נרחב במחקר בסיסי בשל תכונתו הלא-פולשנית, עדיין אין יישומים קליניים מוצלחים. ניתן לסכם את המכשולים של PTT בתיווך ננו-חומר בטרנספורמציה קלינית לשש קטגוריות. (1) המגבלות הנגזרות מהתכונות החומריות של רוב הננו-חומרים כוללות יציבות ופיזור דם לקויים, יכולת מחזור מוגבלת ארוכה, העשרת כבד ודלקת ותהליך פרמקוקינטי לא ברור. (2) המגבלות של PTAs מבוססי ננו-חומר, כוללות יעילות פוטותרמית נמוכה ויציבות צילום ירודה, במיוחד עבור PTAs מבוססי זהב. (3) המכשולים הנובעים מתהליך הקרנת האור, לרבות רעילות קלה וחדירת רקמה שטחית. (4) איזו טמפרטורה מועילה לתהליך ICD? האם יש עיקרון כללי לכל ה-PTAs מבוססי ננו-חומרים (5) הגבלת הידע על תהליך ה-ICD המושרה על-ידי PTT בעזרת ננו-חומרים, למשל, האם כל ה-PTT הנעזר בננו-חומרים גורם ל-ICD של תאים סרטניים וכיצד להעריך ולחזות היכולת של PTAs מבוססי ננו-חומר לגרום לתהליך ICD. (6) עוצמת תהליך ה-ICD המושרה על ידי PTT בסיוע ננו-חומרים אינה מספיקה כדי להניע מחדש את מחזור החסינות לסרטן, והשילוב של PTT בסיוע ננו-חומרים עם אימונותרפיה אחרת לסרטן הוא הכרחי, מה שמגביר את המורכבות של מערכת הטיפול.

איור 7 טיפול פוטותרמי עם ננו-חלקיקים מסייעים למערכת החיסון גרם לחסינות אנטי-סרטנית. (א) סכימה של ננו-חלקיק אדג'ובנטי חיסון שנבנה על ידי PLGA עמוס ב-ICG ו-R837 והשפעתו על מערכת החיסון. (ב) נפח גידול של גידולים מרוחקים 4T1 ו-CT26 בעקבות הטיפול המצוין בגידול הראשוני. (ג) ספירת תאי T CD4þ ו-CD8þ של גידולים מרוחקים בעקבות הטיפול המצוין בגידול הראשוני. נדפס מחדש באישור מ-Ref. 145. זכויות יוצרים ª 2016 Nature Publishing Group.
3.2.2. ננו חומר פוטודינמי
ב-PDT, חומרי רגישות פוטו (PSs) יכולים לספוג פוטונים ולהפוך אותם ממצב קרקע למצב נרגש. במצב נרגש, ה-PS בדרך כלל לא יציב ומעביר בקלות אלקטרוניקה עתירת אנרגיה למצעים אחרים. בתגובות מסוג I, PS במצב נרגש, מגיב עם קרום התא או ביומולקולות אחרות ליצירת רדיקלים, אשר מגיבים עוד יותר עם O2 ליצירת מוצרים מחומצנים. בתגובות מסוג II, PS במצב נרגש מגיב ישירות עם O2 ליצירת חמצן יחיד, שהוא ROS162 פעיל מאוד (איור 9). לכן, תפוקת PDT קשורה קשר הדוק לריכוז O2. בסביבת גידול היפוקסי, קשה להפגין יעילות גבוהה עם PDT. למרות ש-PDT הופיע בשנות ה-1970 ושימש בהצלחה לטיפול בסוגי סרטן שטחיים, הפעלה חיסונית בתיווך PDT אושרה בסוף המאה ה-20, והטיפולים עדיין בפיתוח163e165. במחקרים עדכניים יותר, הוכח כי PDT הוא שיטה יעילה להשראת ICD בתאי סרטן166,167. יש לציין כי נראה כי ROS נדרשים עבור ICD מכיוון שהאימונוגניות של התהליך מעוכבת במידה רבה בנוכחות נוגדי חמצון. ה-PS של PDT כולל צבעים אורגניים וננו-חומרים. לצבעים אורגניים יש כמה חסרונות מהותיים, כולל הידרופוביות, עומק חדירה נמוך וסגוליות נמוכה לתאים סרטניים. שימוש בננו חומרים כנשאים עבור PSs אורגניים יכול להתגבר על מספר החסרונות שלהם, ותוכן קשור הוצג בסעיף 3.1.3. כאן נציג ננו-חומרים בעלי יכולת מהותית לעורר תהליכים פוטודינמיים ויישומם באימונותרפיה של סרטן. ננו-חומרי PDT נפוצים כוללים ננו-חומרים מתכתיים אצילים, ננו-חומרים מבוססי פחמן, זרחן שחור ומסגרות מתכת-אורגניות בקנה מידה ננו-מטרי (MOFs)168. בקצרה, ננו-חומרים מתכתיים אצילים מיוצגים על ידי ננו-חלקיקי זהב וכסף. ננו-רודי זהב, למשל, דווחו שהם מייצרים חמצן בודד תחת אור NIR ב-915 ננומטר, שהרס גידולי מלנומה B16F0 במודל של עכבר. בנוסף, ננו-רודי זהב אלה גרמו לעלייה בטמפרטורה סביב רקמות סרטן בעקבות הקרנה באור NIR ב-780 ננומטר 169. המעבר באור עירור יכול לשנות את המודל הטיפולי בין PTT ל-PDT. ננו-חומרי PS מבוססי פחמן מכילים ננו-צינוריות פחמן, פולרנים ונקודות קוונטיות של גרפן. PS מקורי המבוסס על פחמן מייצר חמצן יחיד מוגבל תחת קרינת NIR. עם זאת, סימום ושינוי פני השטח יכולים להעניק ל-PS מבוסס פחמן יעילות המרה קוונטית מעולה תחת הקרנת NIR170e172. זרחן שחור עם פער פס מתכוונן, תאימות ביולוגית מעולה ופירוק ביולוגי יושם לראשונה כ-PS בשנת 2015. זרחן שחור הפגין תפוקה קוונטית של כ-0.91 של חמצן בודד בהקרנה של 660 ננומטר וגרם למוות משמעותי של תאים ודיכוי גידול173. MOFs המורכבים עם PSs אורגניים בתור ליגנדים, ויוני מתכת (Hf, Fe, Zn ו-Zr יוני) כמרכזי מתכת, הוכחו לתפקד כננו-חומר PS174,175. לדוגמה, נגזרת פורפירין חדשה, 5,15- di (p-benzoato) פורפירין (H2DBP) הגיבה עם HfCl4 באמצעות תגובה סולווותרמית ליצירת מבנה DBP-UiO MOF. ה-DBP-UiO-O MOF הראה יעילות PDT משופרת וחסל סרטן בכמחצית מהעכברים לאחר מתן יחיד, וחשיפה אחת לקרינה של 640 ננומטר176. מחקר שלאחר מכן פיתח MOF מבוסס כלור על ידי החלפת H2DBP ב-5,15-di (p-benzoate)-chlorin (H2DBC) כדי להשיג DBCUiO, שהיה לו עירור לאדום ומקדם הכחדה 11- גדול יותר בהשוואה ל- DBP-UiO177. בהשוואה ל-PTA, הסוגים ופוטנציאל היישום של ננו-חומרי PS הנוכחיים מוגבלים. רוב ננו-חומרי ה-PS נרגשים באור נראה או באזור NIR-I, מה שמגביל את עומק חדירת הרקמה. ננו-חומרי PDT לעירור שני פוטונים מספקים פתרון לקרינת NIR-II178. עירור קונבנציונלי של פוטון אחד של PSs סופג פוטון בודד כדי להפעיל PSs. עם זאת, PSs לעירור שני פוטונים מסוגלים לספוג שני פוטונים בעלי אנרגיה נמוכה בו זמנית כדי להשיג את אנרגיית פער הלהקה של PSs בסכום של שתי אנרגיות הפוטונים. עירור שני פוטונים מאפשר חדירה עמוקה יותר לרקמות והפחתת צילום של PSs. לדוגמה, CdSe QDs שימשו כננו-חומרים לעירור שני פוטונים שניתן לעורר תחת לייזר של 1100 ננומטר ולפלוט פוטונים באורך גל של 635 ננומטר. הסיליקון phthalocyanine 4 (Pc 4) המצומד על CdSe QDs היה מסוגל לספוג פוטונים של 635 ננומטר ותפקד כ-PS באמצעות תהליך FL FL (FRET) בין QD ל-Pc 4179. למרות שננו-חומרי PS קיימים יכולים לעכב בעוצמה סרטן מקומי. , מניעת סרטן רחוק וגרורתי תלויה בשילוב עם טיפולים אימונותרפיים אחרים לסרטן. לדוגמה, Fe-TBP MOF נבנה מ-[Fe3O(OAc)6(H2O)3] OAc והליגנד 5,10,15,20-tetra (p-benzoate) porphyrin (TBP). Fe3þ יכול לקיים אינטראקציה עם H2O2, שנמצא בשפע ברקמות סרטן, כדי ליצור O2 ולהקל על היפוקסיה ברקמות הסרטן, וכתוצאה מכך יעילות PDT משופרת. Fe-TBP בשילוב עם aPD- 1 עיכבו גם סרטן ראשוני מקומי וגם סרטן רחוק באמצעות השפעות אבסקופליות180. לאחרונה, ננו חלקיקים פולי (g-glutamic acid) @glucose oxidase @carbon dot ננו ושולבו עם aPD-1. ננו-חומר זה יצר O2 מ-H2O2 תחת קטליזה של Mn2þ ו-PDT מבוסס נקודות פחמן מתווך, מה שגרם עוד יותר לתגובה חיסונית אנטי-סרטנית נגד גידולים מרוחקים מטופלים ולא מטופלים181. בהשוואה ל-PSs אורגניים קונבנציונליים, PDT תפקודי בתיווך ננו-חומר נדיר יחסית. הפיתוח של ננו-חומרי PDT שמקורם ב-NIR-II עם תאימות ביולוגית מעולה ופירוק ביולוגי עשוי לספק הזדמנויות חדשות ל-PDT. מלבד המגבלות הכלליות של ננו-חומרים, PDTowns בסיוע ננו-חומרים המכשולים הייחודיים שלה. ראשית, יש לו פוטוטוקסיות ועומק חדירת רקמות ירוד, שהן בעיות נפוצות בטיפול בהקרנות פוטו. שנית, יש צורך בספיגה תוך-תאית טובה יותר של ננו-חומרי PDT, שכן ה-ROS המיוצר ב-PDT פעיל ויעיל רק בטווח הננומטר. שלישית, זה אמור להשיג איזון בין תהליך PTT ו-PDT המושרה על ידי ננו-חומרים, שכן לננו-חומרים רבים יש את היכולת להמיר פוטונים לחום ולרדיקלים חופשיים עתירי אנרגיה בו-זמנית. רביעית, O2 נחוץ ל-PDT והיפוקסיה ברקמות סרטן פוגעת ביעילות של PDT. עם זאת, אספקת O2 עם PS מבוסס ננו-חומר מסבך את מערכת התרופות ואינה ברת קיימא.
3.2.3. ננו-חומר רדיותרפיה
רדיותרפיה היא טיפול בוגר לסרטן. מאמינים כי חלק מהננו-חומרים משפרים את השפעת הקרנות. בשילוב עם יכולת המיקוד שלה לסרטן, רדיותרפיה מבוססת ננו-חומר יכולה להפחית את הנזק לרקמות הרגילות שמסביב182. ננו-חומרים משופרים בקרינה מורכבים בדרך כלל מאלמנטים בעלי Z גבוה. גורמי הרגישות לרדיו הרווחים ביותר הם ננו-חלקיקים על בסיס זהב184. חומרי רגישות לרדיו אחרים שנחקרו כוללים NPs185,186 מבוססי לנתניד, ננו-חלקיקי Bi2Se3187 וננו-חומרי MOF מבוססי Hf188,189. ננו-חלקיקים אלה גורמים לרגישות לרדיו הוכחו כמשפרים את היעילות של טיפול בקרינה על ידי שיפור ההשפעות הפוטואלקטריות והקומפטון, אשר מגבירים עוד יותר את פליטת האלקטרונים המשניים ואת ייצור ה-ROS. במהלך טיפול רדיותרפיה, רדיקלי DNA צריכים להגיב עם O2 כדי לגרום להפסקות כפולות של DNA. לכן, הסביבה ההיפוקסית של רקמות הסרטן מחלישה את ההשפעות האנטי-סרטניות של הקרנות. כדי לעקוף את המיקרו-סביבה ההיפוקסית, רגישים לרדיו מלווים בדרך כלל במולקולות אספקת O2, כגון ננו-חלקיקי MnO2 או פחמנים פר-פלואוריים. לדוגמה, core-shell Au@MnO2-PEG נבנה כדי לשלב אטומים עם רגישות רדיו-Z גבוהה ומחוללי O2. ליבת Au, גורם רגיש לרדיו ידוע, יכולה לשפר את הייצור של רדיקלי DNA. ל-MnO2 יש את היכולת לפרק H2O2 ל-O2 כדי להתגבר על עמידות המתווכת בהיפוקסיה לרדיותרפיה190. בנוסף, ננו-חלקיקי Bi2Se3 חלולים מצופים ב-perfluorocarbon הוכחו כמשפרים את יעילות הקרנות באמצעות שלושה מנגנונים: perfluorocarbon, כנשא O2, הפחית את המצב ההיפוקסי בגידולים מוצקים; חלקיקי Bi2Se3, כחומרי רגישות לרדיו עם אטום Z גבוה Bi, שיפרו ביעילות את האפקט הפוטואלקטרי של RT; Bi2Se3 ספג אור NIR ויצר אפקט פוטותרמי כדי להגדיל את עמית הדם הבין-גידולי, ובכך להגביר את הריכוז של O2 ברקמות הגידול191. ההשפעה האבסקופלית, שהוצעה לראשונה ב-1953, מרמזת על התפתחות מערכת החיסון בהקרנות192. מחקרים שלאחר מכן מצאו שטיפול בקרינה יכול להגביר את הביטוי של מולקולות MHC I ו-TAAs, ובכך לגרום להצגת אנטיגן של DCs והפעלה וסחר של תאי T CD8þ193. מחקרים נוספים הראו שטיפול בקרינה הגביר את התגובה החיסונית באמצעות ICD194. שילוב הקרנות עם אסטרטגיות אימונותרפיות אחרות מחזק את התגובה החיסונית ומשרה יעילות אנטי סרטנית סינרגטית. לדוגמה, nMOFs מבוססי Hf עם השפעות רגישות לרדיו גרמו לחשיפה חזקה ל-CRT והפעלה של תאי אפקטור חיסון (כולל תאי DC, CD4þ T, CD8þ T ו-NK), אשר עיכבו עוד יותר את הצמיחה של גידולים ראשוניים ומרוחקים. יתרה מכך, שילוב של nMOFs מבוססי Hf עם aPD-L1 שיפר בבירור את התגובה החיסונית וכמעט חיסל את הגידולים הראשוניים והאבסקופליים188. טיפול בקרינה משיג חדירת רקמות עמוקה יותר מאשר הקרנת צילום. הגירוי החיסוני המתווך על ידי הקרנות מתועד היטב יחסית להקרנת צילום. עם זאת, המיקרו-סביבה ההיפוקסית של הגידול מהווה מכשול לטיפול בהקרנות כדי לייצר מספיק ROS. יתרה מכך, מנגנוני עמידות להקרנות בתאים סרטניים, כמו אנזימי תיקון DNA בעלי וויסות מעלה, מפחיתים את התוצאה האנטי-סרטנית של הקרנות. חוץ מזה, יש צורך להעריך בקפידה את ההשפעה האנטי-סרטנית שהביאה התגובה החיסונית המוגברת ואת העלות של ננו-חומר. יתר על כן, לא ניתן להתעלם מהמגבלות הכלליות של ננו-חומרים בהקרנות.

איור 8 ננו-חלקיקי זהב באתרם שנוצרו ב-B16F10 ו-DCs עבור השילוב של PPT ואימונותרפיה. (א) סכמטי של בנייה ופונקציות אימונולוגיות של AUNP@DCB16F10. (ב) תמונות TEM של AUNP@DCB16F10. (C) שינוי טמפרטורה (DT) של AuNP, AuNP@DCL929 ו-AuNP@DCB16F10. (ד) תמונות המציגות תאים חיים/מתים לאחר טיפול עם AuNP@DCB16F10 או/ו לייזר. (ה) נפח גידול ראשוני לאחר הטיפול המצוין. (ו) משקל גידול מרוחק בעקבות הטיפול המצוין. (ז) התבגרות DC בעקבות הטיפול המצוין. (H) ספירת תאי CD4þ לאחר הטיפול המצוין. נדפס מחדש באישור מ-Ref. 161. זכויות יוצרים ª 2019 ACS Publishing Group.

איור 9 יצירת ROS בטיפולים פוטודינמיים.
3.2.4. ננו חומרים פונקציונליים אחרים
בנוסף לשיפור היעילות של PTT, PDT והקרנות, ננו-חומרים מציגים גם פונקציות אחרות, כולל אפקט כימודינמי, גרימת פרופטוזיס והשפעות היפרתרמיה מגנטית (MHT). האפקט הכימודינמי נגזר בעיקר מתגובת פנטון, המתארת בעיקר את התגובה של Fe2þ עם H2O2 לייצור Fe3þ ורדיקלים הידרוקסיל ($OH) בעלי יכולת חמצון גבוהה. ריכוזים גבוהים של $OH קטלניים לתאים סרטניים. פרט ליונים ברזליים, קטיונים אחרים, כגון Cu2þ, Mn2þ, V2þ ו- Cr4þ, מסוגלים לזרז תגובות דמויות פנטון195. בהשוואה לננו-חלקיקי Fe3O4 יציבים שמשתמשים רק ב-Fe2þ שטחי כדי לזרז את תגובת הפנטון, ננו-חלקיקי Fe אמורפיים (AFeNPs), אשר יהיו יעילים יותר מיוננים תחת מיקרו-סביבה של גידול חומצי וישחררו Fe2þ פעיל, שיפרו את העיכוב של התפתחות סרטן196. למרות ש-H2O2 קיים ברמות גבוהות בהרבה בתאים סרטניים בהשוואה לתאים רגילים, נראה כי H2O2 אנדוגני אינו מספיק כדי לתווך השפעה כימודינמית קטלנית על תאים סרטניים במבחנה. עבור טיפולי CDT רבים, אספקת H2O2 נוספת נחוצה כדי לגרום למוות של תאי סרטן ולנסיגה של הגידול197. לכן, CDT משולב בדרך כלל עם טיפולי סרטן אחרים. לדוגמה, הקבוצה שלנו פיתחה Z-scheme heterojunction עם ליבת FeS2 ו-Fe2O3 מעטפת. גליונות הפיריט המחומצנים תרמית הדו-ממדיים החדשים (TOPY NSs) הצליחו להרוג תאים סרטניים באמצעות צריכת גלוטתיון, תגובת פנטון, PDT בתיווך הטרוג'נקציה ו-PTT. יתר על כן, TOPY NSs כמעט הכחידו גידולי קסנוגרפט HepG2 תחת הקרנה ב-650 ו-808 ננומטר. מכיוון ש-CDT מייצר ROS כמו PDT, הוא עשוי לגרום ל-ICD גם בתאי סרטן. עם זאת, האינטראקציה בין CDT למערכת החיסון דורשת מחקר נוסף. פרופטוזיס הוא סוג חדש של מוות תאי מתוכנת. תחת הפעולה של ברזל דו ערכי או אסטר אוקסיגנאז, הוא מזרז את הביטוי הגבוה של חומצות שומן בלתי רוויות על קרום התא כדי לגרום לחמצן שומנים, ובכך לגרום למוות של תאים. ייצור ה-ROS בפרופטוזיס והטבע הלא-אפופטוטי של פרופטוזיס מרמזים על יכולתו לווסת את מערכת החיסון. Ferroptocide, מוצר טבעי שזוהה לאחרונה, הוכח כגורם ל-ferroptosis באמצעות צימוד קוולנטי על thioredoxin, מרכיב קריטי של מערכת נוגדי החמצון. הפררופטוזיס גרמה לעיכוב של 40% בגידול בעכברי BALB/c 4T1-, אך הייתה לו עיכוב נדיר בעכברים עירומים 4T1-, מה שהציע השתתפות של תאי T ו-B בפרופטוזיס במדיטציה של עיכוב גידולים in vivo198 . הננו-חומרים הגורמים להשפעות כימודינמיות עלולים להפעיל את תהליך הפררופטוזיס מכיוון שתגובת פנטון יכולה ליזום חמצון ליפוזום199. עם זאת, מספר ננו-חומרים שאינם מכילים ברזל דו ערכי מראים את הפוטנציאל לעורר פרופטוזיס. ננו-חלקיקי סיליקה אולטרה-קטנים מסוג PEGylated (כ-6 ננומטר) הוכחו כגורמים ל-ferroptosis בתאים סרטניים חסרי חומרים מזינים. מוות התאים המושרה על ידי ננו-חלקיקי סיליקה עוכב על ידי טיפול בסורקים של שומנים ב-ROS (ליפרוקססטטין-1) או החזרת גלוטתיון באמצעות תוספת של גלוטתיון או N-אצטילציסטאין (NAC). יתרה מכך, הזרקה תוך ורידית של חלקיקי הסיליקה (12 ננומול למנה) עיכבה באופן משמעותי את הצמיחה של גידולי קסנוגרפט 786-O ו-HT-1080 בעכברים עירומים. מינונים תוך-צפקיים של ליפרוקססטטין-1 הפחיתו באופן משמעותי את עיכוב הגידול שנגרם על ידי חלקיקים200. לאחרונה, הוכח כי ננו-בועות מנגן סיליקט עשירות בארגינין (AMSN) מעוררות פרופטוזיס על ידי דלדול יעיל ביותר של גלוטתיון (GSH) ובכך מעוררות את השבתת פרוקסידאזים 4 תלויי גלוטתיון (GPX4). מנגן ב-AMSNs תיווך את דלדול ה-GSH, ושינוי ארגינין מספק יכולת מיקוד לגידול. ה-AMSNs גרמו לעיכוב גידול על ידי מנגנון פרופטוזיס במבחנה ו-in vivo201. לאחרונה, שלפוחית ליבה-קליפה היברידית (HCSVs) נבנתה על ידי שימוש בחומצה אסקורבית (AA) בתור הליבה ו-PLGA כקליפה המעוטרת בננוקוביות תחמוצת ברזל (IONCs). HCSVs גרמו לחשיפה של calreticulin באמצעות תגובת פנטון ומוות תאים דמוי פרופטוזיס לאחר טיפול בשדה מגנטי. יתרה מכך, הזרקה תוך-גידולית של HCSVs הגבירה שגשוג משמעותי של ספלנוציטים, הפעלת DC ב-LNs מפשעתי והפעלת תאי T בגידולים ו-LN202. MHT תלוי בעיקר בחומרים סופר-מגנטיים, שיכולים להשיג מיקוד מגנטי ולהפוך אנרגיה אלקטרומגנטית לתרמית תחת שדה מגנטי מתחלף. בהשוואה ל-PDT ו-PTT, ל-MHT יכולת חדירה עמוקה יותר והוא קשור לרעילות נמוכה יותר לרקמות שמסביב203. חלקיקי Fe3O4 הם הננו-חומרים העל-פארמגנטיים המיושמים ביותר, שיכולים לחמם גידולים מעל 43 C ולעורר את ההפעלה והשגשוג של תאי T CD4þ ו-CD8þ. עיכוב של גידולים דיסטליים ומשניים על ידי ננו-חלקיקי Fe3O4 מעיד על מעורבות מערכת החיסון. ניצול ננו-חלקיקי Fe (FeNPs) כסוכני MHT, מתן מקומי של PLGA-R837 וניהול סיסטמי של חסימת נקודת ביקורת aCTLA-4 נמצאו כמונעים ביעילות גרורות סרטן205. לסיכום, ננו-חומרים פונקציונליים המעוררים השפעות פוטותרמיות, פוטודינמיות, רגישות לרדיו, כימודינמיות, פרופטוטיות ומגנטיות, מראים פוטנציאל רב לגרום לתהליך ה-ICD של תאים סרטניים שבהם תאים סרטניים גוססים יכולים לשחרר אנטיגנים של גידול ולהציג אותות אימונוסטימולטוריים להפעלת ה-APCs. . מחוללי הננו הפוטנציאליים של ICD מסוכמים בטבלה 4. לגבי ננו-חומרים פונקציונליים רבים, נותר לחקור האם הם מעוררים ICD של תאים סרטניים והאם חוזק ICD מספיק כדי להפעיל מחדש את מחזור החסינות לסרטן. בנוסף, קשה להסביר מספר קטן של דיווחים על ננו-חומרים פונקציונליים המעוררים ICD וכל הננו-חומרים הפונקציונליים מאותו סוג יכולים לגרום ל-ICD. עם זאת, היעדר אפיון סטנדרטי ומחקר על תהליך ICD המתווך על ידי ננו-חומרים מעכב את האופטימיזציה הרציונלית של מחוללי ננו של ICD.
טבלה 4 מחוללי ננו פוטנציאליים של ICD

3.3. תוספים אימונומודולטורים
אדג'ובנטים הם מרכיבים חיוניים של חיסונים מודרניים, אשר מחזקים ו/או מעצבים את התגובה החיסונית נגד פתוגנים או ממאירות. בתחום החיסונים לסרטן, חיוני להפעיל חסינות תאית חזקה נגד אנטיגנים של גידול. ננו-חומרים בגדלים שונים, צורות ושינויי פני השטח עשויים לתפקד כעזרים באמצעות המנגנונים הבאים206: משלוח ושחרור עקבי של אנטיגנים, מיקוד ל-APC בצורה פסיבית או אקטיבית, אספקה ציטוזולית של אנטיגנים כדי לשפר את ההצגה ההולכת של APC, ו לווסת את התגובה החיסונית. השימוש בננו-חומרים כפלטפורמות מסירה להובלת אנטיגנים של גידול לאיברים חיסוניים ולציטופלזמה של DCs מתואר בסעיף 3.1.3. כאן, נדון בהשפעות האימונומודולטוריות של ננו-חומרים ויישומם באימונותרפיה של סרטן. ההשפעות האימונומודולטוריות של ננו-חומרים כוללות בעיקר הפעלה של דלקת, הפעלת מערכת משלימה וגיוס של תאי חיסון207. תוספי אלום, הנמצאים בשימוש קליני נרחב, הוכחו כגורמים להפעלת דלקת דלקת של NLPR3. בחשיפה לסכנה, כגון פתוגנים, DAMPs או PAMPs, NLPR3 וחלבונים קשורים אחרים יקיימו אינטראקציה עצמית ליצירת קומפלקסים בעלי משקל מולקולרי גבוה המעוררים חיתוך אוטומטי של קספאז-1. זה מווסת עוד יותר את הפרשת IL-b ו-IL-18208. בנוסף לאלום, ננו-חומרים רבים הוכחו כגורמים להפעלת NLRP3 inflammasome, כולל ננו-חלקיקי פחמן שחור209, SiO2 210,211 ו-TiO2 ננו-חלקיקים212. Inflammasomes מופעלים בתגובה לאות הסכנה שמספקים ננו-חלקיקים, כגון ערעור ליזוזומלי וייצור ROS. חלבונים משלימים קיימים בסרום ובנוזל הרקמה אצל בני אדם ובעלי חוליות. ניתן להפעיל משלים על ידי קומפלקסים של אנטיגן-נוגדנים או מיקרואורגניזמים, מה שמוביל לתמוגה או פגוציטוזה של מיקרואורגניזמים פתוגניים. מחקרים אחרונים הוכיחו כי אופסונין, סוג של משלים, יכול להיספג על ננו-חלקיקים כדי לתווך זיהוי ואנדוציטוזיס של חלקיקים על ידי תאים פגוציטים. לאחר בליעה על ידי פגוציטים, ננו-חומרים עשויים לגרום לפגוציטים לסנתז ולהפריש ציטוקינים מעוררי דלקת וכימוקינים כדי לגייס תאי חיסון, כגון מקרופאגים, DCs ותאי T. לדוגמה, בשנת 2010, Yang et al.213 דיווחו על [Gd@C82(OH)22]n ננו-חלקיקים, אשר גרמו לייצור ציטוקינים (כולל IL-12p70), ביטוי מולקולה מעוררת וביטוי מולקולת MHC ב-DCs. יתר על כן, עכברים שחוסנו עם OVA ו-[Gd@C82(OH)22]n הציגו תגובה חיסונית חזקה של Th1. בשנת 2017, Luo et al.214 בנו חלקיקי PC7A פולימריים חדשים, שהיו רגישים ל-pH במיוחד ובעלי קטרים של 20e50 ננומטר למיקוד בלוטות לימפה. שימוש ב-PC7A כנשא ללא חומרים מעוררי חיסון אחרים כדי להעביר אנטיגנים של גידולים לבלוטות הלימפה עיכב בעוצמה את הצמיחה של מלנומה וסרטן המעי הגס. ננו-חלקיקי PC7A אלה הוכחו כמווסתים את התגובה החיסונית, כולל קידום התבגרות DC דרך מסלול STING. בדרך כלל מתעלמים מהפונקציה הרגולטורית של ננו-חומרים ביישום של ננו-חומרים לאספקת תרופות. לאחרונה, הושגה הסכמה על כך שהרבה ננו-חומרים משפיעים על מערכת החיסון. ההשפעה על התגובה החיסונית של ננו-חומרים היא מגוונת. למרות שהצגנו בעיקר את ההשפעה האימונוסטימולטורית של ננו-חומרים, דווחו ננו-חומרים אחרים שעוררו דלקת או דיכוי חיסוני. יש לצבור כמות גדולה של הערכה חיסונית של ננו-חומרים. הקשר בין המבנה של ננו-חומרים לבין תפקוד אימונו-רגולציה נותר לחשוף.

איור 10 NIR הפעיל טיפול קומבינטורי PDT עם חסימה של נקודת ביקורת חיסונית. (א) סכמטי המציג את הפונקציה האנטי סרטנית של UCNP-Ce6-R837. (ב) נפח הגידול של גידולי CT26 ראשוניים ומרוחקים לאחר הטיפול המצוין; רמת תאי CD8þ CTL (C), תאי Treg (D), ויחס CD8þ CTL/Treg (E) בגידולים מרוחקים, ורמות ציטוקינים IFN-g בסרה (F) מעכברים בעקבות הטיפול המצוין. נדפס מחדש באישור מ-Ref. 215. זכויות יוצרים ª 2017 ACS Publishing Group.
3.4. אימונותרפיה קומבינטורית לסרטן המתאפשרת על ידי ננו-חומרים
טיפולים אימונותרפיים משולבים הפועלים בו-זמנית על המרכיבים השונים שפורטו לעיל, או על שלבים שונים במחזור החסינות לסרטן, יש אפשרות מוגברת לעורר חסינות תאית חזקה ספציפית לאנטיגן. לננו-חומרים, הפועלים כנשאים, מעוררי ICD וחומרים אימונומודולטורים, יש פוטנציאל לשלב פונקציות אנטי-סרטניות שונות בפלטפורמה אחת ולהשיג תוצאות אנטי-סרטניות יעילות יחסית. בתחילה, ננו-חומרים שימשו להעברת אנטיגנים לגידול וחומרים אימונוסטימולטוריים לפיתוח חיסונים אנטי סרטניים חזקים בשילוב עם אימונותרפיות. לדוגמה, Xu et al.127 בשנת 2013 בנו חלקיקי lipid-calcium-phosphate (LCP) שהשתנו עם מנוז ל-DCs מטרה, אשר הועמסו יחד עם פפטיד חלבון 2 (Trp 2) הקשור לטירוזינאז כאנטיגנים למלנומה ו-CPG ODN כ. תוסף. לאחרונה, נעשה שימוש בננו-חומרים המצוידים במשרצים של ICD וחומרים אימונוסטימולטוריים בשילוב עם טיפולי ICB. לדוגמה, בשנת 2017, Chen et al.145 הכינו ננו-סיסטם המורכב מ-PLGA עמוס ב-ICG ו-R837. ICG יצר אפקט פוטותרמי חזק, שתווך את שחרור אנטיגנים של גידול. R837, אגוניסט TLR-7 חזק, מופעל בעוצמה של DCs. ניצול של PLGA כדי לספק שיתוף ICG ו-R837 הוכח כגורם להשפעה החזקה ביותר על התבגרות DC וייצור TNF-a תחת הקרנה של 808 ננומטר. לאחר טיפול משולב עם aCTLA-4, PLGA-ICG-R837 עם הקרנת לייזר כמעט חיסל גידולים מרוחקים של xenograft 4T1 ו-CT26, ועיכבה ביעילות את הגרורות וההישנות של הגידולים. העיכוב של צמיחת סרטן, גרורות וחזרה הוגבר על ידי הפעלה ושגשוג של תאי T CD4þ ו-CD8þ, והפחתה של תאי Treg. לאחר מכן, Xu et al.215 בנו ננו-מערכת רב-תכליתית המשלבת ננו-חלקיקים (UCNPs), Ce6, R837 ו-aCTLA-4. ה-UCNPs שונו עם פולימרים אמפיפיליים לטעינת Ce6 ו-R837. UCNPs הצליחו לספוג אור ב-980 ננומטר ולפלוט אור ב-550 ננומטר כדי להפעיל Ce6 ולייצר ROS. הוכח ש-UCNP-Ce6-R837 מעורר בעוצמה התבגרות DC והפרשת ציטוקינים פרו-דלקתיים תחת הקרנה של 908 ננומטר. יתר על כן, UCNP-Ce6-R837 בשילוב עם מתן סיסטמי של aCTLA-4 עיכבו באופן חזק את הצמיחה של גידולים ראשוניים, מרוחקים וגרורתיים (איור 10).
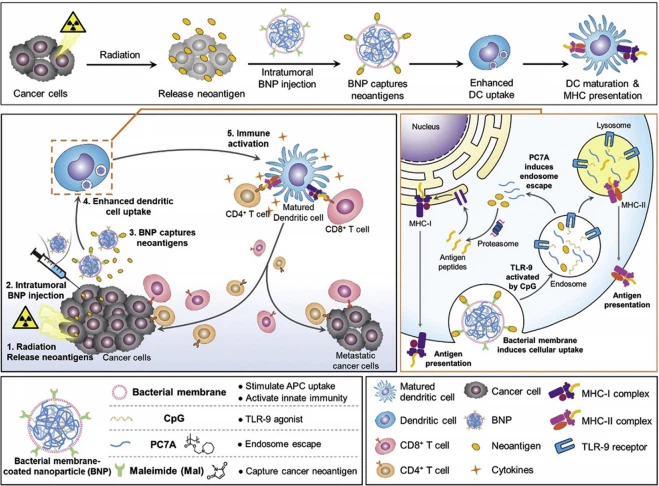
איור 11 חיסון באתרו שנוצר על ידי RT משולב þ BNP. נדפס מחדש באישור מ-Ref. 217. זכויות יוצרים ª 2019 John Wiley and Sons Group.

איור 12 הסכימה של טיפול סרטן משולב בתיווך OSPS. נדפס מחדש באישור מ-Ref. 218. זכויות יוצרים ª 2019 John Wiley and Sons Group.
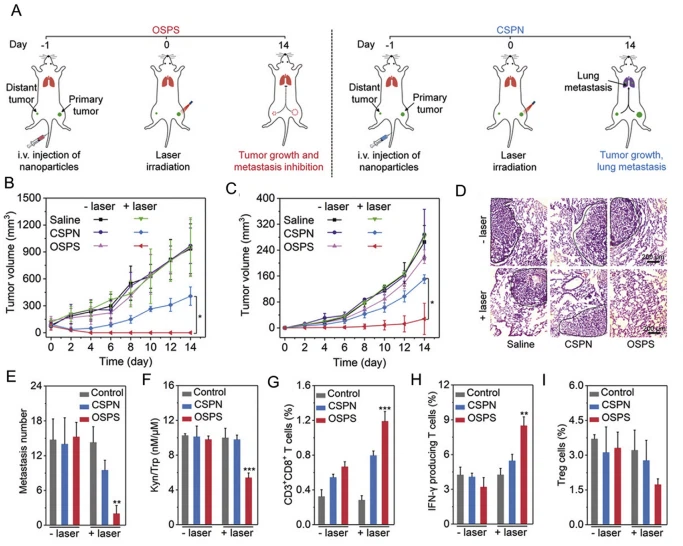
איור 13 תגובה חיסונית אנטי סרטנית הנגרמת על ידי OSPS. (א) עיכוב גידול בתיווך OSPS וגרורות בריאות. (ב) עקומות גדילה של גידולים ראשוניים בעכברים נושאי גידול 4T1. (ג) עקומות גדילה של גידולים מרוחקים בעכברים נושאי גידולים 4T1. (ד) צביעת H&E של גרורות בריאות בעכברים נושאי גידולים 4T1. (ה) מספר גושים גרורתיים בעכברים נושאי גידול 4T1 (F) יחס Kyn/Trp בגידולים ראשוניים בעכברים נושאי גידול 4T1. (ז) אוכלוסייה של תאי T CD3þCD8þ בגידולים מרוחקים. (H) תאי T המייצרים IFN-g בגידולים מרוחקים. (I) תאי טרג בגידולים מרוחקים. *P < 0.05, **P < 0.01, ***P < 0.001, n Z 5. CSPN, ננו-חלקיקים ללא NLG919. נדפס מחדש באישור מ-Ref. 218. זכויות יוצרים ª 2019 John Wiley and Sons Group.

תוסף תוסף cistanche-הגברת חסינות
לחץ כאן לצפייה במוצרי Cistanche Enhance Immunity
【בקש עוד】 דוא"ל:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
4. מסקנות
האינטראקציה של סרטן עם מערכת החיסון היא מסובכת. היווצרות גידול דורשת בדרך כלל בדיקה חיסונית ארוכת טווח ומיקרו-סביבה סובלנית למערכת החיסון. לכן, ייתכן שמערכת החיסון של אדם אינה מספיקה בפני עצמה כדי לחסל תאים סרטניים. השימוש בחומרים חיצוניים המניעים מחדש את מחזור החסינות לסרטן בשלב אחד או מרובים הוא הבסיס לאימונותרפיה של סרטן. שחזור מחזור החסינות לסרטן כולל את השלבים המרכזיים הבאים: הפיכת אנטיגנים לגידול זמינים עבור APCs, גרימת הבשלה של APCs, קידום הצגה צולבת של APCs ושיפור המיקרו-סביבה המדכאת את מערכת החיסון. מיקוד במספר נקודות מפתח בו זמנית הוא אמצעי יעיל להתגבר על מנגנוני פיצוי ולקדם חסינות אנטי סרטנית חזקה. ננו-חומרים נמצאים בשימוש נרחב בתחומי האבחון ואספקת התרופות בגלל גודלם, צורתם ומאפייני פני השטח הניתנים לשליטה. פיתוח ומחקר מעמיק על ננו-חומרים מראים כי ניתן להשתמש בננו-חומרים לא רק למתן תרופות, אלא גם בעלי תכונות מגוונות, כגון השפעתם הפוטותרמית, האפקט הפוטודינמי, היכולת לשפר את הקרנות, השפעת היפרתרמיה מגנטית והשפעה אימונומודולטורית. תכונות אלו מאפשרות שימוש בננו-חומרים כפלטפורמה מקיפה לשילוב תרופות או אסטרטגיות מגוונות המתמקדות בשלבים שונים של מחזור החיסוניות הסרטני, מה שמקדם תוצאות נוספות, או אפילו סינרגטיות נגד סרטן. כפלטפורמה מצוינת לאספקת תרופות, לננו-חומרים יש את היכולת לטעון ולשחרר באופן בר-קיימא מספר אימונומודולטורים בו-זמנית לרקמות סרטן או בלוטות לימפה כדי להפעיל בעוצמה את התהליכים השונים של מחזור החסינות לסרטן, כמו אספקת אנטיגנים של גידול, הפעלה של APC ועיכוב. של נקודת ביקורת חיסונית או תא חיסון מווסת מדכא חיסון. כננו-חומרים פונקציונליים, ננו-חומרים מסוגלים להפעיל את תהליך ICD של תאים סרטניים, ובכך לגרום לקליטת אנטיגנים של גידולים אימונוגניים על ידי APC והפעלה של APC. באשר לאימונומודולטורים, ננו-חומרים יכולים לתפקד כאדג'ובנטים ולגרום ישירות להפעלה של דלקת דלקת וייצור ציטוקינים מעוררים להפעלת מערכת החיסון ולהקלה של דיכוי חיסוני. שלושת הפנים של ננו-חומרים הופכים אותם למועמדים מצוינים לוויסות ידני של מחזור החסינות הסרטני. יתר על כן, ננו-חומרים יכולים להיות בעלי תפקידים מרובים בו-זמנית, לדוגמה, ננו-חומרים פונקציונליים מסוגלים לספק אימונומודולטורים מולקולריים קטנים.
