עיצוב ננו-תרופות המבוסס על המאפיינים הפיזיולוגיים של גלוטתיון
May 15, 2023
תַקצִיר:גלוטתיון (GSH) מעורב ומווסת תפקודים פיזיולוגיים חשובים של הגוף כנוגד חמצון חיוני. GSH ממלא תפקיד חשוב באנטי חמצון, ניקוי רעלים, נוגד הזדקנות, חיזוק חסינות, ופעילות אנטי גידולית. כאן, מבוסס על התכונות הפיזיולוגיות של GSH במחלות שונות, כולל בעיקריכולת הפחתה חזקה של GSH, תכולת GSH גבוהה בתאי גידול, והדלדול NADPH כאשר GSSH מופחת ל-GSH, אנו מדווחים בהרחבה על עקרונות התכנון, ההשפעה והבעיות הפוטנציאליות של שונותננו-תרופות בסוכרת, מחלת הסרטן, מחלות מערכת העצבים, בדיקות פלורסנט, הדמיה ומזון. מחקרים אלו עושים שימוש מלא בערך הפיזיולוגי והפתולוגי של GSH ומפתחים שיטות עיצוב מצוינות שלננו-תרופותהקשורים ל-GSH, אשר מראה את המשמעות המדעית החשובה וערך היישום הבולט עבור מחקר המחלות הקשורות ש-GSH משתתף בו או מגיב אליו.
מילות מפתח:גלוטתיון; תכונה פיזיולוגית; ננו-תרופות; סקירה

לחץ כאן כדי לקבל Cistanche לאנטי אייג'ינג
1. מבנה גלוטתיון
גלוטתיון (GSH) התגלה על ידי הופקינס בשנת 1921 [1], והוא תרכובת טריפפטיד הנוצרת מחומצה גלוטמית, ציסטאין וגליצין באמצעות עיבוי קשרי פפטיד. שמו הכימי הוא -L-glutamyl-L-cysteyl-glycine, והנוסחה המולקולרית היא C10H17O6SN3 [2]. ישנם שני סוגים של גלוטתיון, כלומר גלוטתיון מופחת (GSH) וגלוטתיון מחומצן (GSSG). המבנה של GSH מכיל קבוצה מפחיתה פעילה, sulfhydryl (-SH), אשר מתחמצנת בקלות ומתרוקנת. גלוטתיון פרוקסידאז (GSH-Px) יכול לזרז GSH ל-GSSG, בעוד שגלוטתיון רדוקטאז (GSH-R) יכול להשתמש ניקוטינמיד אדנין דינוקלאוטיד פוספט (NADPH) כדי לזרז GSSG ל-GSH. הקבוצה הפעילה העיקרית של GSSG היא קשר דיסולפיד (-SS-). ביוסינתזה של GSH נשלטת ישירות על ידי מערכת הסינתאז, ולא כמו סינתזת החלבון על הריבוזום [3-5]. המבנה הספציפי ונוהל הסינתזה מוצגים באיור 1.
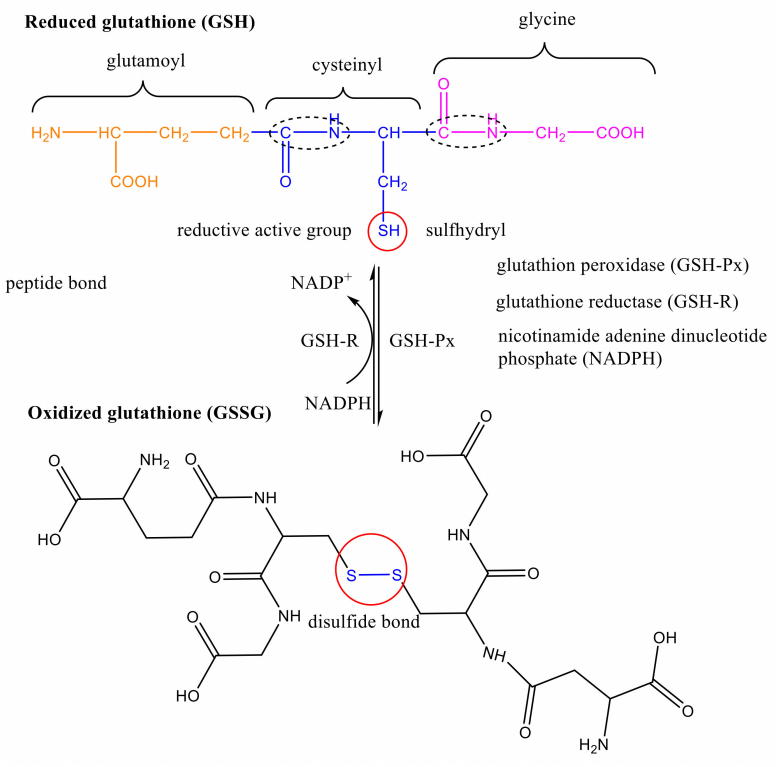
2. תפקוד פיזיולוגי של GSH
GSH נמצא כמעט בכל תא בגוף [6], ומופיע באופן נרחב במגוון של איברים ורקמות חיוניים, כגון דם, כבד וכליה, שבהם הכבד והכליה הם החומרים הסינתטיים, המטבוליים וההפרשות העיקריים. איברים של GSH [7]. באופן כללי, GSH ממלא תפקיד פיזיולוגי חשוב באורגניזמים, בעוד ש-GSSG צריך להיות מופחת ל-GSH כדי להשיג פעילות פיזיולוגית. GSH שומר על תפקוד תקין של מערכת החיסון ויש לו השפעות נוגדות חמצון וניקוי רעלים ברורות. יתרה מכך, המבנה הייחודי של GSH הופך אותו לסורק רדיקלים חופשיים בולט בגוף [8-10]. לכן, ל-GSH יש את היתרונות של תפקידים מצוינים באנטי-אייג'ינג, שיפור חסינות ופעילות אנטי-גידולית [11-13]. כאשר נוצרת כמות קטנה של H2O2 בתא, GSH מפחית את H2O2 ל-H2O עם GSH-Px, תוך שהוא מחומצן ל-GSSG. GSSG מקבל H פלוס ומפחית ל-GSH עם GSH-R, כך שתוכל להמשיך את תגובת הניקוי של רדיקלים חופשיים בגוף, מה שמגן על המבנה והתפקוד של קרום התא מפני הפרעות ונזקים של תחמוצות [14]. בנוסף, ל-GSH יש גם פעילות מקלה על שיכרון מעורר עצבי [15], אשר ניתן להשתמש בה כדי להקל על תגובות הרעילות והלוואי הנגרמות על ידי כימותרפיה בחולים עם גידולים ממאירים [16].

למרות ש-GSH ממלא תפקיד חשוב בתפקודים פיזיולוגיים, נותרו מגבלות משמעותיות, כולל חוסר יכולתו לחדור לקרום התא, חמצון קל, יציבות ירודה וזמינות ביולוגית נמוכה, הפוגעים באופן דרמטי ביעילות הטיפול במחלות. ננוטכנולוגיה היא טכנולוגיה חדשנית לאספקת תרופות אשר הופכת את החומר הפעיל ביולוגית למוטבע או משתנה על הננו-חומרים בעיקר באמצעות מתודולוגיות צימוד פיזיקליות, כימיות ואחרות. ננו-חלקיקים הנוצרים על ידי אנקפסולציה או הרכבה עצמית יכולים לא רק להגן על הפעילות הביולוגית של GSH אלא גם לשפר את היציבות והזמינות הביולוגית שלו. בנוסף, ניתן להשתמש במאפיין ההפחתה החזק של GSH במיקרו-סביבה כדי לפצל ננו-חלקיקים ספציפיים המגיבים לחיזור על מנת להשיג השפעות של שחרור מבוקר ויעד של תרופות. לכן, בסקירה זו, אנו מתמקדים בנפרד בעקרונות התכנון, ההשפעות והבעיות הפוטנציאליות של ננו-תרופות שונות המבוססות על התכונה הפיזיולוגית של GSH במחלות שונות. יתר על כן, האתגרים הנוכחיים ואסטרטגיות עתידיות לפיתוח ננו-תרופות נדונים גם מנקודת מבט של יישום מעשי.
3. מערכות אספקת ננו-תרופות
עם ההשקעה הגבוהה והפיתוח המהיר בשנים האחרונות, ננוטכנולוגיה יושמה בכל תחומי המדע והטכנולוגיה הביו-רפואית [17]. באופן דומה, ננוטכנולוגיה מספקת גישה חדשה לאספקת תרופות, במיוחד מתן תרופות ממוקדות. מערכות אספקת תרופות ממוקדות מספקות תרופות רצויות לחלקים החולים ומפחיתות את ההפצה לרקמות או תאים נורמליים [18]. היתרונות של ננו-חלקיקים כמערכות אספקת תרופות מתוארים באופן הבא: (1) ממיסים תרופות בלתי מסיסות ומונעים פירוק תרופות מהגוף; (2) להאריך את זמן מחזור התרופות; (3) להפגין תאימות ביולוגית טובה ומתכלות; (4) בעלי יכולת העמסת סמים גבוהה ורעילות נמוכה; (4) מתן תרופות באופן סלקטיבי למטרות טיפוליות, כגון רקמת גידול, תאי גידול, תאי סטרומה הקשורים לגידול, ואברוני משנה [19]. עד כה, חומרים רבים כגון פולימרים, ליפידים וחומרים אנאורגניים פותחו והשתמשו בהם כנשאי תרופות כדי לשלוט בהתנהגות השחרור של תרופות [20,21]. בנוסף, גירוי תגובת REDOX מוערך מאוד בטיפול במחלות ונמצא בשימוש נרחב במתן תרופות ננו-רפואיות [22,23]. פוטנציאל REDOX במיקרו-סביבות הם רב-משתנים ברקמות שונות וניתן להשתמש בהם לתכנון מערכות אספקה רגישות ל-REDOX. לכן, התכנון והייצור של ננו-חלקיקים המגיבים לגלוטתיון עשויים להיות גישה מבטיחה למתן תרופות ממוקדות [24].

4. עיצוב ננו-תרופות לסוכרת בהתבסס על המאפיינים הפיזיולוגיים של GSH
4.1. עיצוב ננו-תרופות מבוסס על תפקידו של GSH בלחץ חמצוני
עקה חמצונית אושרה כפתוגנזה דומיננטית לסוכרת, והיפרגליקמיה היא גורם סיכון ראשוני לקידום הייצור של מיני חמצן תגובתיים (ROS). ישנם סוגים מרובים של ROS, כגון אניון סופראוקסיד (O2−), מי חמצן (H2O2), רדיקל הידרוקסיל (OH−), דו תחמוצת החנקן (NO2) וחנקן אוקסיד (NO) רדיקלים חופשיים, וכן הלאה [25]. סדרה של נוגדי חמצון בגוף התקין, כוללות ויטמין A, ויטמין C, ויטמין E, GSH, סופראוקסיד דיסמוטאז (SOD), GSH-Px ו-GSH-R וכו' [26]. ביניהם, GSH הוא חבר חשוב בנוגד החמצון האנדוגני של הגוף. יש לו את היתרונות של ניקוי רדיקלים חופשיים, הקלת נזקים ושמירה על שיווי משקל חיזור בתאים [27]. כאשר הגוף מותקף על ידי רדיקלים חופשיים, GSH יכול לשמש כסורק ישיר של רדיקלים חופשיים, מצע משותף של GSH-Px, קו-פקטור של תגובה אנזימטית וצימוד של תגובות אנדוגניות רבות כדי לשפר את הלחץ והעיכוב החמצוני. התפתחות סוכרת [28].
ראוי לציין כי חוקרים רבים עיצבו תרופות ננו לטיפול בסוכרת ובסיבוכים בהתבסס על התפקיד הפיזיולוגי של GSH בלחץ חמצוני. Wei Wang et al. [29] עיצב ליפוזום גלוטתיון נוגד חמצון חדש (GSH-LIP) ליישום בטיפול בנפרופתיה סוכרתית. GSH-LIP יכול לא רק לשפר את הזמינות הביולוגית של GSH, אלא גם להסיר את עודף ה-ROS שנגרם כתוצאה מלחץ חמצוני ולשפר את יכולת נוגד החמצון. Xiao et al. [30] פיתח מערכת אספקה המורכבת מציסטאין Eudragit L100- אנטרי/ננו-חלקיקים מופחתים של גלוטתיון (Eul-cys/GSH NPs) לאספקה פומית של אינסולין. הם מצאו ש-Eul-cys/GSH NPs יכולים לקדם את ספיגת האינסולין במעיים ולהאריך את זמן הפחתת הסוכר בדם, מה שהצביע על כך ש-Eul-cys/GSH NPs עשוי להיות מערכת אספקה מבטיחה לטיפול בסוכרת. העיצובים הננו-תרופות לעיל של GSH היו שתרופות היו מובלעות בפוספוליפידים או חומרים אמפיפיליים, כגון ליפוזומים ומיצלות, כפי שמוצג באיור 2A. Kuan et al. [31] עיצב את הננו-חלקיקים המגנטיים הקשורים ל-GSH אשר הוכנו באמצעות קישור הקשר הקוולנטי של GSH וננו-חלקיקים. זה הצביע על כך שננו-חלקיק מגנטי זה קשור ל-GSH יכול לשמור על כ-87 אחוז פעילות אנזים ולקבל פפטיד דמוי גלוקגון -1, הורמון פפטיד לטיפול בסוכרת מסוג 2. עיצוב זה של ננו-תרופה שילב SH ב-GSH עם silla-NH2 על ידי קשר קוולנטי, כפי שמוצג באיור 2B. Mottaghipisheh et al. [32] גילה שתמציות S. marianum, B. vulgaris ו-D. sophia המשלבות ננו-חלקיקי CuO הראו השפעה מסוימת על חולדות סוכרתיות, והן יכולות להפחית משמעותית את התוכן של GSH-Px כדי למנוע חמצון GSH. קבוצת המחקר Gurunathan [33] הפעילה חלקיקי Au (AuNPs) לטיפול בסוכרת ופיצתה על הפרצות במערכת ההגנה נוגדת החמצון של הגוף. תוצאות הניסוי הצביעו על כך שרמות ה-GSH, סופרוקסיד דיסמוטאז (SOD), קטלאז ו-GSH-Px עלו באופן משמעותי בחולדות סוכרתיות שטופלו ב-AuNPs, על ידי עיכוב של חמצון שומנים ויצירת ROS במהלך היפרגליקמיה. רוב הננו-תרופות הללו הן אנזימים ננו פעילים הפועלים ישירות על GSH או GSH-Px כדי לווסת את סינתזת GSH, כפי שמוצג באיור 2C.


איור 2. ננו-תרופות לסוכרת מתוכננות על בסיס GSH. (א) GSH הוכנס ל-Enteric eudragit L100-cysteine להכנת ננו-חלקיקים מופחתים של גלוטתיון (Eul-cys/GSH NPs) [30]; (ב) ננו-חלקיקים מגנטיים הקשורים ל-GSH (SPION@silica-NH2). ל-GSH הגיב עם אנהידריד מאלין ליצירת ננו-חלקיקים SPION@silica-GSH [31]; (ג) תמונות מיקרוסקופ אלקטרוני שידור של ננו-חלקיקי CuO ואנזים ננו-חלקיקים Au [32,33]
4.2. עיצוב ננו-תרופות מבוסס על התפקיד של GSH במסלול הפוליאול
כאשר ריכוז הגלוקוז בדם בסוכרת עולה ועולה על היכולת המטבולית הרגילה, הרבה גלוקוז עובר חילוף חומרים דרך מסלול הפוליול. אלדוזה רדוקטאז (AR) במסלול הפוליול מפחית את עודף הגלוקוז לסורביטול על ידי NADPH כקו-פקטור. כמות גדולה של הצטברות סורביטול גורמת לכמות מוגזמת של סורביטול בתא ופוגעת בחדירות התא בשל הליפופיליות הנמוכה שלהם. לאחר מכן, סורביטול אינו חודר לממברנת התא, וגורם עוד יותר לנפיחות וקרע בתאים, מה שגורם לסדרה של התפתחות סוכרת וסיבוכים כרוניים [34-37]. GSSH יכול לדלדל את NADPH ולהצטמצם ל-GSH על ידי GSH-R. אם הסינתזה של GSH תקינה, או שמתרחשת ירידה דרמטית ב-GSH, צריכת NADPH חייבת לעלות [21]. לפיכך, מסלול הפוליול מתהפך כדי לרסן את ייצור הסורביטול, המספק יעד חדש למניעה והקלה של סוכרת (איור 3A).
על ידי תחרות על NADPH עם GSH-R וכתוצאה מכך כמות מופחתת של GSH, מסלול הפוליאול מגביר את הרגישות ללחץ חמצוני תוך תאי. וואנג וחב'. [29] הכינו ליפוזומים GSH נוגדי חמצון חדשים (GSH-LIP) שיושמו בטיפול בנפרופתיה סוכרתית. זה הצביע על כך ש-GSH-LIP דלקה ביעילות את NADPH כדי לחסום את מסלול הפוליול, והקלה באופן דרמטי על נפרופתיה סוכרתית, מה שסיפק בסיס תיאורטי חדש למחקר הננו-תרופות בטיפול בנפרופתיה סוכרתית
5. עיצוב ננו-תרופתי לגידול בהתבסס על המאפיינים הפיזיולוגיים של GSH
5.1. ננו-חלקיקים מיישמים מנגנוני מסירה של מיקוד גידולים
5.1.1. מיקוד פסיבי
מיקוד פסיבי תלוי בעיקר בגודל הננומטר שלו ובמבנה המיקרו-וסקולרי באתר הגידול. בהשוואה לרקמות רגילות, לרוב רקמות הגידול יש שיפוץ כלי דם לא שלם עקב צמיחה וחילוף חומרים נמרצים, עם פער של 10-1000 ננומטר בין האנדותל של כלי הדם. לכן, ננו-חלקיקים בגודל המתאים יכולים להגיע לרקמות הגידול דרך זרימת הדם ומועשרים ברקמות הגידול באמצעות אפקט החדירות והשמירה המוגברת (EPR) [38]. מאמינים בדרך כלל שלננו-חלקיקים של 10-100 ננומטר יש אפקט EPR טוב יותר [39]. מצד שני, מצב הגדילה והצפיפות של אנדותל כלי הדם באזורי הגידול יכולים להשפיע גם על אפקט ה-EPR [40].
5.1.2. מיקוד פעיל
על מנת לשפר עוד יותר את הספיגה של מערכת האספקה של ננו-תרופות על ידי תאי גידול, ניתן לשנות את פני השטח של הננו-חלקיקים עם ליגנים ממוקדים באופן פעיל, כך שהם יכולים להיכנס לתאים דרך אנדוציטוזיס בתיווך קולטן על ידי זיהוי קולטנים ספציפיים על פני השטח של תאי הגידול [41]. בהשוואה למיקוד פסיבי, לננו-חלקיקי מיקוד פעילים יש סגוליות חזקה יותר ויכולים להגביר באופן משמעותי את ריכוז התרופה התוך-תאית בתאי הגידול [42].
5.1.3. מערכת מתן ננו-תרופות רספונסיבית לגידול מיקרו-סביבה
בהשוואה לרקמות נורמליות, רקמות הגידול והתאים מציגים מאפיינים ייחודיים של המיקרו-סביבה, המשקפים בעיקר את ההיבטים הבאים [43]: (1) ערך pH: סביבת הגידול היא חומצית חלשה, pH 6.5-7.0. לתכלילים של תאי גידול או ליזוזומים יש pH נמוך יותר של 4.0–6.0 [44]; (2) תאי גידול מציגים סביבה רדוקטיבית שבה ריכוז הגלוטתיון יכול להגיע ל-1-10 mM, שהם פי 100-1000 מזה של סביבת הדם [45]; (3) המיטוכונדריה של תאי הגידול מציגות סביבה חמצונית, שבה הריכוז של מיני חמצן תגובתיים (ROS) יכול להגיע לרמת mM [46]. מערכת אספקת ננו-תרופות מגיבה ל-pH: השינוי בתכונות הגוף תחת גירוי pH גורם לננו-חלקיקים לבצע דה-פולימריזציה כדי להשיג את המטרה של אספקת תרופה ממוקדת בתאי גידול [47]. מערכת אספקת ננו-תרופות רדוקטיבית: בהתאם להפרש הריכוזים בין GSH בתאי גידול לרקמות תקינות, מתוכננים חומרים ננו-נשאים רגישים להפחתה. קשרי דיסולפיפיד או דיס-סלניום הכלולים בחומר הנשא יכולים להיות מופחתים על ידי GSH תוך תאי ולשבור, ובכך לגרום לשינויים דרסטיים בתכונות הנשא ולשחרר את התרופות המובלעות [48].

5.2. עיצוב ננו-תרופות מבוסס על דלדול NADPH במהלך הפחתת GSSG בפררופטוזיס
פרופטוזיס הוא מסלול מוות מתוכנת של תאים הכולל הומאוסטזיס של ברזל וחיזור. בדרך כלל מאמינים כי הייחודיות של פרופטוזיס היא הצטברות של ROS הנשענת על ברזל, וכתוצאה מכך להתרחשות של חמצון שומנים ומוות תאי [49]. יתר על כן, פרופטוזיס מראה גם את הירידה בוויסות של אנזים הליבה GPX4 במערכת נוגדת החמצון (מערכת הגלוטתיון). פרוקסיד השומנים ייסרקו על ידי GPX4. אם הפעילות של GPX4 מעוכבת, ייווצרו יותר פרוקסידים של שומנים וכתוצאה מכך חוסר איזון חמצוני והתרחשות פרופטוזיס [50]. לכן, עיכוב GPX4 או אפנון ביוסינתזה של GSH להפחתת פעילות GPX4 הן שתי גישות אופייניות להשראת פרופטוזיס. GSSG מופחת ל-GSH עם GSH-R וצורכת NADPH. NADPH הוא חומר מפחית תוך תאי חיוני לסילוק של הידרופרוקסידים ליפידים, וכאשר תהליכים אלו נפגעים, פרופטוזיס מופעלת [51]. בנוסף, מנגנון נוסף של פרופטוזיס הוא חומצה ארכידונית/חומצה אדרנית (AA/AdA), שבה הצטברות של PE-AA-OOH היא סמן נוסף של פרופטוזיס. ראוי לציין כי הצטברות של PE-AA-OOH בתאים תלויה בפעילות של GPX4, וניתן לחמצן PE-AA-OOH ל-PE-AA-OH בנוכחות GPX4 [52-54]. לכן, דלדול NADPH, PE-AA-OOH מוגזם ומחסור ב-GPX4 מוצעים בדרך כלל כמאפיינים העיקריים של פרופטוזיס מושרה [55-57], כפי שמוצג באיור 3B.

איור 3. פתוגנזה של GSH המעורבת ב: (א) המנגנון של מסלול הפוליאול [21]; (ב) המנגנון של פרופטוזיס [58].
וואנג וחב'. [58] עיצב את מקשר אזובנזן עם פוליפפטיד מצומד ניטרואימידאזול (DHM@RSL3), שהתפצל בסביבה אנאירובית. ננו-micelle DHM@RSL3 נכנסו לתאים והתפצלו כדי לשחרר RSL3, מעין מעכב GPX4. בינתיים, אזובנזן מדלדל את NADPH, קו-אנזים מרכזי בסינתזה של GSH ו-Trx(SH)2, וכתוצאה מכך ירידה בתכולת GSH ו-Trx(SH)2, והשראת פרופטוזיס כפולה כדי לקדם אפופטוזיס של תאי גידול. Zhao et al. [59] הכין מעורר קרינה RSL3 ברזל FL, שהיה מוקף במיצלות למיקוד GPX4. הם מצאו כי במודלים של תאי אדנוקרצינומה בשחלות עמידים לתרופות, מיצללי RSL3 נמצאו רעילים פי 30 מאשר מיצללי הבקרה הניתנים להפעלה. הדבר נובע בעיקר מירידה ב-GSH, אשר משפרת את יכולתו של RSL3 לעורר פרופטוזיס.
5.3. עיצוב ננו-תרופות מבוסס על יכולת הפחתת GSH במיקרו-סביבה של גידול
5.3.1. התיאוריה של חיזור רגיש במערכת אספקת ננו-תרופות
GSH נחשב למאגר החיזור העיקרי של מרקפטן-דיסולפיד כחומר מפחית בתאים [60,61]. הריכוז של GSH בדם הוא רק 0.1 אחוז עד 1 אחוז מזה שבתאים [62], מכאן שהדם הוא בדרך כלל הסביבה שבה GSH פחות מתווכות תגובות חיזור. עם זאת, תאי גידול מאופיינים כמטבוליזם לא תקין של הגידול ורמת GSH מוגברת כאשר נוצר לחץ חמצוני, וריכוז ה-GSH הציטוסוליים בתאי הגידול (2-20 mmol·L -1) גבוה פי 1000 מזה שבתאים רגילים, וכתוצאה מכך מציג סביבה מצמצמת חזקה [63,64]. הבדל קיצוני זה בריכוז הופך את GSH לטריגר חיזור במערכת אספקת התרופות. לכן, נוצרה מערכת אספקת ננו-תרופות ממוקדת רגישה לחזור, שתכונת העיצוב העיקרית שלה היא הכנסת קשרים כימיים מגיבים בעמוד השדרה של הנשא, בשרשרת הצדדית או בחומר המצולב. יתרה מכך, קשרים כימיים אלו יציבים יחסית בסביבה הרגילה של גוף האדם כולל דם ורקמות, אך קל לעבור אותם תגובות חיזור עם ריכוז גבוה של GSH, מה שמוביל לביקוע של קשרים כימיים לשחרור תרופות, ולהשגת מסירה מדויקת. של תרופות בתאי גידול [65,66].
5.3.2. קשרים כימיים המגיבים עם GSH
הקשרים הכימיים הרגישים לחיזור ממלאים תפקיד מכריע במערכת אספקת ננו-תרופות ממוקדת הרגישה לחמצון, המקבילה למתג של מערכת האספקה ומשפיעה ישירות על שחרור התרופה. ישנם כמה קשרים כימיים נפוצים הרגישים לחיזור, כגון קשר דיסולפיד (-SS-), קשר מונו-תיו-אתר (-S-), הקשר המצומד של -Pt-O-, קשר מצומד דיסלניד (-Se-Se-) , הקשר המצומד של -Se-N-, קשר מונו סלניום (-Se-). ביניהם, נעשה שימוש נרחב בקשר הדיסולפיד לפיתוח מערכת מתן תרופות המגיבה להפחתה לטיפול בסרטן. הסוגים והמאפיינים של קשרים כימיים נפוצים הרגישים לחיזור מוצגים בטבלה 1.

5.3.3. עיצוב ננו-תרופות המבוסס על קשרים כימיים שונים ננו-תרופה עם SS
קשר דיסולפיפיד (SS) הוא אחד מהקשרים הנפוצים ביותר ברגישות להפחתת GSH, והשיטה העיקרית להחדרת -SS- היא לעצב תרופות פרו עם קשרים רגישים לחזור. שאו וחב'. [67] שילב בהצלחה קמפטותיצין וכלורמבוציל על ידי קשרי דיסולפיד כדי לעצב פרו-תרופה חדשה מצומדת לתרופה. תחת ריכוז גבוה של GSH בתאי הגידול, הקשרים הדיסולפידים נהרסים ומשחררים ביעילות את שתי התרופות האנטי-סרטניות הללו. בהשוואה לתרופה אחת אנטי סרטנית, שתי תרופות אנטי סרטניות יכולות לא רק להרוג ביעילות תאי גידול, אלא גם להפחית באופן ניכר את תופעות הלוואי השליליות על תאים נורמליים (איור 4א). חורסנד ואחרים. [68] עיצב את המיצללים המתכלים המגיבים לתיול המורכבים מבלוק פולימר מתאקרילט (PHMssEt) תלוי מתאקרילט (PHMssEt) ובלוק פולי (אתילן אוקסיד) (PEO) הידרופילי. הקשר הדיסולפידי ב-PEO-b-PHMssEt מבוקע תחת פעולת GSH, מה שמוביל לחוסר יציבות של המיצלות בהרכבה עצמית. חוסר יציבות המיצל המופעל על ידי GSH שינתה את התפלגות הגודל שלהם ויצרה אגרגטים גדולים, ובכך הגבירה את השחרור של תרופות אנטי-סרטניות מובלעות וסיפקה יישומים רב-תכליתיים לאספקת תרופות (איור 4B). Sun et al. [69] הכינו ננו-חלקיקים PTX-SS CIT עם רגישות חיזור כפולה גבוהה יותר, שחרור מהיר יותר של תרופה ספציפית לגידול ופעילות אנטי-גידולית חזקה יותר (איור 4C). Luo et al. [70] עיצב את המצומדים החדשים המגיבים לחיזור על ידי גישור PTX ו-OA עם קשר דיסולפידי (PTX-SS-OA). ננו-חלקיקי PTX SS-OA הפגינו עליונות ברורה על פני טקסול ו- PTX-OA, והגידול נעלם כמעט לחלוטין בעכברים לאחר הטיפול על ידי ננו-חלקיקים (איור 4D). יתר על כן, ישנם תכנונים רבים של ננו-תרופות לטיפול אנטי-גידול המבוסס על קשרי דיסולפיפיד [71,72], המספקים פרספקטיבה מבטיחה לתכנון מערכת האספקה של ננו-תרופות.


איור 4. עיצוב סכמטי של תרופות אנטי-סרטניות שונות המגיבות ל-GSH עם קשר דיסולפיפיד. (א) קמפטוצין וכלורמבוציל מצומדים עם תרופות נוגדות סרטן על-מולקולריות בקשר דיסולפיפיד (SS). ננו-חלקיקים מתפצלים ל-CPT עם GSH [67]; (ב) מיצלות PEO-b PHMssEt מתכלות המגיבות ל-GSH. PEO-b-PHMssEt מחשוף ל-PEO-b-PHMSH עם GSH [68]; (ג) התרופות הפרו-תרופות PTX-SS-CIT מגשרות על קשרי דיסולפיפיד מתפצלות לתרכובות שונות עם GSH [60]; (ד) צימודים מגיבים לחזור על ידי גישור PTX ו-OA עם קשר דיסולפיפיד (PTX-SS-OA). PTX-SS-OA מחשוף ל-PTX עם GSH [70].''
תבקש עוד:
דוא"ל:wallence.suen@wecistanche.com whatsapp: פלוס 86 15292862950
