חתימות עצביות של קידוד זיכרון בסכיזופרניה מווסתות על ידי טיפול אנטי פסיכוטי
Mar 17, 2022
למידע נוסף:ali.ma@wecistanche.com
תַקצִיר
אין טיפול תרופתי לתיקון ליקוי קוגניטיבי בסכיזופרניה (SZ). זה הכרחי לאפיין פתולוגיות בסיסיות של עיבוד זיכרון כדי לפתח ביעילות טיפולים חדשים.
במחקר האורך הזה, שילבנו fMRI במהלך משימת קידוד זיכרון עם פרוטון MR ספקטרוסקופיה למדידת גלוטמט בהיפוקמפוס בתוספת גלוטמין (Glx). 17 SZ נסרקו ללא תרופות ולאחר 6 שבועות של טיפול בריספידון והשוואה לקבוצת ביקורת בריאים תואמים (HC) שנסרקו בהפרש של 6 שבועות.

לחץ ליתרונות Cistanche ותופעות לוואי לזיכרון
מטופלים ללא תרופות הראו תגובה מופחתת של רמת חמצן בדם (BOLD) במספר אזורים, כולל ההיפוקמפוס, ותגובת BOLD גדולה יותר באזורים של רשת מצב ברירת המחדל (DMN) במהלך קידוד זיכרון נכון. ניגודים פוסט-הוקים מהאינטראקציות המשמעותיות של קבוצה-לזמן הצביעו על ירידה בתגובת BOLD בהיפוקמפוס בקו הבסיס עם עלייה לאחר מכן בעקבות הטיפול. Hippocampal Glx לא היה שונה בין הקבוצות בתחילת המחקר, אך בשבוע 6, Hippocampal Glx היה נמוך משמעותית ב-SZ בהשוואה ל-HC. לבסוף, ב-SZ ללא תרופות, Glx בהיפוקמפוס גבוה יותר חזה פחות נטרול של תגובת BOLD באזורים של ה-DMN.

שימוש בשני אופני הדמיית מוח אפשרו לנו לחקור במקביל מנגנונים שונים המעורבים בתפקוד לקוי של קידוד זיכרון בסכיזופרניה. הפתולוגיה של ההיפוקמפוס במהלך קידוד הזיכרון נובעת מירידה בגיוס ההיפוקמפוס והשבתה שגויה של ה-DMN, וניתן לשנות את גיוס ההיפוקמפוס במהלך הקידוד על ידי טיפול אנטי פסיכוטי. High Glx בחולים ללא תרופות ניבא פחות נטרול של ה-DMN; תוצאות אלו מצביעות על מנגנון שבאמצעותו מושגת נטרול DMN שגוי, סימן היכר של ממצאים פתולוגיים ב-SZ.

דמט גרלר1, דייוויד מתיו ווייט1, נינה ונסה קרגולצ'אק1, לורנס ור הוף2,
קלינטון מרטין1, בלייק טננט1, אדריאן קרול להטי1,*
1 המחלקה לפסיכיאטריה ונוירוביולוגיה התנהגותית, אוניברסיטת אלבמה בבירמינגהם
2 המחלקה לנוירולוגיה, אוניברסיטת אלבמה בבירמינגהם
מילות מפתח:
הַצפָּנָה; שְׁלִיפָה; היפוקמפוס; רשת מצב ברירת מחדל (DMN); גלוטמט; טיפול אנטי פסיכוטי; MRI פונקציונלי; ספקטרוסקופיה תהודה מגנטית (MRS)
מבוא
כ-75-85 אחוז מחולי סכיזופרניה מראים ליקויים בקוגניציה עם ליקויים סלקטיביים בלמידה ובזיכרון (1). חשוב לציין, ליקויים בזיכרון האפיזודי אינם מוסברים באופן בלעדי על ידי ליקויים כלליים ב-IQ או בתפקוד מנהלי (2). לאחרונה, שילוב של טכניקות הדמיית מוח הפך לפרקטיקה נפוצה במחקר כדי לנצל מידע צולב ולשפר את זיהוי החתימות הפתולוגיות של מחלות (3). ניתן לחקור קורלטים עצביים של עיבוד זיכרון אפיזודי בחולים עם סכיזופרניה (SZ) באמצעות פרדיגמות התנהגותיות מתאימות יחד עם הדמיית תהודה מגנטית פונקציונלית (fMRI) (4, 5). ספקטרוסקופיה של תהודה מגנטית של פרוטונים (1H-MRS) מאפשרת מדידה in vivo של מטבוליטים במוח כגון גלוטמט, חומצת אמינו המעורבת בהולכה עצבית מעוררת (6) ומטבוליזם (7, 8). בהתחשב בתפקידו של גלוטמט בתור הנוירוטרנסמיטור המעורר העיקרי המעורב בקוגניציה (9) ותפקידו של ההיפוקמפוס בתהליכי למידה וזיכרון, מדידת גלוטמט בהיפוקמפוס יכולה לספק תובנה לגבי הפתולוגיה של ליקויי למידה וזיכרון ב-SZ. חשוב לציין, מספר קבוצות דיווחו כעת על רמות גבוהות של גלוטמט בתרופות תמימות או לא תרופתיות באזורי מוח שונים (10, 11), כולל בהיפוקמפוס (12).
עדויות מצטברות מצביעות על כך שחסרי זיכרון ב-SZ עשויים להיות קשורים לליקויים בקידוד מכוון (13, 14). מחקרים קודמים הראו קשר חיובי בין הצלחה בקידוד לבין תגובה תלוית רמת חמצן בדם בהיפוקמפוס (BOLD), והצביעו על תפקידו של ההיפוקמפוס בשילוב מידע מאזורי קליפת המוח השונים (15-17). הוכח שהפעלת היפוקמפוס והפרהיפוקמפוס גירוס במהלך הקידוד מנבאת הצלחה של אחזור לאחר מכן (18, 19). מספר מחקרי הדמיית עצבים דיווחו על הפרעות באות BOLD בהיפוקמפוס וב-parahippocampal gyrus הן ב-SZ (20) והן בקרב קרובי משפחה לא מושפעים (21-24). עם זאת, מחקרים אלה הניבו ממצאים לא תואמים, המדגימים תגובת BOLD מוגברת וירידה גם ב-SZ במהלך משימות זיכרון (25).

דיכוי אזורי רשת מצב ברירת מחדל (DMN) במהלך קידוד זיכרון ממלא תפקיד חשוב בהשגת ביצועי זיכרון מיטביים (26). ה-DMN מדוכא במהלך דרישות קוגניטיביות אך מעורב במהלך מנוחה (27). ב-SZ, היפראקטיבציה של DMN במהלך משימות קוגניטיביות דווחה בהרחבה (28, 29). בהתאם לתפקיד של גלוטמט בנוירואנרגטיקה (30), Hu et al. (31) דיווח על קשר חיובי בין ריכוז גלוטמט גבוה ב-DMN האחורי לבין נטרול מופחת של DMN במהלך משימת זיכרון עבודה. בנוסף, Kapogiannis et al. זיהה קשר בין גלוטמט DMN האחורי (קליפת המוח האחורית) לבין הקישוריות התפקודית הפנימית של ה-DMN (32). שני מחקרים זיהו כעת קשר בין גלוטמט קליפת המוח הקדמית (ACC) לבין תגובת ה-BOLD ב-DMN האחורי בבקרות בריאות וקשר זה נמצא הפוך ב-SZ (33, 34). יש צורך להבהיר את הנוירוכימיה של היפראקטיבציה של DMN ב-SZ.
הרוב המכריע של מחקרי ההדמיה של תפקוד הזיכרון כללו SZ תרופתי, עם זאת, הוכח שלתרופות אנטי פסיכוטיות יש השפעות מווסתות על תפקוד המוח בזמן מנוחה (35, 36), ובמהלך משימות קוגניטיביות (37). לכן, לא ברור באיזו מידה ממצאים אלו קשורים לטיפול אנטי פסיכוטי ולא למאפיינים מהותיים של המחלה. בנוסף, למרות שהתפקיד הקריטי של תרופות אנטי-פסיכוטיות להקלה בסימפטומים, כגון הזיות או אשליות, מבוסס היטב, היתרונות שלהן על תפקודים קוגניטיביים שנויים יותר במחלוקת (38). עם זאת, מחקרים שכללו מספר רב של נבדקים כמו CATIE (39) ו-EUFEST (40) הראו שטיפול במגוון רחב של תרופות אנטי-פסיכוטיות מהדור הראשון והשני קשור לשיפורים מתונים במבחנים קוגניטיביים. רלוונטי למטרות שלנו, מחקרים עדכניים דיווחו שתרופות אנטי פסיכוטיות מפחיתות את רמות הגלוטמט (41-43).
מטרת המחקר הנוכחי הייתה לבחון תגובת BOLD הקשורה לקידוד ורמות גלוטמט בהיפוקמפוס במצב מנוחה ב-SZ תוך שימוש בתכנון אורכי (לפני, בזמן ללא תרופות, ואחרי 6 שבועות של טיפול אנטי פסיכוטי) כדי להשוות בין בקרות בריאות לבין תגובת SZ ללא ההשפעה של תרופות כגורם מבלבל ולחקור את השפעת התרופה על תגובות המוח ב-SZ. שיערנו שב-SZ נשכפל ממצאים של תגובת BOLD מופחתת באזורים שנמצאו בעבר קשורים לעיבוד זיכרון, ותגובת BOLD מוגברת באזורים של ה-DMN, כמו גם שינויים כתוצאה מהטיפול. בהתבסס על ממצאים קודמים, שיערנו כי רמות הגלוטמט בהיפוקמפוס יעלו לפני ותפחתו לאחר הטיפול. בנוסף, חקרנו את הקשר בין גלוטמט ההיפוקמפוס לתגובת BOLD ב-DMN לפני ואחרי הטיפול.

חומרים ושיטות
משתתפים
נבדקים עם סכיזופרניה והפרעה סכיזואפקטיבית (SZ) גויסו מהמרפאות הפסיכיאטריות החוץ ומחדר המיון באוניברסיטת אלבמה בבירמינגהם כדי להשתתף במחקר על בסיס הפסקת תרופות אנטי פסיכוטיות למשך 10 ימים לפחות (הטיפול התרופתי לא הופסק כדי לענות על זה קרִיטֶרִיוֹן). ביניהם, 17 מטופלים סיימו הן מפגשי קידוד והן שליפה של פרדיגמת הזיכרון בשתי נקודות זמן (בסיס/לא תרופתי ושבוע 6). 17 נבדקי ביקורת בריאים (HC), ללא היסטוריה אישית או משפחתית אצל קרוב משפחה מדרגה ראשונה של הפרעות משמעותיות בציר DSM-IV-TR Axis I, גויסו באמצעות פרסומות בפליירים ובעיתון של האוניברסיטה. קריטריוני ההדרה היו מצבים רפואיים עיקריים, שימוש בסמים או תלות (למעט ניקוטין) בתוך שישה חודשים מההדמיה, פגיעת ראש קודמת, הפרעה נוירולוגית, אובדן הכרה במשך יותר משתי דקות והריון. מועצת הביקורת המוסדית של אוניברסיטת אלבמה בבירמינגהם סיפקה אישור למחקר וכל הנבדקים נתנו הסכמה מדעת בכתב לפני ההשתתפות. אבחנות נקבעו באמצעות הרשומות הרפואיות של הנבדקים וראיון האבחון למחקרים גנטיים (DIGS) (44). תפקוד קוגניטיבי כללי של כל נבדק אופיין על ידי הסוללה החוזרת להערכת מצב נוירופסיכולוגי (RBANS) (45).
המטופלים נסרקו ללא תרופות ולאחר מכן הוכנסו לניסוי של 6-שבוע עם ריספרידון (משטר מינון גמיש), שבסופו הם קיבלו סריקה שנייה. חומרת הסימפטומים הוערכה עם סולם הדירוג הפסיכיאטרי קצר (BPRS) (46) ותתי הסולמות החיוביים והשליליים שלו. הציות לתרופות נוטרה על ידי ספירת גלולות. HC נסרק פעמיים במרווחים של 6-שבוע. לפני כל פגישת סריקה, כל הנבדקים עברו בדיקת שתן לסמים.
עיצוב משימות וניתוח התנהגות
משימת הזיכרון האפיזודי (ראה ב-(4, 47) לפרטים) כללה שלב קידוד מכוון, ואחריו שלב זיכרון זיהוי לאחר עיכוב של 15-דקות. כדי למקסם את ביצועי השליפה, נעשה שימוש בפרדיגמת קידוד עמוקה תוך שימוש בהחלטת אנימציה. במהלך משימת הקידוד, המשתתפים ראו סדרה של 60 מילים, שהוצגו אחת בכל פעם למשך 300 אלפיות השנייה ולאחריה מסך קיבוע. 2-סימן פרסטימולוס שני ("חי?") הצביע על כך שהמשתתף היה צריך לענות בלחיצת כפתור אם המילה הקרובה חיה או לא חיה. לאחר מרווח של 15 דקות, המשתתפים ביצעו את משימת האחזור, שבה ראו 60 מילים, כולל 30 מילים שנראו בעבר (מילים ישנות) ו-30 מילים חדשות, שהוצגו אחת בכל פעם למשך 300 אלפיות שניות. 2-גירוי אזהרה שני ("מוכן?") הצביע על כך שהמשתתף היה צריך לענות בלחיצת כפתור אם המילה הקרובה היא "ישן" או "חדש". בהתאם לתגובות המשתתפים, פריטים אלו סווגו כהיטים, החמצות, דחיות נכונות והתראות שווא. מערכת IFIS-SA (In Vivo Corp., אורלנדו, פלורידה) המריץ תוכנת E- Prime (גרסה 1.2; Psychology Software Tools, Inc., פיטסבורג, פנסילבניה) שלטה באספקת גירוי ורשמה תגובות וזמני תגובה.
מילה נחשבה מקודדת כהלכה אם אוחזרה בהצלחה בסשן האחזור שלאחר מכן. מעורבות המשימה חושבה באמצעות לחיצות על כפתורים במהלך נסיונות קידוד. השתמשנו ב-d-prime (d'), המחושב על סמך המידע במהלך הפעלות אחזור, כמדד ביצועי הזיכרון העיקרי. d' הוא מדד לרגישות על ידי חישוב המרחק בין האות לרעש ביחידות סטיית תקן (d′=z(HITS) − z(FALSE ALARMS)) (48)
פרמטרי הדמיה
כל נתוני ההדמיה נרכשו בשני מפגשים בסורק 3T לראש בלבד (Siemens Allegra, Erlangen, גרמניה), מצויד בסליל ראש שידור/קליטה מקוטב מעגלי. נתוני fMRI נרכשו באמצעות רצף ההדמיה (EPI) (זמן חזרה/זמן הד [TR/TE]=2100/30msec, זווית היפוך=70 מעלות, שדה ראייה {{6} }} × 24 ס"מ2, 64 × 64 מטריצה, עובי פרוסה של 4 מ"מ, רווח של 1 מ"מ, 26 פרוסות ציריות). סריקה מבנית ברזולוציה גבוהה נרכשה באמצעות רצף T1-המגנטיזציה המשוקללת שהוכנה לרכישה מהירה שיפוע-הד (MPRAGE) (TR/TE/זמן היפוך [TI]= 2300/ 3.93/ 1100msec, זווית היפוך=12 מעלות , 256 × 256 מטריצה, ווקסלים איזוטריים בגודל 1 מ"מ). סדרה של סריקות אנטומיות אנטומיות Sagittal, Coronal ו-Axial T1- המשמשות כ-MRS-localizers נרכשו להצבת ווקסלים ספקטרוסקופיים. פרוסות היו מיושרות לקו האמצע האנטומי כדי לשלוט על הטיית הראש. כדי להקל על מיקום ה-voxel, התמונות הציריות התקבלו לאורך הציר הארוך של ההיפוקמפוס, כפי שניתן לראות מהתמונות הסגיטליות. הווקסל הונח בהיפוקמפוס השמאלי כך שכמות החומר האפור הייתה מקסימלית (גודל ווקסל 2.7 × 1.5 × 1 ס"מ). שיימינג ידני בוצע כדי לייעל את הומוגניות השדה על פני ה-voxel, ופולסים סלקטיביים להזזה כימית (CHESS) שימשו כדי לדכא את אות המים. ספקטרות נרכשו באמצעות רצף הספקטרוסקופיה שנפתר בנקודה (PRESS; TR/TE=2000/80ms כדי לייעל את אות הגלוטמט (49) ולמזער את תרומת המקרומולקולה; רוחב פס ספקטרלי של 1200 הרץ; 1024 נקודות; 640 ממוצעים).
ניתוח סטטיסטי
התנהגות ודמוגרפיה.-ניתוחים נערכו באמצעות SPSS 20 (IBM SPSS Inc., Chicago, IL). השוואות קבוצתיות בוצעו באמצעות צ'י ריבוע או ניתוח שונות, לפי העניין. ניתוחי תגובה בניסויי קידוד, זמן תגובה (RT) לניסויים נכונים, אחוז מילים מקודדות כהלכה וערכי d' נותחו באמצעות מודלים מעורבים ליניאריים המשווים השפעות קבועות של קבוצה (HC לעומת SZ), זמן (ללא תרופות לעומת שבוע 6 ), ואינטראקציות. ניתוחים פוסט הוק בוצעו במידת הצורך עם תיקון Bonferroni.
ניתוח MRS.-לאחר הסרת שיא המים השיורי, נתוני ה-MRS כומתו בתחום הזמן באמצעות אלגוריתם AMARES (50) ב-jMRUI (גרסה 3.0). ידע קודם שמקורו בספקטרום מטבוליטים in vitro ו-in vivo נכלל במודל (51), שהורכב מפסגות עבור N-אצטיל-אספרטאט (NAA), כולין (Cho), קריאטין (Cr), ושלושה פסגות עבור גלוטמט פלוס גלוטמין (Glx). משרעת, רוחב קו והיסט כימי הותאמו עבור כל שיא. גבולות Cramer-Rao תחתונים (CRLB) (52) חושבו עבור כל שיא. קריטריוני ההדרה היו CRLB של יותר מ-25 אחוזים. לא נכללו נתונים על סמך קריטריונים אלה. Glx כומתו לגבי Cr. נתוני MRS היו חסרים עבור 1 SZ, הן בקו הבסיס והן בשבוע 6, ועבור 2 HC בבסיס ו-3 HC בשבוע 6. ההבדלים בין הקבוצות נבדקו באמצעות בדיקת t מדגם עצמאית בקו הבסיס ובשבוע 6. רמת האלפא הייתה נקבע על .05.
ניתוח fMRI.-ניתוחי נתונים יושמו ב-SPM12 הפועל ב-MATLAB (גרסה R2013b). עיבוד מקדים של נתוני ה-fMRI כלל תיקון תזמון פרוסות, יישור מחדש וחתך מחדש לנפח הפונקציונלי הממוצע, תיקון חפצים/תנועה (תנועה > 1 מ"מ) באמצעות ArtRepair, רישום משותף לסריקה המבנית ונורמליזציה למרחב MNI באמצעות DARTEL (53) עם { {4}}mm FWHM החלקת גרעין גאוס. המשתתפים לא נכללו מניתוחים נוספים אם 33 אחוזים או יותר מהנתונים שלהם תוקנו במהלך תיקון חפצים ותנועה.
הניתוח הסטטיסטי ברמת הנושא כלל GLM הקשור לאירועים עם הרגרסורים הבאים: מקודד את האפקט העיקרי, מקודד נכון ומקודד ניסויים שגויים. מילה נחשבה מקודדת כהלכה אם אוחזרה בהצלחה בסשן האחזור שלאחר מכן. כל האירועים עוצבו באמצעות פונקציית תגובה המודינמית קנונית, והנתונים סוננו במעבר גבוה (ניתוק=256 שניות). ברמת הקבוצה, נוצרו מפות פרמטריות סטטיסטיות של האות BOLD במהלך הקידוד והשוואות בין קבוצות נערכו באמצעות מבחני t דו-מדגם. עבור תיקוני השוואה מרובים, סף גודל האשכול הוגדר בתוך SPM12, בהתבסס על תיאוריית השדות האקראיים של גאוס, כמספר הווקסלים הרציפים עם p< .05="" (uncorrected)="" to="" accept="" the="" false="" discovery="" rate="" (fdr)="" of="" 0.05="">
כדי לזהות הבדלים בין קבוצות ספציפיות ל-DMN, בנינו אזור עניין משולב (ROI), הכולל את הג'ירוס הקדמי המדיאלי, הצנצנת האחורית, הפרקונאוס, ההיפוקמפי והג'ירוס הפריאטלי התחתון, באמצעות אטלס AAL בתוך אטלס הפיק של אוניברסיטת ווייק פורסט גרסה 2.4 (55). המתאמים האנטומיים של מסכת ברירת המחדל של הרשת התבססו על באקנר ועמיתיו (56). תיקון נפח קטן (SVC) עמ'< .05="" was="" used="" to="" correct="" for="" multiple="">
כדי להעריך את ההשפעה של תרופות, ערכנו ניתוח פקטוריאלי מלא, זיהוי אזורי מוח הרגישים לאינטראקציה של קבוצה × זמן במהלך ניסויים נכונים לקודד. הערכות הנושא והפרמטרים של קידוד ניסויים נכונים הוכנסו לניתוח אפקט אקראי תוך שימוש ב"מודל הפקטוריאלי המלא" של SPM. הגורמים היו זמן (בסיס/לא תרופתי, שבוע 6) וקבוצה (HC, SZ). עבור ניתוח כל המוח הזה, סף גודל האשכולות להשוואות מרובות הוגדר על ידי סימולציות של מונטה קרלו באמצעות סף ברמת ווקסל ב-p= .05 עם 1000 סימולציות. למטרות המחשה, האות חולץ מאזורים משמעותיים באמצעות REX (CIBSR Stanford University, CA) עם החזר ROI של 6 מ"מ, והאות העצמי הראשון שחולץ שורץ לאחר מכן בכל נקודת זמן ולכל קבוצה. בנוסף, כדי לחקור את הקשר בין אזורים שבהם זוהו אינטראקציות משמעותיות של קבוצה × זמן וביצועי זיכרון, המשתן העצמי הראשון שחולץ זוים כנגד הערך הראשוני המשויך של כל משתתף.
כדי לחקור את הקשר בין DMN BOLD לבין Glx ההיפוקמפוס, המשתנה העצמי הראשון של הניגוד "הקוד הנכון" ב-DMN ROI חולץ באמצעות REX וביצענו מתאם דו-משתני בין הנתונים שחולצו ומדדי Glx בהיפוקמפוס באמצעות SPSS. הקשרים בין Glx ו-BOLD נותחו על ידי מתאם פירסון והושוו באמצעות טרנספורמציה r ל-Z של פישר.
תוצאות
התנהגות וגלוטמט היפוקמפוס
הקבוצות היו מותאמות היטב מבחינת גיל, מגדר, מצב סוציו-אקונומי של ההורים ועישון (טבלה 1).
גם HC וגם SZ הגיבו ברוב ניסויי הקידוד ללא הבדלים משמעותיים בין הקבוצות (F1,32= 2.778; p= .105), זמן (F1,32= 0.001; p{{ 8}} .98) או אינטראקציה קבוצתית לפי זמן (F1,32= 0.001; p= .98). זמני התגובה הממוצעים היו ארוכים יותר עבור SZ בהשוואה ל-HC (HC, 1100ms; SZ, 1459ms; F1,29=11.141; p= .002) אך השפעה משמעותית של זמן, או קבוצה-לפי- לא נצפתה אינטראקציה בזמן (HC baseline, 1103ms, שבוע 6, 1096ms; SZ baseline, 1530ms, שבוע 6, 1389ms; F1,29=2.294; p= .141) לא נצפתה. היה הבדל משמעותי בין הקבוצות באחוז המילים המקודדות כהלכה (HC, 85 אחוז; SZ, 67 אחוז; F1,32=11.141; p= .002) ללא הבדל משמעותי בזמן , או אינטראקציה קבוצתית לפי זמן (HC baseline, 86 אחוז , שבוע 6, 84 אחוז ; SZ baseline, 66 אחוז , שבוע 6, 67 אחוז ; F1,32= 0.306; p{{ 55}} .584). השוואה של ערכי d' על פני קבוצה וזמן גילתה השפעות עיקריות משמעותיות עבור הקבוצה (HC, 2.1; SZ, 1.44; F1,32=7.02; p= .012) אבל לא זמן, או אינטראקציה קבוצה לפי זמן (HC baseline, 2.14, שבוע 6, 2.07; SZ baseline, 1.43, שבוע 6, 1.44; F1,32=0.152; p= .699 ).
רמות ה-Glx בהיפוקמפוס לא היו שונות משמעותית בין הקבוצות בקו הבסיס, אך בשבוע 6, רמות ה-Glx של ההיפוקמפוס היו גבוהות משמעותית מ-SZ (בסיס, t= 0.425, nHC= 15, nSZ{{4} }, p= 0.675; week6, z= 2.46, nHC= 14, nSZ= 16, p= 0.02).
תוצאות fMRI
השוואות בסיס והשפעות של תרופות
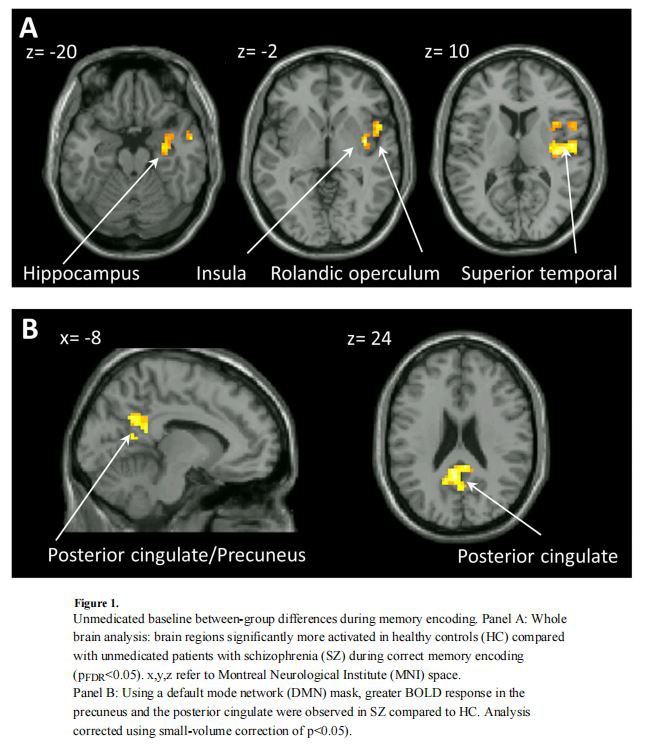
ניתוחי מוח שלם הוכיחו כי גם HC וגם SZ הציגו תגובה BOLD משמעותית באופן דו-צדדי בקליפת המוח הקדם-מצחית והפריאטלית האינסולה, הגב והגחון, קליפת המוח העליונה והאמצעית, התלמוס והפוטמן במהלך ניסויים נכונים. בהשוואה ל-HC, SZ לא תרופתי גילה תגובה מופחתת של BOLD באינסולה הימנית, בהיפוקמפוס, בקליפת המוח הקדמית והטמפורלית התחתונה (טבלה 2, איור 1, לוח עליון). שימוש במסכת DMN, תגובות מודגשות גדולות יותר (איור 1, לוח תחתון) בפרקונאוס (קואורדינטות MNI שיא ברמת voxel: x= 0, y= −63, z= 27, z=3.07) וה-cingulate האחורי (קואורדינטות MNI שיא ברמת voxel x= −3, y= −51 z= 24, z= 2. 89) נצפו ב-SZ בהשוואה ל-HC.
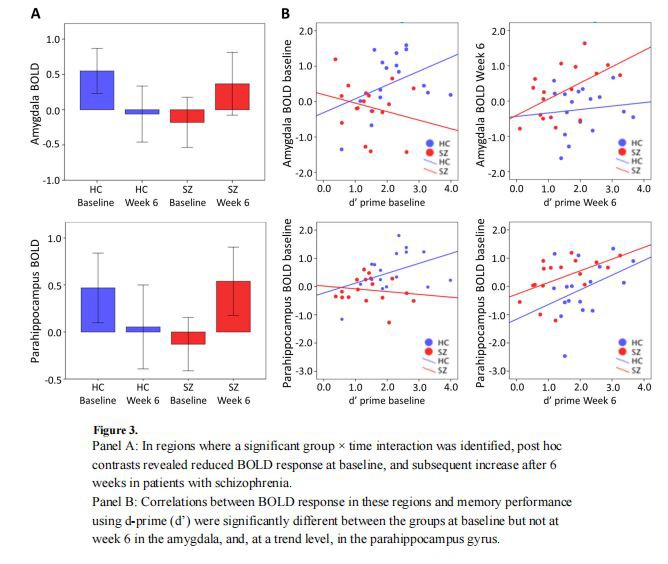
ניתוח פקטוריאלי מלא גילה אינטראקציה משמעותית של קבוצה × זמן בהמיספרה השמאלית בקליפת המוח העליונה והאמצעית, הגירוס והאינסולה של השל; בהמיספרה הימנית, ב-parahippocampal gyrus, בהיפוקמפוס, באמיגדלה ובקורטקס הטמפורלי האמצעי (טבלה 3, איור 2). באזורים אלה, ניגודים פוסט-הוק חשפו תגובת BOLD מופחתת בקו הבסיס, ועלייה לאחר מכן בשבוע 6 ב-SZ (איור 3 א').
כדי לבחון אם דפוסים אלו השפיעו על הביצועים, בחנו את הקשר בין אזורים שבהם זוהו אינטראקציות משמעותיות בקבוצה × זמן לבין ביצועי זיכרון. ב-HC, אך לא ב-SZ, יותר הפעלה באזורים אלו נקשרו לביצועים טובים יותר. ניתוח המתאם בין הפעלה באזורים אלה ל-d' היה שונה באופן מובהק בין HC ו-SZ בקו הבסיס אך לא בשבוע 6 באמיגדלה (בסיס, z= 1.75, nHC= 17, nSZ{{ 4}}, p= 0.04; week6, z= −1.36, nHC= 17, nSZ= 17, p= 0. 1), וברמת מגמה, ב-parahippocampal gyrus (בסיס, z= 1.54, nHC= 17, nSZ= 17, p=0.06; שבוע 6, z= −0.43, nHC= 17, nSZ= 17, p=0.33; איור 3B).
הקשר בין גלוטמט לאות BOLD
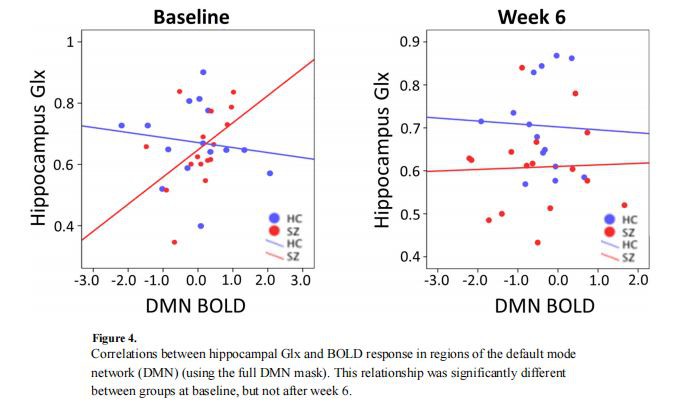
כדי לחקור את הקשר בין ההיפוקמפוס Glx לתגובת DMN BOLD, ערכנו ניתוח מתאם בין משתנים אלה. בקו הבסיס, ב-SZ אך לא ב-HC, היה מתאם מובהק בין ההיפוקמפוס Glx לתגובת BOLD שנמדדה באזור ה-DMN האחורי שבו SZ הראתה הפעלה מוגברת (r{0}} .49, n{ {2}}, p= 0.03). הקשר בין האות BOLD באזורי ה-DMN (באמצעות מסכת ה-DMN המלאה) לבין Glx ההיפוקמפוס היה שונה באופן משמעותי בין הקבוצות (z= −1.62, nHC= 15, nSZ= 16 , p= 0.05) בקו הבסיס (איור 4). לפיכך באזורים אלה, רמות גלוטמט גבוהות יותר היו קשורות להפעלה מוגברת של ה-DMN ב-SZ. בשבוע 6, המתאם בין רמות Glx בהיפוקמפוס לרשת מצב ברירת המחדל לא היה מובהק ולא היה שונה באופן מובהק מ-HC (z= −0.19, nHC= 14, nSZ= 16, p{ {19}}.42) (איור 4).
דִיוּן
למיטב ידיעתנו, זהו המחקר הראשון המשתמש בתכנון אורך יחד עם קבוצת ביקורת להערכת תגובת BOLD במהלך קידוד זיכרון והקשרים שלה עם גלוטמט בהיפוקמפוס בחולים עם סכיזופרניה לפני (ללא תרופתי) ואחרי קורס של 6-שבוע של טיפול עם ריספרידון. הממצאים שלנו הם 1) בחולים ללא תרופות, נוכחות של תגובת BOLD מופחתת במספר אזורים, כולל בהיפוקמפוס, ותגובת BOLD גדולה יותר באזורים של ה-DMN במהלך קידוד זיכרון נכון; 2) קבוצת תגובה BOLD משמעותית לפי אינטראקציה בזמן בקורטקס הטמפורלי, דו-צדדית, כולל בהיפוקמפוס הימני; אך לא באזורים של ה-DMN; 3) אפנון BOLD חריג של ההיפוקמפוס בקו הבסיס שנראה מנרמל בשבוע 6; בנוסף, הבדל קבוצתי מובהק בקשר בין ההיפוקמפוס BOLD לביצועים בקו הבסיס, אך לא בשבוע 6. 3) Hippocampal Glx לא היה שונה משמעותית בין הקבוצות בתחילת הדרך, אך בשבוע 6, Hippocampal Glx היה נמוך משמעותית ב-SZ בהשוואה ל-HC; 4) בקו הבסיס, Glx בהיפוקמפוס גבוה יותר חזה הפעלה גדולה יותר (או פחות נטרול) של תגובת ה-BOLD באזורים של ה-DMN ב-SZ, אך לא ב-HC; לא היה הבדל קבוצתי בקשר הזה בשבוע 6.
דפוסים לא תרופות והשפעה של תרופות על BOLD
תפקוד ההיפוקמפוס ב-SZ נחקר באמצעות טכניקות הדמיה שונות, כגון PET, SPECT, תיוג ספין עורקי ו-fMRI. חריגות בזרימת הדם המוחית האזורית (rCBF) (57-59), נפח (60-63) ואות BOLD (64, 65) דווחו באופן עקבי. בהתחשב בכך שרוב המחקרים כללו מטופלים תרופתיים, היה חשוב להעריך נבדקים ללא תרופות. הנה קבוצה של מטופלים ללא תרופות, אנו רואים תת-הפעלה של ההיפוקמפוס במהלך קידוד זיכרון נכון ומתאם בין BOLD ההיפוקמפוס לביצועים שהיה שונה באופן משמעותי מאשר בביקורות בריאים. תוצאות אלו עולות בקנה אחד עם רוב המחקרים המדווחים על ירידה בגיוס ההיפוקמפוס במהלך ביצועי זיכרון בסכיזופרניה (65-67), כולל בפסיכוזה של פרק ראשון (68). חוסר תפקוד זה זוהה גם אצל אחים בריאים (23, 24), מה שמצביע על כך שזו תכונה תורשתית ומועמדת טובה לפנוטיפ ביניים. התוצאות שלנו ב-HC עולות בקנה אחד עם מחקרים אחרים המראים שהפעלת היפוקמפוס ופרהיפוקמפוס במהלך הקידוד מנבאת הצלחה של אחזור לאחר מכן (18, 19). בקבוצה של חולים ללא תרופות שחופפו לקבוצה הנוכחית, דיווחנו על ניתוק תפקודי משמעותי בין ההיפוקמפוס ואזורים קליפת המוח אחרים בזמן מנוחה (69), כמו גם קישוריות אפקטיבית חריגה, שנמדדה בשיטות גריינג'ר סיבתיות, בין ההיפוקמפוס הדו-צדדי לפרה-פרונטלי. אזורים במהלך משימת אחזור זיכרון (4).
דווחו גם תגובות BOLD חריגות באזורים הפרונטליים ובאזורים זמניים אחרים ב-SZ בהשוואה ל-HC (64, 65). בקו הבסיס, נצפתה תגובה גדולה יותר של DMN BOLD ב-SZ בהשוואה ל-HC בקליפת המוח האחורית וה-precuneus. התוצאות שלנו עולות בקנה אחד עם ממצאים קודמים של הפעלת יתר של DMN ב-SZ על פני מגוון משימות קוגניטיביות (70-73).
זיהינו קבוצת תגובה משמעותית של BOLD לפי אינטראקציה בזמן באזור המקיף את ההיפוקמפוס, הפרהיפוקמפוס והאמיגדלה; באזורים אלה, ניגודים פוסט-הוק חושפים תגובה מופחתת של BOLD בקו הבסיס עם עלייה שלאחר מכן בשבוע 6, מה שמרמז על דפוס מנורמל עם הטיפול. בנוסף, מה שמצביע על השפעת תרופה באזור זה, הקשר בין תגובת ה-BOLD לביצועים כבר לא היה שונה באופן משמעותי מזה של קבוצת ביקורת בריאות, כפי שהיה בקו הבסיס. תוצאות אלו תואמות את אלו של מחקר PET קודם שבו הדגמנו אפנון משמעותי של rCBF בהיפוקמפוס על ידי טיפול אנטי פסיכוטי במהלך מצב מנוחה וביצוע משימה (58). בנוסף, לאחר שבוע אחד של טיפול אנטי פסיכוטי, דיווחנו על נורמליזציה של הקישוריות האפקטיבית החריגה בין ההיפוקמפי והאזורים הפרה-פרונטליים שנראתה כאשר החולים לא קיבלו טיפול תרופתי (4).
למרות שצפינו באפנון של תגובת BOLD בהיפוקמפוס, לא ראינו שיפורים משמעותיים בציוני הזיכרון לאורך זמן בחולים. אחרים דיווחו על שיפור הן בתגובת BOLD והן בקוגניציה עם תרופות אנטי פסיכוטיות. במהלך משימת בקרה קוגניטיבית, מטופלים תרופתיים הפגינו הפעלה גבוהה יותר של קליפת המוח הקדם-מצחית וכן ביצועים התנהגותיים טובים יותר בהשוואה למטופלים שאינם מטופלים (74). למרות שבמחקר שלנו, הזמן לפי אינטראקציה קבוצתית לא הצביע על השפעה של טיפול תרופתי באזורים של ה-DMN, במחקר אורך, 8 שבועות של טיפול אנטי פסיכוטי נמצאו כמשפרים ביצועים התנהגותיים ומווסתים את הקישוריות התפקודית של ה-DMN ב-SZ במהלך א. משימת זיכרון עבודה (75). חשוב יהיה לקבוע אם השינויים שנצפו במחקר זה קשורים לשיפור בתהליכי זיכרון, מכיוון שהם יכולים לספק סמנים ביולוגיים שעלולים להוביל לזיהוי של גורמים חדשים לטיפול בהפרעות זיכרון בסכיזופרניה.
כיצד תרופות אנטי פסיכוטיות יכולות לשפר את תפקוד ההיפוקמפוס? תרופות אנטי פסיכוטיות לא טיפוסיות נמצאו כמגבירות רמות של חלבונים סינפטיים ומעודדות צמיחה דנדרטית (76). אחד מהחלבונים הללו, גורם נוירוטרופי שמקורו במוח (BDNF) אשר מאוחסן ומשוחרר על ידי נוירונים גלוטמטריים, הוא מווסת חשוב של העברה סינפטית. BDNF חיוני גם לפלסטיות הסינפטית ומסייע בהגנה מפני אפופטוזיס (77, 78). עדויות נוספות מראות ש-BDNF קשור לעלייה ברמות צפיפות עמוד השדרה (79). מטה-אנליזה גדולה שכללה למעלה מ-7000 נבדקים מאת Fernandes et al. מראה כי SZ קשור לרמות נמוכות יותר של BDNF וכי רמות אלו עלו עם טיפול אנטי פסיכוטי (80). קיימת עדיפות לכך שתרופות אנטי פסיכוטיות לא טיפוסיות במיוחד עוזרות להפוך, או לפחות להקל, אפופטוזיס דנדריטי של השכבות החיצוניות של הקורטקס (81).
גלוטמט
בתחילת המחקר, לא היה הבדל קבוצתי משמעותי ברמות Glx. בעבר הדגמנו רמות גבוהות של Glx בהיפוקמפוס בקבוצה של 27 מטופלים ללא תרופות בהשוואה לקבוצה מתאימה של ביקורת בריאות (12). לכן יתכן שהמחקר שלנו לא הועיל להראות הבדל קבוצתי. לאחר 6 שבועות של טיפול, ראינו ירידה משמעותית ב-Glx ההיפוקמפוס במטופלים תרופתיים בהשוואה ל-HC, אך לא בהשוואה לקו הבסיס הלא-תרופתי שלהם. קיים מספר מצומצם של מחקרים אורכיים המעריכים את ההשפעה של טיפול אנטי פסיכוטי קצר טווח על מטבוליטים גלוטמטרגיים. בחולים כרוניים שנשטפו מתרופות, Szulc דיווח על ירידה באונה הטמפורלית Glx לאחר ארבעה שבועות של טיפול במגוון תרופות אנטי פסיכוטיות (43). בחולי פסיכוזה בפרק ראשון שלא טופלו בטיפול תרופתי, דיווח Egerton על הפחתה ב-cingulate cortex glutamate לאחר ארבעה שבועות של טיפול באמיסולפרייד (41). בנבדקי פסיכוזה סטראטליים שלא עברו טיפול תרופתי בהשוואה לאנשי ביקורת בריאים, דה לה פואנטה-סנדובל ראה גלוטמט סטריאטלי גבוה יותר בקו הבסיס והפחתה משמעותית בגלוטמט סטריאטלי לאחר ארבעה שבועות של טיפול בריספידון (42). לכן ישנן אינדיקציות חזקות לכך שרמות הגלוטמט מווסתות על ידי תרופות אנטי פסיכוטיות. אנו מכירים בכך שגודל המדגם שלנו היה מוגבל ויש צורך להתייחס לשאלות אלו עם גודל מדגם גדול יותר.
אות גלוטמט/BOLD
בקו הבסיס, Glx גבוה יותר חזה פחות נטרול של תגובת BOLD באזורים של ה-DMN ב-SZ, אך לא ב-HC; קשר זה לא היה קיים בשבוע 6. בביקורות בריאות, Hu et al. דיווח על קשר חיובי בין ריכוז גלוטמט גבוה ב-DMN האחורי והפחתת DMN במהלך משימת זיכרון עבודה (31). גם בבקרות בריאות, Kapogiannis מצא קשר בין גלוטמט DMN אחורי (קליפת המוח האחורית) לבין הקישוריות התפקודית הפנימית של ה-DMN (32). כאן מצאנו מתאם בין ההיפוקמפוס Glx לתגובת BOLD באזור ה-DMN, אזור מחוץ לזה שממנו נמדד Glx. בעוד שריכוזים נוירוכימיים מקומיים חייבים להשפיע על הפעילות העצבית המקומית, ניתן גם לטעון שהם עשויים לתרום לפעילות של אזורי הקרנה מרוחקים; זה כנראה כרוך בשידור סינפטי מורכב. כעת היו מספר מחקרים המדגימים מתאמים בין גלוטמט לאות BOLD באזורים מרוחקים מהמקום שבו נמדד גלוטמט (33, 47, 82-84).
מכיוון שרמות גבוהות יותר של גלוטמט נמצאו בעקביות בתרופות תמימות או לא תרופתיות SZ (10-12), ניתן לשער שרמות גבוהות יותר של Glx בחולים ללא תרופות מייצגות מצב פתולוגי המשנה את היחס המקומי של עירור על פני עיכוב וכוונון של תחזיות עצביות עם השפעה משמעותית על האות BOLD באזורי הקרנה. באופן מסקרן, בדומה למחקרים קודמים (82, 85), הקשר החריג בין תגובת BOLD לבין Glx ב-SZ נצפה ב-DMN האחורי. ה-DMN האחורי נקשר באופן עקבי להיזכרות מוצלחת (Vincent et al., 2006); בנוסף, זהו אזור רכזת מרכזי המקושר באופן צפוף עם אזורי מרכז אחרים, ויוצרים יחד מועדון עשיר (86). בשבוע 6, לנוכח רמות Glx נמוכות יותר ב-SZ, הקשר הזה לא היה משמעותי יותר.
מסקנות
הקוגניציה נפגעת בסכיזופרניה, ועד היום אין טיפול תרופתי לשיקום. זה הכרחי לאפיין פתולוגיות בסיסיות ספציפיות של עיבוד זיכרון במחלה כדי לפתח ביעילות טיפול חדש. שימוש בשני אופני הדמיית מוח אפשרו לנו לחקור במקביל מנגנונים משוערים שונים המעורבים בתפקוד לקוי של קידוד זיכרון בסכיזופרניה. אישרנו שהפתולוגיה של ההיפוקמפוס במהלך קידוד הזיכרון נובעת מירידה בגיוס ההיפוקמפוס והשבתה שגויה של ה-DMN וכי גיוס ההיפוקמפוס במהלך קידוד הזיכרון מווסת על ידי טיפול אנטי פסיכוטי עם נורמליזציה של הקשר בין BOLD לביצוע המשימות. לבסוף, הראינו ש-Glx גבוה בחולים ללא תרופות מנבא פחות נטרול של ה-DMN; תוצאות אלו שיש לשכפל עם קבוצות גדולות יותר מציעות מנגנון שבאמצעותו מושגת נטרול DMN שגוי, סימן היכר של ממצאים פתולוגיים ב-SZ.
התייחסות
1. Saykin AJ, Gur RC, Gur RE, Mozley PD, Mozley LH, Resnick SM, et al. תפקוד נוירופסיכולוגי בסכיזופרניה. פגיעה סלקטיבית בזיכרון ובלמידה. Arch Gen פסיכיאטריה. 1991;48(7):618–24. [PubMed: 2069492]
2. Kopald BE, Mirra KM, Egan MF, Weinberger DR, Goldberg TE. גודל ההשפעה של תפקוד מנהלים ו-IQ על זיכרון אפיזודי בסכיזופרניה. ביול פסיכיאטריה. 2012;71(6):545–51. [PubMed: 22265665]
3. Sui J, Yu Q, He H, Pearlson GD, Calhoun VD. סקירה סלקטיבית של שיטות היתוך מולטי-מודאליות בסכיזופרניה. חזית המהום Neurosci. 2012;6:27. [PubMed: 22375114]
4. Hutcheson NL, Sreenivasan KR, Deshpande G, Reid MA, Hadley J, White DM, et al. קישוריות יעילה במהלך אחזור זיכרון אפיזודי בקרב משתתפי סכיזופרניה לפני ואחרי תרופות אנטי פסיכוטיות. Hum Brain Map. 2015;36(4):1442–57. [PubMed: 25504918]
5. Ragland JD, Gur RC, Valdez J, Turetsky BI, Elliot M, Kohler C, et al. fMRI הקשור לאירועים של פעילות פרונטומפורלית במהלך קידוד וזיהוי מילים בסכיזופרניה. Am J Psychiatry. 2004;161(6):1004–15. [PubMed: 15169688]
6. פטרוף או"א. גאבא וגלוטמט במוח האנושי. מדען מוח. 2002;8(6):562–73. [PubMed: 12467378]
7. Magistretti PJ, Pellerin L. מנגנונים סלולריים של מטבוליזם אנרגטי במוח. רלוונטיות להדמיית מוח תפקודית והפרעות ניווניות. Ann NY Acad Sci. 1996;777:380–7. [PubMed: 8624117]
8. Moffett JR, Ross B, Arun P, Madhavarao CN, Namboodiri AM. N-Acetylaspartate ב-CNS: מנוירודיאגנוסטיקה לנוירוביולוגיה. פרוג נוירוביול. 2007;81(2):89–131. [PubMed: 17275978]
9. רובינס TW, מרפי ER. פרמקולוגיה התנהגותית: 40 שנים פלוס של התקדמות, עם התמקדות בקולטני גלוטמט וקוגניציה. Trends Pharmacol Sci. 2006;27(3):141–8. [PubMed: 16490260]
10. de la Fuente-Sandoval C, Leon-Ortiz P, Favila R, Stephano S, Mamo D, Ramirez-Bermudez J, et al. רמות גבוהות יותר של גלוטמט בסטריאטום האסוציאטיבי של נבדקים עם תסמינים פרודרומליים של סכיזופרניה וחולים עם פסיכוזה בפרק ראשון. נוירופסיכופרמקולוגיה. 2011;36(9):1781–91. [PubMed: 21508933]
11. Kegeles LS, Mao X, Stanford AD, Girgis R, Ojeil N, Xu X, et al. רמות גבוהות של קליפת המוח הקדם-מצחית של חומצה גמא-אמינו-בוטיר וגלוטמט-גלוטמין בסכיזופרניה שנמדדה in vivo עם ספקטרוסקופיה של תהודה מגנטית של פרוטון. Arch Gen פסיכיאטריה. 2012;69(5):449–59. [PubMed: 22213769]
12. Kraguljac NV, White DM, Reid MA, Lahti AC. הגברת גלוטמט בהיפוקמפוס וחסרים נפחיים בחולים ללא תרופות עם סכיזופרניה. JAMA פסיכיאטריה. 2013;70(12):1294–302. [PubMed: 24108440]
13. Cairo TA, Woodward TS, Ngan ET. ירידה ביעילות הקידוד בסכיזופרניה. ביול פסיכיאטריה. 2006;59(8):740–6. [PubMed: 16229823]
14. Cirillo MA, Seidman LJ. חוסר תפקוד זיכרון הצהרתי מילולי בסכיזופרניה: מהערכה קלינית לגנטיקה ומנגנוני מוח. Neuropsychol Rev. 2003;13(2):43–77. [PubMed: 12887039]
15. Preston AR, Eichenbaum H. משחק הגומלין של ההיפוקמפוס והקורטקס הפרה-פרונטלי בזיכרון. קור ביול. 2013;23(17): R764–73. [PubMed: 24028960]
16. Preston AR, Shohamy D, Tamminga CA, Wagner AD. תפקוד היפוקמפוס, זיכרון הצהרתי וסכיזופרניה: שיקולי הדמיה אנטומיים ותפקודיים. Curr Neurol Neurosci Rep. 2005;5(4):249–56. [PubMed: 15987607]
17. שוהמי ד, וגנר לספירה. שילוב זיכרונות במוח האנושי: קידוד ההיפוקמפוס-המוח התיכון של אירועים חופפים. עֲצָבוֹן. 2008;60(2):378–89. [PubMed: 18957228]
18. Brewer JB, Zhao Z, Desmond JE, Glover GH, Gabrieli JD. יצירת זיכרונות: פעילות מוחית החוזה עד כמה תיזכר החוויה החזותית. מַדָע. 1998;281(5380):1185–7. [PubMed: 9712581]
19. Jackson O 3rd, Schacter DL. פעילות הקידוד באונה הטמפורלית המדיאלית הקדמית תומכת בזיהוי אסוציאטיבי לאחר מכן. תמונה עצבית. 2004;21(1):456–62. [PubMed: 14741683]
20. Jessen F, Scheef L, Germeshausen L, Two Y, Kockler M, Kuhn KU, et al. הפחתת הפעלת ההיפוקמפוס במהלך קידוד וזיהוי מילים בחולי סכיזופרניה. Am J Psychiatry. 2003;160(7):1305–12. [PubMed: 12832246]
21. Achim AM, Bertrand MC, Sutton H, Montoya A, Czechowska Y, Malla AK, et al. אפנון חריג סלקטיבי של פעילות ההיפוקמפוס במהלך היווצרות זיכרון בפסיכוזה של פרק ראשון. Arch Gen פסיכיאטריה. 2007;64(9):999–1014. [PubMed: 17768265]
22. Goldberg TE, Torrey EF, Gold JM, Bigelow LB, Ragland RD, Taylor E, et al. סיכון גנטי להפרעה נוירופסיכולוגית בסכיזופרניה: מחקר על תאומים מונוזיגוטיים בחוסר התאמה והתאמה להפרעה. Schizoph Res.1995;17(1):77-84 [PubMed:8541253]
23. Pirnia T, Woods RP, Hamilton LS, Lyden H, Joshi SH, Asarnow RF, et al. תפקוד לקוי של ההיפוקמפוס במהלך קידוד זיכרון הצהרתי בסכיזופרניה והשפעות של אחריות גנטית. Schizophr Res.2015;161(2-3):357-66.[PubMed:25497222]
24. Rasetti R, Mattay VS, White MG, Sambataro F, Podell JE, Zoltick B, et al. Changed function parahippocampal hippocampal במהלך קידוד גירוי: אינדיקטור פוטנציאלי של אחריות גנטית לסכיזופרניה. JAMA Psychiatry.2014;71(3):236-47.[PubMed:24382711]
25. Kraguljac NV, Srivastava A, Lahti AC. חסרי זיכרון בסכיזופרניה: סקירה סלקטיבית של מחקרי תהודה מגנטית תפקודית (FMRI). Behay Sci(Basel).2013:3(3):330-47. [PubMed:25379242]
26.Anticevic A,Repovs G,Shulman GL,Barch DM.When less is more: TPJ וכיבוי רשת ברירת מחדל במהלך הקידוד מנבאים ביצועי זיכרון עבודה. תמונה עצבית. 2010;49(3):2638-48. [PubMed:19913622]
27. רייכל ME. רשת מצב ברירת המחדל של המוח.Annu Rev Neurosci.2015;38:433-47. [PubMed:25938726]
28. Anticevic A, Repovs G,Barch DM. קידוד זיכרון עבודה ותחזוקה בסכיזופרניה: עדות עצבית להפרעות בהפעלה ובנטרול. Schizophr Bull 2013;39(1):168-78. [PubMed:21914644]
29. Whitfield-Gabrieli S.Thermenos HW. Milanovic S.Tsuang MT. Faraone SV. McCarley RW, et al. היפראקטיביות וקישוריות של רשת ברירת המחדל בסכיזופרניה וקרובי משפחה מדרגה ראשונה של אנשים עם סכיזופרניה. Proc Natl Acad Sci US A.2009;106(4):1279-84. [PubMed:19164577]
30. שולמן RG, Rothman DL, Behar KL, Hyder F. בסיס אנרגטי של פעילות המוח: השלכות על הדמיה עצבית. Trends Neurosci.2004;27(8):489-95. [PubMed:15271497]
31. Hu Y, Chen X, Gu H, Yang Y. ריכוזי גלוטמט ו-GABA במצב מנוחה מנבאים נטרול הנגרמת על ידי משימה ברשת מצב ברירת המחדל. J Neurosci.2013;33(47):18566-73. [PubMed:24259578]
32. Kapogiannis D, Reiter DA, Wiltte AA, Mattson MP. גלוטמט ו-GABA בקליפת המוח הפוסטרומדיה מנבאים קישוריות פונקציונלית מהותית של רשת מצב ברירת המחדל. Neuroimage.2013:64:112-9. [PubMed:23000786]
33.Falkenberg LE,Westerhausen R,Craven AR,Johnsen E,Kroken RA.EM LB, et al.השפעה של רמות גלוטמט על תגובה נוירונית ויכולות קוגניטיביות בסכיזופרניה. Neuroimage Clin. 2014;4:576-84. [PubMed:24749064]
34. Overbeek G הקשר בין גלוטמט לאפקט BOLD Stroop בסכיזופרניה של הפרק הראשון. כתב היד הוגש 2018.
35. Lahti AC, Weiler MA. Holcomb HH, Tamminga CA, Cropsey KL. Modulation of limbic circuitry מנבא תגובת טיפול לתרופות אנטי פסיכוטיות; מחקר הדמיה תפקודית בסכיזופרניה. Neuropsychopharmacology.2009;34(13):2675-90. [PubMed:19675535]
36. Kraguljac NV, White DM, Hadley JA, Visscher K, Knight D, ver Hoef L, et al. אבנורמליות ברשתות תפקודיות בקנה מידה גדול בחולים לא מטופלים עם סכיזופרניה והשפעות של ריספרידון. Neuroimage Clin.2016;10:146-58. [PubMed:26793436]
37. Honey GD, Bullmore ET, Soni W, Varatheesan M, Williams SC, Sharma T.Differences in activation cortical frontal by task memory work after replacement of risperidone for תרופות אנטי פסיכוטיות טיפוסיות בחולים עם סכיזופרניה. Proc Natl Acad Sci US A. 1999;96(23):13432-7. [PubMed:10557338]
38. מינצנברג מ.ג. קרטר CS. פיתוח טיפולים לפגיעה בקוגניציה בסכיזופרניה. Trends Cogn Sci.2012;16(1):35-42.[PubMed:22178120]
39, Keefe RS.Bilder RM, Davis SM, Harvey PD, Palmer BW, Gold M, et al. השפעות נוירוקוגניטיביות של תרופות אנטי פסיכוטיות בחולים עם סכיזופרניה כרונית ב-CATIE Trial.Arch Gen Psychiatry.2007;64(6):{ {4}}. [PubMed: 17548746]
40. Davidson M, Galderisi S, Weiser M, Werbeloff N, Fleischhacker WW, Keefe RS, et al. השפעות קוגניטיביות של תרופות אנטי פסיכוטיות בסכיזופרניה בפרק ראשון והפרעה סכיזופרניפורמית:
