אינטראקציות בין מזון ותרופות, ומצב תזונתי בחולי כליות: סקירה נרטיבית Ⅱ
Jul 26, 2024
2.3. שינויים בהוצאה לאנרגיה במנוחה
הוצאת אנרגיה במנוחה (REE)מייצג כ-55-70% מהדרישה לאנרגיה אצל נבדקים בריאים ופעילים פיזית. REE תלוי בגיל, מגדר, הרכב גוף, פעילות גופנית, מצב בריאותי והרגלי תזונה, כמו גם באחוז המסה הרזה והאיברים הקרביים. תרופות הפעילות על מנגנוני הבקרה המרכזיים (פרו-אופיומלנוקורטין (POMC) נוירונים ונוירופפטידים אורקסיגניים Yו-AGRP), או פריפריאליים (כלומר, אינסולין, קורטיזול, הורמוני בלוטת התריס) יכולים להשפיע על משקל הגוף על ידי מווסת חילוף החומרים של פחמימות, שומנים וחלבונים. סטרואידיתרופות אנטי דלקתיות, תכשירי אסטרוגן-פרוגסטין ותרופות נגד סוכרת(הן דרך הפה והן בהזרקה) משפיעים על חילוף החומרים של גלוקוז ו/או שומן [28]. לגלוקוקורטיקואידים, בפרט, יש השפעות מרובות. הם יכולים לעורר תנגודת לאינסולין, כמו גם שינויים בחלוקת מסת השומן, ושימור מים ומלח באמצעות פעילות קורטיקואידית מינרלית שיורית.
אסטרוגנים עלולים גם לפגוע ברגישות לאינסולין. מעניין, אסטרוגניםלקדם סינתזה של הכבד, במחזור HDL וטריגליצרידים עם ספיגה מוגברת ומטבוליזציה היקפית של LDL, ובכך מוביל ליחס HDL/LDL מוגבר. פרוגסטין מראים השפעות הפוכות, במיוחד אם יש להם פעילות אנדרוגנית שיורית שיכולה להיות מסומנת כחלשה (דסוגסטרל וגסטודן) או אנטגוניסטי גרידא (דרוספירנון וכלורטלידון) [28].

פורמולציה חדשה של צמחי מרפא למחלת כליות
לתרופות נוגדות סוכרת דרך הפה יש מנגנוני פעולה שונים, ולכן הן עשויות לגרום לירידה במשקל הגוף (כלומר, ביגואנידים, אגוניסטים ל-GLP-1), עלייה במשקל הגוף (כלומר, גליטזונים, סולפונילאוריאה) או לא להשפיע עליו (כלומר. , גלינידים, גליטזונים, מעכבי DPP4). בנוסף, חלקם קשורים לסיכון להיפוגליקמיה (סולפונילאוריאה וגלינידים) וכן לדיסגאוזיה (ביגואנידים) [29]. לבסוף, מעכבי acarbose (מעכב אלפא גלוקוזידאז במעיים) ומעכבי SGLT2 (סוג 2 נתרן-גלוקוז טרנספורטר) עשויים להיות קשורים לירידה במשקל. תרופות אנטי-פסיכוטיות מהדור הראשון (כלומר, haloperidol) והשני (כלומר, olanzapine, clozapine ו-risperidone) משפיעות על השליטה הגליקמית, הן פועלות ישירות על תאי הלבלב והן על הרקמות ההיקפיות ומעוררות תנגודת לאינסולין. בנוסף, השפעת ההרגעה מובילה להפחתה בהוצאת האנרגיה ובעלייה במשקל, בולטת במיוחד אצל מתבגרים. מעכבי פרוטאז אנטי-רטרו-ויראליים ומעכבי נוקלאוזידים שלתמלול הפוך(NRTI) עשוי להעדיף עלייה במשקל על ידי השפעה על תאי הלבלב [30].
שינוי בחילוף החומרים של הגלוקוז נמצא גם במהלך תיאזידים וחוסמי בטא. הראשון עלול לגרום להיפרגליקמיה על ידי הפחתת הפרשת אינסולין משנית להיפוקלמיה, בעוד שהאחרון עלול לגרום להיפרגליקמיה ולהפחית את הרגישות לאינסולין היקפית ועלייה במשקל. טבלה 2 מציגה את ההשפעה של כמה תרופות או מחלקות של תרופות על משקל הגוף.
2.4. חוסר תזונתי כתוצאה מתרופות
מחסור במיקרו-נוטריינטים (כלומר, ויטמינים ומינרלים) הוא מצב נוסף של תת תזונה, שעלול להיגרם על ידי תרופות מסוימות המפריעות לספיגה או להפרשה. השינויים הנפוצים ביותר הם אלו הנוגעים לאשלגן, נתרן, מגנזיום, ברזל, סידן, אבץ ונחושת. אכן, תרופות מסוימות יכולות להגביר את הפרשת האשלגן, ואת שימור הנתרן, או להפחית את הספיגה או השחרור של יוד, להפחית את ספיגת הברזל והאבץ ולהגביר את רמות הנחושת.
היפוקלמיה קשורה לעתים קרובות למשתנים (משתני לולאה ותיאזידים), ממריצים אדרנרגיים, או חומרים משלשלים [31], כמו גם כמה נוגדנים חד שבטיים המשמשים באונקולוגיה [32]. היפרקלמיה יכולה להופיע גם במהלך טיפול עם מעכבי מערכת רנין-אנגיוטנסין-אלדוסטרון (RAASi), כלומר אליסקירן, מעכבי ACE, חוסמי קולטן אנגיוטנסין II (ARB), אנטגוניסטים לקולטן אלדוסטרון, חוסמי - נוגדי דלקת לא סטרואידים (NSAIDS), הפרינים, מדכאים חיסוניים (כלומר, טקרולימוס, ציקלוספורין), קורטיקואידים מינרלים וגלוקוקורטיקואידים, דיגוקסין [33-36].
היפונתרמיה היא הפרעה אלקטרוליטית נפוצה בקרב אנשים הנוטלים תרופות הפועלות על הומאוסטזיס של נתרן ומים, או מגבירות את הייצור/משפרות את ההשפעה של ההורמון האנטי-דיורטי (ADH), המעודדות ספיגה חוזרת של מים ברמת הצינורית האוספת הכלייתית. תרופות רבות עשויות לייצר ירידה ברמות הנתרן בסרום [37], כולל משתני תיאזידים, SSRIs, תרופות אנטי פסיכוטיות כגון phenothiazine והלופרידול (שעשויים לגרום להפרשה לא תקינה של ADH), תרופות אנטי אפילפטיות (כלומר, קרבמזפין, חומצה ולפרואית), NSAIDS, מעכבי משאבות פרוטונים (PPI, כלומר אומפרזול ו-Esomeprazole), תרופות אנטי-ניאופלאסטיות (כלומר, וינקריסטין וציקלופוספמיד), ותרופות אנטי-סוכרתיות (כלומר, כלורפרומיד, טולבוטמיד).
מספר תרופות עלולות לגרום להיפומגנזמיה [38]. תרופות אנטיבקטריאליות, כגון טטרציקלינים, יוצרות קומפלקס בלתי מסיס עם קטיוני מתכת; PPI וסותרי חומצה מורידים את ה-pH בקיבה וגורמים לוויסות מטה של הטרנספורטר הפעיל של המעי למגנזיום TRPM6, ואילו תיאזיד ומשתני לולאה מונעים ספיגה חוזרת של מגנזיום ברמת הכליה. חלק מהתרופות האנטי-נאופלסטיות (כלומר, ציספלטין) וגלולות למניעת הריון גורמים להפרשה מוגברת של מגנזיום בכליות. לבסוף, מעכבי calcineurin ומקשרי מעיים מבוססי ברזל קשורים גם להיפומגנזמיה [39].

מחסור בברזל עשוי לנבוע מספיגה מופחתת, הנגרם בעיקר על ידי אנטיביוטיקה כגון טטרציקלינים וקינולונים, ותרופות נוגדות הפרשת קיבה, כלומר אנטגוניסטים לקולטן PPI ו-H2 [40]. אכן, הפרשת חומצת קיבה מקלה על ספיגת הברזל החופשי, ומאפשרת המרתו לצורת ברזל הנספגת יותר מזו הברזלית; לפיכך, בהפחתת חומציות הקיבה, הספיגה התזונתית של מינרל זה פחות יעילה. מצב של היפוקלצמיה עשוי להיות תוצאה של ארבעה מצבים שונים [39,41]: hypoparathyroidism, hypovitaminosis D, חומרים קושרים סידן או הפרעה בספיגת עצם. התרופות הקשורות לרוב להיפוקלצמיה הן משתני לולאה (להפרשת סידן מוגברת), חומרים קלאטיים (כלומר, אתילן-דיאינטטראצטט, ציטראט, פוספט), תרופות אנטי-נאופלסטיות (כלומר, cisplatin, leucovorin, 5-fluorouracil, nab-paclitaxel, axitinib) , ביפוספטים, קלציטונין ודנוסומאב (נוגדן חד שבטי המשמש לטיפול באוסטיאופורוזיס).
תרופות שעשויות להקל על הפרשת נחושת ו/או אבץ מכילות בדרך כלל קבוצות סולפהדריל, כמו פרופילתיאורציל ומתימאזול, קפטופריל (ACEi) ופניצילאמין (בשימוש במחלת וילסון, דלקת מפרקים שגרונית וכו') [42]. מעניין שתרופות אלו עלולות לגרום גם לדיסגאוזיה.
שינויים נפוצים בזמינות ויטמין עשויים להשפיע על תיאמין (B1), ניאצין (B3) ופירידוקסין (B6), חומצה פולית, יחד עם ויטמינים B12, C ו-D. תרופות שעלולות לגרום למחסור בוויטמין B (בפרט B12, B6 ו-B3 ) הם בעיקר משתנים (הם מגבירים את הסרת ויטמינים B, B1 בפרט) ופיברטים. נוגדי חומצות כגון H2- אנטגוניסטים ו-PPI עשויים להפחית את ספיגת ויטמין B12 על ידי הפחתת חומציות הקיבה [43]. מחסור בוויטמין B12 עלול להופיע גם עם חומצה אצטילסליצילית (ASA), תרופות אנטי פסיכוטיות (כלומר, טריפלואורפרזין), קולכיצין, אסטרוגנים ומטפורמין [44]. ירידה ברמות ויטמין B6 וויטמין PP עלולה להתרחש במהלך טיפול בתרופות נוגדות דיכאון, במיוחד SSRI, וכמה תרופות נגד שחפת (כלומר, איזוניאזיד). מחסור בפולאט עלול להיגרם על ידי אנטיביוטיקה מסויימת (פניצילינים, צפלוספורינים, טטרציקלינים), פיברטים, גלולות למניעת הריון, ASA ותרופות אנטי-ראומטיות (כלומר מתוטרקסט), תרופות כימותרפיות מסוימות, נוגדי סוכרת פומיים (במיוחד ביגואנידים וסולפונילאוריאה), נוגדי פרכוסים (כלומר, , פנוברביטל, פרימידון) ונוירולפטיקה (פנוטיאזינים).
תרופות שיכולות לגרום למחסור בוויטמין C כוללות משתנים, גלולות למניעת הריון ו-ASA. מבין הוויטמינים המסיסים בשומן (A, D, E ו-K), המחסור בויטמין D הוא השכיח יותר ועשוי להיגרם על ידי תרופות כמו סטטינים, נוגדי חומצה, נוגדי פרכוסים (כלומר פניטואין), כולסטיראמין, גלוקוקורטיקואידים, ו sevelamer, קושר פוספט למעיים [45]. קו-אנזים Q10 (אוביקינון) הוא יסוד לתפקוד תקין של המיטוכונדריה. תרופות מסוימות עלולות להפריע לתפקודו, כמו במקרה של תרופות נוגדות סוכרת (ביגואנידים, מטפורמין, ובפרט סולפונילאוריאה גליבוריד וטולאזמיד), - חוסמים, סטטינים, קורטיקוסטרואידים, וורפרין ומשתנים (כלומר, אצטאזולאמיד).
3. אינטראקציה בין מזון ותרופות
האינטראקציות האפשריות בין מזון לתרופות רלוונטיות בפרקטיקות קליניות [46], אך לרוב אינן ידועות או מתעלמות מהן. הם מתרחשים בתדירות גבוהה יותר עם תרופות הניתנות דרך הפה [47]. ואכן, מזון ומשקאות עשויים לשנות את הפרופילים הפרמקוקינטיים והפרמקודינמיים של תרופה, מה שמוביל לשני מצבים שונים:
(1) ריכוז מוגבר בנוזלים ביולוגיים שעלולים לשפר את השפעת התרופה, עד לסיכון לתופעות לוואי ורעילות;
(2) ריכוזים מופחתים בנוזלים ביולוגיים, ובכך מופחתת השפעת התרופה, עם סיכון לחוסר יעילות מוחלט או חלקי.
הנקודה הראשונה שיש לקחת בחשבון היא שיש להכיר ולמנוע אינטראקציות וחומרתן, כדי למנוע את הסיכון של רעילות או חוסר יעילות טיפולית. ואכן, למרות שאינטראקציות רבות הן היפותטיות, חלקן יכולות להיות ברורות קלינית או יכולות להיות מסווגות כתופעות לוואי אמיתיות (ADR). תופעות לוואי הן תגובות לוואי לא מכוונות הנגרמות על ידי תרופה, ובמקרה של אינטראקציות עם מזונות, הן עשויות להיות בעלות מאפיינים של רעילות או כישלון טיפולי.

יש צורך להבחין בין שלושה גורמים העלולים להגביר את הסיכון לאינטראקציות חמורות: סוג התרופה המעורבת באינטראקציה, חומרת המחלה שעבורה ניתנת התרופה והמצב הכללי של המטופל [20,48]. תרופות בעלות אינדקס טיפולי נמוך יכולות להיות מעורבות באינטראקציות ברורות מבחינה קלינית בשל הטווח הצר שבין יעילות ובטיחות מאחר ותופעות לוואי יכולות להופיע במינונים המשמשים בדרך כלל לטיפול. מכאן שאפילו שינויים קטנים בריכוזי הדם או הפלזמה של תרופה עם טווח טיפולי צר עלולים לגרום לרעילות או לכשלים טיפוליים תרופות מדכאות חיסון (מעכבי קלציניורין או mTOR), תרופות הפעילות על מערכת הלב וכלי הדם (תרופות אנטי-ריתמיות, גליקוזידים קרדיו-אקטיביים, נוגדי קרישה דרך הפה ועוד. מערכת הנשימה (כלומר, תיאופילין) הן דוגמאות לתכשירים תרופתיים עם אינדקס טיפולי נמוך [49-51] תרופות הפעילות על מערכת העצבים המרכזית (כגון תרופות נוגדות דיכאון, תרופות מהפנטות, מייצבי מצב רוח ותרופות אנטי-אפילפטיות). יתר על כן, תרופות הניתנות למחלות כרוניות חושפות את המטופלים לסיכון גבוה יותר לאינטראקציות בגלל הגורם השני בחומרת המחלה שעבורה נדרשות התרופות, למשל, טיפול נוגד קרישה מעמיד את החולה בסיכון לסיבוכים דימומיים או פקקתיים, במקרים של מינון יתר או תת-מינון, בהתאמה [50]. באופן דומה, מטופל עלול להסתכן בדחיית האיבר המושתל או בהופעת רעילות במקרה של אינטראקציה עם אימונוסו! סמים מדכאים.
ניתן לזהות את הטרקטור השלישי במצבו הכללי של המטופל. לדוגמא, גיל מתקדם עשוי להיות קשור למחלות קרדיווסקולריות או מטבוליות, אשר עשויות להשפיע לרעה על התמרה ביולוגית של התרופה והכבד ועל הפרשת הכליות [50]. השינוי האפשרי בקצב הספיגה עלול להיגרם גם משינויים בתנועתיות המעיים, הרכב גוף שונה (כלומר, הפחתה במסת רקמת השומן), ומעל לכל, היכולת המופחתת של האורגניזם בתנאים קריטיים לבצע חילוף חומרים של תרופות ולחסל. אותם בצואה או בשתן. האינטראקציות העיקריות של מזון ותרופות מסוכמות בטבלה 3.
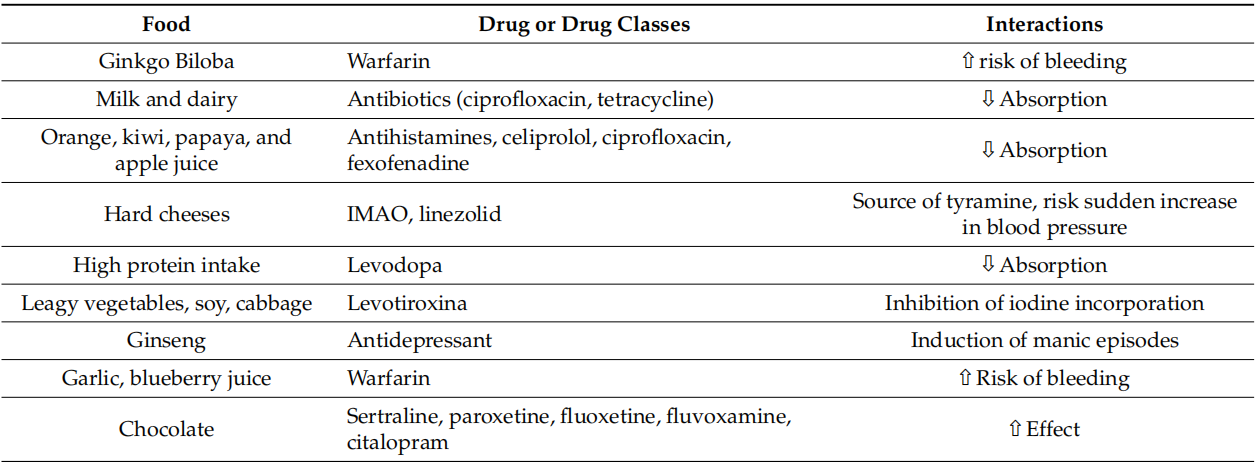
טבלה 3. אינטראקציות בין מזון לתרופה. מזונות שיש להימנע או לא לקחת יחד עם תרופות, בשל הסיכון להפרעות חמורות בתרופות.

4. פרמקוקינטיקה בסיס של אינטראקציות בין מזון לתרופות
אינטראקציות פרמקוקינטיות נוגעות לתהליכי ספיגה, הפצה, חילוף חומרים וסילוק. בנוסף למזונות בודדים או חומרים מזינים, אפילו הארוחה כולה יכולה להשפיע באופן משמעותי על הפרמקוקינטיקה של התרופה, על ידי שינוי הבטיחות והיעילות הטיפולית שלה [52-54]. יתרה מכך, צורות התרופות השונות בהן ניתן החומר הפעיל והמאפיינים הכימיים והפיזיקליים השונים, כגון מסיסות או חדירות לאורך מערכת העיכול, עלולים לגרום לתרופה להיות מושפעת אחרת מהמזון.
באופן כללי, בין ארבעת התהליכים התרופתיים, מזון יכול בעיקר להפריע לספיגה ולחילוף חומרים. אכן, השינויים בשני התהליכים הללו יכולים לשנות את הזמינות הביולוגית האפקטיבית של התרופה (כלומר, אחוז המנה של התרופה הפעילה שנמצאת בגוף לאחר מתןה). לאחר מתן דרך הפה, לוקח לתרופה כ-1-2 דקות להגיע לקיבה, שם היא מתמוססת, וחלק מהחומר הפעיל עובר לזרם הדם. החלק הנותר עובר לתוך המעי, שם הספיגה הושלמה. הימצאות מזון מסוג מסוים עלולה להוביל לאינטראקציה כימית-פיזיקלית, המורכבת מהיווצרות הקשר המולקולרי בין המזון למרכיבו, לבין החלק הפעיל של התרופה. כתוצאה מכך, סוג זה של הפרעות גורם לירידה בספיגת התרופה. מנגנון נוסף מבוסס על שינוי הפיזיולוגיה של מערכת העיכול [53], המתרחש כתוצאה מצריכת מזון, הפחתת חומציות הקיבה, עלייה בזמני ריקון הקיבה, שינויים בהפרשת המרה, עלייה בתנועתיות המעיים ושינוי במעיים. הרכב מיקרופלורה. כל השינויים הללו יכולים סוף סוף לשנות את קצב הספיגה של תרופה
5. שינויים בזמינות הביולוגית של תרופות
תרופות שהן חומצות חלשות נספגות ברמת הקיבה, בעוד שבסיסים חלשים נספגים רצוי ברמת המעי הדק. גם תכונות כימיות וגם פיזיקליות עשויות להשפיע על שלב הספיגה של תרופות, כגון קבוע הדיסוציאציה [55], פרמטר רגיש ל-pH המושפע מהיווצרות של קשרים ו/או קומפלקסים עם ישויות מולקולריות אחרות. לכן הכנסת מזון הגורם לשינוי ב-pH בתוך מערכת העיכול, במיוחד ברמת הקיבה, יכולה להשפיע על יכולת הספיגה של התרופה. בנוסף, עלולים להיווצר קשרים ו/או קומפלקסים בין התרופה לבין כמה מולקולות או יונים הכלולים במזון. שינוי בספיגת התרופה על ידי מזון או ארוחה יכול להתרחש גם על ידי קשירה של החומר הפעיל עם חלבון נושא התרופה; התחרות בין מזון לתרופות על הקישור עם חלבוני תחבורה יכולה להגביל את ספיגת הסוכן התרופתי.
לאורך מערכת העיכול, pH, זלוף, משטח ספיגה ליחידת נפח ותנועתיות עשויים להשפיע על קצב הספיגה של תרופות בדרכים שונות [56]. לדוגמה, זמן ריקון הקיבה וזמן מעבר המעי הם שני גורמים המשתתפים במתן מוצלח של התרופה [57]. בפרט, בליעת מזון מוצק, במיוחד אם חם, צמיג ועשיר בשומן, גורמת להאטה בזמני ריקון הקיבה ולפיכך לעיכוב בספיגת התרופה ברמת המעי, גם אם כמות התרופה הכוללת שנספגה. הוא ללא שינוי. יתר על כן, בליעת מזון מוצק מגרה את הייצור של מרה קיבה ומיצי לבלב, מה שבדרך כלל משפר את פירוק התרופה ומקל על ספיגתה [58]. ארוחות עם תכולת שומנים גבוהה מעוררות ייצור ושחרור גדול יותר של מרה בתריסריון, ומעדיפות ספיגה רבה יותר של אותן תרופות הזקוקות למלחי מרה לספיגה מיטבית. מעניין שחלק מהתרופות המצומדות עם חומצה גלוקורונית עוברות מחזור דם אנטרוהפטי המבטיח נוכחות ארוכה יותר בזרם הדם וברקמות [59].
6. שינויים עקב צריכת נוזלים, חלבון, שומנים וסיבים
צריכת נוזלים יכולה להשפיע על ספיגת התרופה. אכן, הנפח והטמפרטורה של המשקאות עשויים לשנות את מעבר התרופה דרך הקיבה, ולכן לשנות את הזמן הדרוש להופעת ההשפעה התרופתית [60]. למעט מים, צריכת כל משקה בשילוב עם התרופה עלולה להוביל לספיגה שונה של האחרון. כלומר, עשויים להיות שינויים ב-pH בקיבה, עיכוב של ריקון קיבה או תגובות קלציה, או מניעת ספיגת תרופות. לדוגמה, זה קורה עם קולה, קקאו, קפה (קפאין) וחלב [61,62]. זאת ועוד, השימוש במים לנטילת תרופות מונע היצמדות התרופה לוושט ולדופן הקיבה ומאפשר מעבר מהיר אל מקום הספיגה. יש לשים לב לטמפרטורת הנוזל: יש להימנע ממים חמים או קרים מדי, מכיוון שבשני המקרים זמן ריקון הקיבה עלול להתארך.
הרכב הארוחה עשוי להשפיע על ספיגת התרופה במספר דרכים. תכולה גבוהה של חומצות אמינו שמקורן בארוחה עתירת חלבון יכולה ליצור קשרים עם התרופה או להתחרות איתה על הקישור לנשאי התחבורה [63]. יתרה מכך, הפרשה מוגברת של מיצי הלבלב עלולה לגרום לכמות מוגברת של מים ברמת המעי, מה שמוביל לדילול תרופות. מצד שני, ארוחה עשירה בחלבון מגבירה את אספקת הדם למעי, מקלה ומזרזת את ספיגת התרופה. ארוחה עשירה בליפידים מעכבת את תנועתיות הקיבה ומגבירה את ייצור המרה [64]. ארוחה מסוג זה מסייעת בספיגת התרופות המכונה "ליפופיליות". להיפך, תכולת הסיבים בארוחה מגבירה את תנועתיות מערכת העיכול ומפחיתה את זמן מעבר המעי. כתוצאה מכך, הזמינות הביולוגית של תרופות מופחתת, יחד עם ההשפעות הפרמקודינמיות שלהן.
מקרה מיוחד של הפרעות מזון-תרופות מתרחש בין צריכת מזונות עשירים בטירמין (מונואמין הנובע מחומצת האמינו טירוזין) ותרופות IMAO, הגורמות להצטברות מוגזמת של מונואמינים שגורמת לעלייה חריפה בלחץ הדם וכאבי ראש. במקרה זה, התזונה צריכה להגביל את צריכת גבינות קשות, בשר בקר, בשר מעובד, תמצית שמרים, פירות יבשים, סויה, שוקולד וכו'. חשוב לשים לב גם לצריכת טירמין במהלך הטיפול בלינזוליד, תרופה משמש לטיפול בזיהומים קשים. אכן, לינזוליד פועל כמעכב MAO, ולכן מתן בו-זמנית עם מזונות עשירים בטירמין עלול לגרום לעלייה פתאומית בלחץ הדם. גורם חשוב נוסף הוא הזמן בין מתן התרופה ביחס לארוחה או לצריכת המזון [65]. התרופות הרגישות ביותר לאינטראקציות אלו הן בעיקר אלו שאינן יציבות בנוזלי קיבה או שיש סיכוי גבוה יותר ליצור קשרים עם מולקולות מזון. מסיבה זו, התרופות מחולקות לשתי קטגוריות עיקריות: תרופות שיש ליטול עם ארוחה או בשילוב עם ארוחה (ניתן בחצי השעה לפני הארוחה או אחריה) ותרופות שיש ליטול ללא אוכל, כלומר בערך שעתיים לפני או 3-4 אחרי הארוחה.

7. שינויים בתפוצת התרופות
מספר גורמים משפיעים על נפח ומהירות הפצת התרופה, בהתאם לרקמה שבה מופצת התרופה והמאפיינים הכימיים-פיזיים של התרופה, כך שאחוז השומן והמסה הרזה של הנבדק משפיעים על קצב ההפצה של התרופה, זמן מחצית החיים שלה והזמן הדרוש כדי להגיע למצב יציב, הן בחולים מבוגרים והן בחולים בילדים [66]. הפרמקוקינטיקה של התרופה הליפופילית תלויה בעיקר במסת הגוף השומנית. רקמת השומן דלה במים (במיוחד תוך תאית), ובקושי מכילה כלי דם. תכולת מים נמוכה יותר גורמת לפיזור נמוך יותר של תרופות הידרופיליות ברקמת השומן ופיזור גדול יותר של ליפופיליות [67]. להיפך, תרופות הידרופיליות הניתנות לנבדקים הסובלים מעודף משקל או השמנת יתר, בעלי אחוז גבוה יותר של מסת גוף שומנית, מופצות בנפח נמוך יותר של מים. לכן, חישוב המינון על סמך משקל הגוף בפועל עלול לחשוף את הנבדק לסיכון של מנת יתר, מכיוון שכמות הנוזלים שבה מופצת התרופה אינה פרופורציונלית למשקל הגוף. כתוצאה מכך, לתרופה תהיה ריכוז פלזמה גבוה יותר זמן מחצית חיים ארוך יותר, וככל הנראה השפעות גדולות מהצפוי, גם אם כלל זה עשוי שלא להיות נכון עבור כל התרופות [68,69]. גורם נוסף המשפיע על חלוקת התרופות מיוצג על ידי הקישור לחלבוני פלזמה מכיוון שרק הצורה החופשית של התרופה יכולה להתפשט בתוך החלל החוץ-וסקולרי או בתוך התאים שבהם היא מפעילה את השפעותיה. יש לציין, אלבומין קושר תרופות חומציות, בעוד שתרופות בסיסיות חומצות אלפא-גליקופרוטאינים וליפופרוטאינים, בשילוב עם מספר גורמים (כלומר, מחלות כבד וכליות, דלקות, סרטן), עשויות להשפיע על ריכוז חלבוני הפלזמה הזמינים לקשירת תרופות [70,71 ].
שינויים בהרכב הגוף מתרחשים לא רק במקרה של עודף משקל/השמנה, או הפחתת מסת גוף רזה אלא גם בטווחי גילאים קיצוניים. ואכן, גם אצל יילודים וגם אצל קשישים, הרכב הגוף שונה בתכלית מאשר אצל מבוגרים. בילודים, יש אחוזים גבוהים של מי גוף (75-80% בערך) ואחוזים נמוכים של מסת שומן, בעוד בקשישים יש ירידה פיזיולוגית במי הגוף ועלייה ברקמת השומן [72,73]. עם הגיל המתקדם, ישנה גם יכולת קשירה נמוכה יותר של חלבוני פלזמה (כלומר, היפואלבומינמיה), נפח פלזמה נמוך יותר, פעילות אנזימטית מופחתת, וירידה בתפקוד הכליות. הדבר מוביל לשינוי בנפח הפצה של תרופות: בחולים מבוגרים יותר, לתרופות מסיסות במים יש נפח פיזור נמוך יותר, בעוד שלתרופות מסיסות שומן יש נפח פיזור גבוה יותר ביחס למשקל הגוף.
8. שינויים במטבוליזם של תרופות
ראוי לציין כי תרופות, רכיבי תזונה ומזון עלולים להשפיע על פעילות אנזימי הכבד, וכתוצאה מכך חילוף חומרים מוגבר או מופחת של תרופות, וכתוצאה מכך השפעה תרופתית מופחתת או מוגברת, בהתאמה. צורות האיזו של CYP450 (כלומר, CYP3A4,5,6, CYP1A2, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6 ו-CYP2E1) הם האנזימים החשובים ביותר המעורבים בביוטרנספורמציה של תרופות.
בפרט, צריכת מזונות מסוימים (כלומר, סויה) או משקאות (כלומר מיץ אשכוליות ואוכמניות) עשויה לעכב את הפעילות של אנזימי ציטוכרום P450, ובכך לשנות את ריכוז התרופה ברמת אתר הפעולה של היעד [74] ]. במקרה של מיץ אשכוליות, העיכוב נמשך מספר שעות ופעילות הכבד CYP3A4 חוזרת לנורמה תוך 48 שעות מצריכת המיץ [75]. ברור שהסיכון לאינטראקציה בין מזון לתרופה, שיכולה להיות רלוונטית מבחינה קלינית, עשויה להיות תלויה בבטיחות התרופה (כלומר, אינדקס טיפולי), משך הצריכה במקביל של התרופה והמזון, וכן, לבסוף, על המצבים הקליניים של החולה וחומרת המחלה. יתר על כן, תזונה עשירה בתכולת חלבון ושומנים אך דלה בפחמימות מסוגלת לעכב את פעילות ה-CYP450, וכתוצאה מכך להגביר את ריכוז הפלזמה של התרופה. עיכוב זה חמור במיוחד עבור שרשראות ארוכות ובלתי רוויות של חומצות שומן [76].
9. שינויים בחיסול תרופות
ההכליה אחראית בעיקר לסילוק רוב התרופות, באמצעות סינון גלומרולרי והפרשה צינורית. ראוי לציין כי החלק החופשי של התרופה המסונן על ידי גלומרולוס יכול, עם זאת, להיספג מחדש במהירות ברמה הצינורית, אם הוא בצורה לא מיונן. אופי החומצה או הבסיס החלש של התרופה מסביר את שיווי המשקל בין הצורה המנותקת והלא מנותקת התלויה ב-pH של האולטרה-פילטר, וכתוצאה מכך את ההפרשה הסופית או הספיגה מחדש של הצורה המנותקת או הבלתי מנותקת של התרופות, בהתאמה. לכן, כל אותם מאכלים או משקאות שיכולים להחמצן או להכשיר את השתן, יכולים לשנות את הספיגה ולהקל על הפרשת תרופות מסוימות. דוגמה לכך היא מה שנקרא דיאטות בסיסיות או מחמצות [77]. תזונה בסיסית מאופיינת בנוכחות של ירקות ופירות טריים וצריכה מופחתת של מזונות מחמיצים; הוא עשיר בגופרית, זרחן וכלור, הכלול במזונות כגון גבינה, בשר, נקניקיות, ביצים, סוכרים פשוטים, קמחים מזוקקים, קפה ותה. להיפך, בתזונה המחמצת, צריכת חלבונים ממקור מן החי גבוהה, ודלה בפירות, ירקות וקטניות (מה שנקרא דיאטות מערביות). ניתן להגדיר את החומציות או הבסיסיות של המזון על ידי מדד PRAL (Potential Renal Acid Load): מזונות עם PRAL שלילי עלולים להיות בסיסיים, בעוד שאלו עם PRAL חיובי מחמיצים [77]. חלק מהמזונות "ניטרליים", או מחמיצים מעט, כמו דגנים מלאים, קטניות, חלב ופירות יבשים.
10. פרמקודינמיקה ופרמקוקינטיקה של אינטראקציות בין מזון לתרופות
ניתוח של הספרות המדעית הראה שתשומת לב מועטה מופנית לחקירת אינטראקציות בין מזון לתרופה. יתר על כן, מזון מכיל כל כך הרבה תרכובות המסוגלות להפריע לתרופות שקשה לחקור את כולן [78]. הסבר נוסף הוא שריכוזי מרכיבי המזון וחומרי הזנה המסוגלים לשנות את הפרמקודינמיקה של התרופה תלויים במספר משתנים, כגון סוג הפרי/ירק, המוצא הגיאוגרפי, עונת הקציר, מידת ההבשלה של הפרי/ירק ואחסון. תנאים [79]. מסיבה זו, רוב המחקרים התמקדו בעיקר בתוספי מזון ומשקאות, או תמציות כגון מיצי פירות, תה, תה צמחים, משקאות אלכוהוליים, קפה וחלב.

11. ירקות עשירים בויטמין K
בין האינטראקציות בין תרופות למזון הידועות ביותר, הקשר של וורפרין למזונות עשירים בוויטמין K הוא ללא ספק הידוע ביותר. השפעת הוורפרין נובעת מסינתזה לא מלאה של גורמי קרישה, באמצעות קרבוקסילציה של שאריות חומצה גלוטמית, שעבורן ויטמין K ממלא תפקיד חיוני. מזונות עשירים בוויטמין K עלולים להפריע להשפעה הטיפולית של התרופה. מזונות אלו מיוצגים בעיקר על ידי מצליבים (ברוקולי, כרוב וכו'), חסה, תרד, פטרוזיליה וכו'. תכולת ויטמין K גבוהה עשויה להימצא גם באספרגוס, אפונה, עדשים, סויה, חלמון ביצה, כבד וכו'. למרות זאת בסיכון, חולים בטיפול בוורפרין עשויים לאכול את הירקות הללו, תוך שימת לב לאכילת כמות מתונה לאורך זמן, לאכול את אותה כמות מדי יום, ולהתאים את מינון הוורפרין בהתאם. מטה-אנליזה עדכנית דיווחה כי ההגבלה של צריכת ויטמין K אינה נראית כאסטרטגיה שימושית לשיפור היעילות של warfarin [80]. מספר מחקרים מצאו קשר שלילי בין צריכת ויטמין K לבין וריאציות של היחס המנורמל הבינלאומי (INR), בעוד שאחרים מצאו קשר חיובי, אך תלוי מינון: עם צריכה מינימלית של ויטמין K, עדיין ניתן לשמור אפקט נוגד קרישה נאות. אם הצריכה עולה על 150 מיקרוגרם ליום של ויטמין K, השפעת התרופה משתנה [80]. לכן, גישה שימושית להתגבר על בעיה זו היא לשמור על הרגל תזונה יציב, הימנעות משינויים נרחבים בצריכת ויטמין K [80,81].
12. מזונות גויטרוגניים
אינטראקציה נוספת בין מזון לתרופות היא בין לבוטירוקסין לבין מזונות שנקראים גויטרוגניים, הכוללים מצליבים (כרוב, כרובית, ברוקולי וכו'), סויה, חסה ותרד, חלב ותוספים מסוימים כמו ניטריטים. מזונות אלו יכולים להפריע לחילוף החומרים של יוד החיוני לפעילות תקינה של בלוטת התריס באמצעות סינתזה של הורמוני בלוטת התריס T3 ו-T4 [82]. אכן, הריכוז הגבוה של איזותיוציאנטים במזונות אלו יכול לעכב את שילוב היוד ולכן היווצרות של תירוקסין, ירידה בתפקוד בלוטת התריס [83]. עם זאת, ברוב המקרים, אין הדבר מעיד על החרגה מוחלטת של מזונות אלו מהתזונה. אפשר לצרוך אותם תוך שימת לב לכמות, לתדירות ולזמן הצריכה. בכל מקרה, מטופלים עשויים לקבל מזונות אלו מדי פעם, במנות מתונות ולא לפני 30-60 דקות מצריכת הלבותירוקסין.
עם זאת, חלק מהאינטראקציות הללו לא אושרו, כמו במקרה של סויה שעלולה להגביר את הסיכון להיפותירואידיזם. סקירה שיטתית עדכנית הראתה שאכילת סויה אינה משפיעה על הורמוני בלוטת התריס ועלולה לגרום לעלייה מתונה ברמות ההורמון הממריץ את בלוטת התריס (TSH) [84]. לכן, במסגרת תזונה מגוונת, ניתן לצרוך סויה בנבדקים עם בעיות בבלוטת התריס, בתנאי שהתזונה אינה חסרה ביוד. יש לנקוט זהירות מיוחדת במקרה של Hashimoto thyroiditis המטופל ב-levothyroxine, מכיוון שסויה יכולה להפריע לתרופה זו. עם זאת, צריכת פולי סויה במרחק של לפחות 4 שעות מהתרופה יכולה להיחשב בלתי מזיקה [84].
13. מיצי פירות או ירקות
מיצי אשכוליות, תפוזים, תפוחים, רימונים, אוכמניות ועגבניות נחקרו על האינטראקציות הפוטנציאליות שלהם עם תרופות. מבין כל מיצי הפירות, מיץ אשכוליות הוא הידוע ביותר [85]. זהו מעכב חזק של פעילותם של כמה איזופורמים של הציטוכרום P450 הפעילים במעי, איזופורם CYP3A4 בפרט, האחראי על ניקוי רעלים של כ-50% מהתרופות. פעילות מעכבת זו נובעת מחומרים מסוימים הכלולים באשכולית ובמיץ שלה, כלומר הנרינגין (תרכובת פנולית בעלת תכונות אנטי-דלקתיות ונוגדות חמצון) ו-bergamot tin (furanocoumarin). רשימת התרופות שעלולות להיות מושפעות ממיץ אשכוליות היא ארוכה, וכוללת תרופות נפוצות כמו [86]:
פלבונואידים הכלולים במיץ אשכוליות, כגון נרינגן והספרידין, אחראים לעיכוב של טרנספורטרים טרנסממברניים, אשר ממלאים תפקיד במעבר התרופה לומן המעי בתוך זרם הדם. תרכובות אלו קיימות גם במיצי פירות אחרים, כגון מיצי פירות הדר. ואכן, מיצי תפוזים, תפוחים, קיווי ופפאיה, המכילים את אותם פלבנואידים (נרינגין, הספרידין ופלורידין, פלורטין) מסוגלים לעכב את הפוליפפטידים המשלוחים של אניונים אורגניים (OATP) במינונים הרגילים. כלומר, 1-2 פירות בגודל סטנדרטי או 200 סמ"ק של מיץ מסחרי או ביתי מספיקים כדי לעכב תהליך זה [79,87-89]. צריכת מיצי פירות אלו קובעת את ההפחתה בספיגת מערכת העיכול של תרופות אנטיביוטיות מסוימות, נוגדות לחץ דם, חוסמי בטא ואנטי-אלרגיות. בפרט, מתן משותף של תרופות כגון acebutolol, celiprolol או fexofenadine עם מיץ אשכוליות, או atenolol, ciprofloxacin, ו-fexofenadine עם מיץ תפוזים, מקטין את הזמינות הביולוגית דרך הפה של תרופות נוגדות יתר לחץ דם ואנטי-היסטמינרגיות [90].
כמה מחקרים העלו כי מיץ אלוורה יכול להפחית את היעילות של כמה תרופות כימותרפיות, אם כי הוא עשוי להגביר את ההשפעה של תרופות נוגדות סוכרת דרך הפה עקב ירידה נוספת ברמות הגלוקוז בדם כאשר מיץ אלוורה נלקח עם תרופות אלו. אין ליטול את מיץ האלוורה עם תרופות כגון משתני תיאזיד, גלוקוקורטיקואידים וגליקוזידים קרדיואקטיביים, כדי למנוע את הסיכון להפרשת אשלגן מוגברת בכליות המובילה להיפוקלמיה [95]. מיץ אננס או תמציות שלו יכולים לקיים אינטראקציה עם NSAIDs, וורפרין, נוגדי טסיות והפרין, ולגרום לסיכון מוגבר לדימום. מיצי ירקות כגון מיצי כרוב, בצל ומיצי פלפל ירוק הוכחו כיכולים לעכב באופן תחרותי את פעילות CYP3A4 [93]. עם זאת, השפעות מעכבות אלו לא נבדקו in vivo, ומספר הפלבנואידים הכלולים בירקות אלה תלוי בתנאי הגידול, כך שלא ניתן להסיק בוודאות שכרוב ובצל יכולים לעכב פעילות CYP3A4 ברמה קלינית [94] ]. מיץ עגבניות מכיל מעכב ישיר תחרותי אחד או יותר של פעילות CYP3A4 [96]. השפעה זו נצפתה גם בצמחי שמש אחרים, כגון תפוחי אדמה, חצילים ופלפלים; לכן, מאמינים שירקות אלה חולקים את אותן תרכובות מעכבות [97].
בסך הכל, מחקרים אלה מביאים מידע חשוב נוסף. ראשית, מיץ טרי או תוצרת בית נוטה פחות לעכב את ספיגת התרופות מאשר מיץ מסחרי. שנית, הוכח כי הירידה בספיגת התרופה עומדת ביחס ישר לכמות המיץ הנצרכת ולזמן שבין המיץ לצריכת התרופה [87]. באופן כללי, נצפה כי מומלץ לפרק זמן של ארבע שעות בין צריכת המיץ לצריכת התרופה כדי למנוע כל סיכוי לאינטראקציה [87]. למחקרים אלה יש מספר מגבלות, כשהחשובה ביותר היא שהם בוצעו במבחנה. מחקרים מעטים חקרו אינטראקציות בין תרופות למזון in vivo, ולעיתים רחוקות בבני אדם [91]. החשיפה הקצרה למזון וחומרי מזון, שנמשכת בדרך כלל שבועיים, יכולה להסביר את היעדר ניסויים קליניים [98,99].
#cistanche #cistanchedeserticola #cistanchetubulosa #cistanchesalsa #glycoside #echinacoside #verbascoside #acteoside #ニクジュヨウ #肉蓯蓉 #ベルバスコゆゃギニン #エキナコシド
שירות תומך של Wecistanche:
דוא"ל:wallence.suen@wecistanche.com
ווטסאפ/טלפון:+86 15292862950






