גילוי של מעכבי STING חדשים המבוססים על המבנה של העכבר STING Agonist DMXAA
Nov 27, 2023
תַקצִיר:
חלבון הממריץ-של-אינטרפרון-גן (STING) מעורב בחסינות מולדת. התרופה DMXAA (5,6-dimethylxanthenone-4-חומצה אצטית) הוכיחה את עצמה כאגוניסט עכברי-STING (mSTING), אך השפיעה מעט על STING (hSTING) של האדם. במאמר זה, אנו מסתמכים על השוואה בין מבני גביש שונים וניתוח יחסי אינטראקציה בין חלבון לליגנד כדי להעלות את ההשערה שלעיצוב התרופה של גרסאות DMXAA יש פוטנציאל להמיר אגוניסטים של STING למעכבים. בהתבסס על הגילוי הקודם שלנו של שני אנלוגים של DMXAA, 3 ו-4 (שניהם יכולים להיקשר ל-STING), ביצענו אופטימיזציה מבנית שלהם וסנתזנו נגזרות חדשות, בהתאמה. במבחני קשירה, מצאנו תרכובות 11 ו-27 כמייצגות קושרי STING שהיו עדיפים על המבנים המקוריים ודנו ביחסי מבנה-פעילות. כל תרכובות המטרה לא היו פעילות במבחנים תאיים לבדיקת פעילות אגוניסטית של STING. למרבה הצער, זיהינו 11 ו-27 כמעכבי STING עם פעילות מיקרומולרית גם במסלולי hSTING וגם ב-mSTING. בנוסף, 11 ו-27 עיכבו את האינדוקציה של אינטרפרון וציטוקינים דלקתיים שהופעלו על ידי 20 3 0 -cGAMP ללא ציטוטוקסיות נראית לעין. ממצאים אלו שוברים את החשיבה הנוקשה לפיה DMXAA מספק את הבסיס המבני במיוחד לאגוניסטים של STING ופותח אפשרויות נוספות לפיתוח אגוניסטים או מעכבי STING חדשים.

cistanche tubulosa- לשפר את המערכת החיסונית
מילות מפתח:
לַעֲקוֹץ; DMXAA; סלקטיביות מינים; אגוניסט STING; מעכב STING
1. הקדמה
הסטימולטור-של-אינטרפרון-גן (STING) הוא מולקולת איתות חיונית לחסינות פנימית, המתווכת בעיקר תגובות חיסוניות טבעיות הנגרמות על ידי DNA ציטופלזמי [1]. כאשר קולטן ה-DNA המחזורי גואנוזין-אדנוזין פוספט סינתאז (cGAS) מזהה DNA דו-גדילי תוך תאי, cGAS מזרז את הסינתזה של 2 0,30 -cGAMP (איור 1), דינוקלאוטיד מחזורי (CDN) המסוגל של קישור ישיר והפעלת STING על הרשת האנדופלזמית [2-4]. עם ההפעלה, STING יוצר אגרגטים המגויסים במורד הזרם ל-TANK-binder kinase 1 (TBK1) וקושרים אינטרפרון רגולטורי 3 (IRF3), אשר מזרחן IRF3, מפעיל דימרים IRF3 לתוך הגרעין, גורם לביטוי אינטרפרון מסוג I (IFN) ומתניע. תגובה חיסונית של אינטרפרון [1]. מחקרים רבים הראו כי STING מעורב בפתוגנזה של מחלות מרובות וכי גירוי של STING משרה תגובות חיסוניות יעילות לזיהומים פתוגניים וסוגי סרטן; עם זאת, כישלון בוויסות איתות דלקתי כרוני מוביל למחלות אוטואימוניות ודלקתיות [5-8]. בשל התפקיד הבסיסי של STING בוויסות החסינות המולדת, מספר רב של צוותים החלו לפתח אגוניסטים או מעכבי STING.
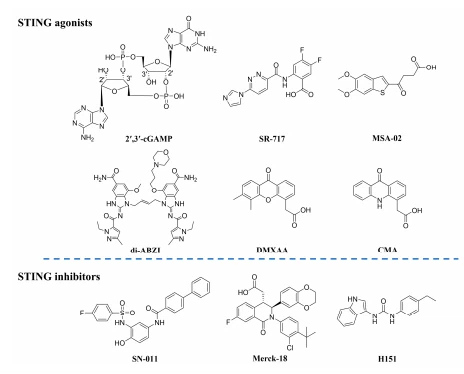
איור 1. מאפננים STING נציגים
מחקר על אגוניסטים STING מהדור הראשון התמקד בשינוי מבני של אנלוגים ל-CDN כדי לעקוף מגבלות מסוימות של CDNs אנדוגניים, כגון חדירות ממברנה ירודה ורגישות להידרוליזה על ידי פוספטאזות [9,10]. המולקולה הקטנה STING אגוניסט 5,6-dimethylxanthenone-4-חומצה אצטית (DMXAA), שהראתה הבטחה טיפולית נגד גידולים מוצקים במודלים של עכברים, יכולה לנטרל את החסרונות של נגזרות CDN [11]. עם זאת, התרופה נכשלה בניסויים קליניים בבני אדם [12]. עוד מאשרים כי DMXAA נקשר באופן סלקטיבי ל-STING של עכבר (mSTING) ולא ל-STING אנושי (hSTING) [13,14], מה שפוגע בפוטנציאל הטיפולי של DMXAA בבני אדם. 10-Carboxymethyl-9-acridinone (CMA) הוא אגוניסט STING מייצג אחר של עכברים ששימש כגורם חזק מסוג I IFN לטיפול אנטי ויראלי בתחילת שנות ה-70 [15]. לכן, סלקטיביות מינים היא גורם חיוני בפיתוח של אגוניסטים STING-מולקולות קטנות. אגוניסטים משמעותיים של hSTING-שלד הובאו לעין על ידי המאמצים הבלתי נלאים של חוקרים, כולל diABZI, SR717, MSA02 ואחרים [16-19].

יתרונות cistanche לגברים מחזקים את המערכת החיסונית
עדויות מתגברות מראות שהיפראקטיבציה של STING קשורה למחלות אוטו-דלקתיות ואוטואימוניות. יש צורך להגביל את ההפעלה המוגזמת של מסלול האיתות STING, מה שמדגיש את הערך הפוטנציאלי של מעכבי STING. בניגוד לאגוניסטים של STING, הפיתוח של מעכבי STING עדיין בחיתוליו, ועדיין לא נכנסו למחקרים קליניים מועמדים לתרופה. מעכבי STING הידועים כוללים שני סוגים של תרכובות: אנטגוניסטים תחרותיים (SN-011 ו-Merk-18) ומעכבים קוולנטיים (H151) [20-22]. מעכבי STING קוולנטיים שזוהו קודם לכן מקיימים אינטראקציה עם Cys88/91 או Cys91 שנמצאים בתחום הטרנסממברני ה-N-טרמינלי של STING מחוץ לכיס הקושר ל-CDN [22]. לאחרונה, שני צוותים דיווחו ברציפות על שני סוגים מבניים של אנטגוניסטים של STING התופסים את כיס הקישור של 20 3 0 -cGAMP כדי לעכב את ההפעלה של 20 3 0 -cGAMP, מה שמרמז על אפקט דו-צדדי בכיס המקשר ל-CDN [20 ,21].
כאן, אנו מספקים נקודת מבט חדשה. אנו מציעים שהכיס התחתון בו נמצאים DMXAA ו-CMA מקל על פיתוח מעכבי STING בהתבסס על כריית הנתונים העמוקה שלנו והשוואה של מידע מבנה הגביש המשותף של חלבוני STING שזוהו. המחקר הקודם שלנו דיווח על סדרה של אנלוגים של CMA ו-DMXAA וזיהה תרכובות 3 ו-4 הנקשרות ל-hSTING אך עם עוצמה תאית חלשה [23] (איור 2).

איור 2. מבנים כימיים של תרכובות 3 ו-4 עם נתונים על פעילותם הביולוגית. ערכי EC50 של תרכובות 1-4 נמדדו על ידי תאי כתב STING, וה-IC50s המקשרים נמדדו על ידי ערכות קשירה מתחרות של STING.
במאמר זה, בנוגע לתכנון של מעכבי STING לגילוי חומרי קשירה חזקים יותר עם יותר מגעים בכיס התחתון, ביצענו אופטימיזציות מבניות עבור 3 ו-4, בהתאמה. לאחר מכן, ערכנו מחקר SAR המבוסס על מבחני מחייבי תחרות. בהערכת הפעילות הביולוגית, תרכובות 11 ו-27 פעלו כמקשרים רחבי טווח והציגו רמות מיקרומולריות של פעילות מעכבת STING במספר תאים מדווחים. מבחינת מבנה העגינה, שתי מולקולות תרכובת 11 מחזיקות hSTING במבנה "פתוח" לא פעיל, ובכך מעכבות באופן תחרותי את הקישור האנדוגני 20 3 0 -cGAMP, הדומה למבנה הגבישי של Merck-18 ולמבנה העגינה. של SN-011 [20,21].
2. תוצאות
2.1. אסטרטגיית עיצוב של נגזרות DMXAA כמעכבי STING
2.1.1. זיהוי אתרי עיצוב עבור מעכבי STING על ידי השוואה בין מבני קריסטל שונים
האפו-חלבון של ה-STING ligand binding domain (LBD) התגבש כדימר סימטרי ב-non-ligand, אשר הוכח שאינו נגרם על ידי סינון ג'ל וניתוח אולטרה צנטריפוגה אנליטי [24-26]. דימר STING מאמץ מבנה דמוי פרפר עם אתר הקישור של הליגנד ממוקם בממשק בין שני המונומרים. ראשית, מאמר זה בוחן את מנגנוני התשתית וההפעלה של חלבוני hSTING ו-mSTING, משווה את ההבדלים ביניהם, וכן חושף כמה תובנות מסקרנות. עבור מבנה האפו, הקונפורמציה הטבעית של שני החלבונים מראה שה-mSTING מרוכז יותר מה-hSTING (איור 3). שי וחב'. השתמשו בסימולציות של דינמיקה מולקולרית (MD) כדי לחקור את ההבדלים בין hSTING ל-mSTING, והראו כי hSTING מעדיף קונפורמציה פתוחה-לא פעילה, ו-mSTING מעדיף קונפורמציה פעילה סגורה גם ללא ליגנד קשור [27].
כאשר הוא קשור ל-20,30 -cGAMP, המעבר הקונפורמטיבי של ה-hSTING הוא מפתוח (אפו-חלבון, מרחק לרוחב ~57 Å) לסגור (חלבון קשור לcGAMP, מרחק לרוחב ~40 Å), ואילו ההפך נכון עבור mSTING (29 Å עד 40 Å). המבנה של apo-hSTING שונה באופן דרמטי מזה של apo-mSTING, אבל המבנים של STING מורכבים עם 20,30 -cGAMP חופפים. DMXAA, CMA ו-cGAMP הם אגוניסטים של STING עם פיגומים מבניים מגוונים, אך גם קונפורמציות ההפעלה שלהם בעת הקישור לחלבוני mSTING זהים בעצם (איור 3). התרחישים שתוארו לעיל מעידים שמנגנוני הגירוי של hSTING ו-mSTING שונים בצורה מדהימה; עם זאת, הקונפורמציות המופעלות על ידי STING הן קבועות יחסית, ללא תלות בסלקטיביות המינים ובסוג עמוד השדרה האגוניסט (בעוד שהן מוגבלות לאגוניסטים של STING המביאים לשינויים קונפורמטיביים). נפחי הכיס הקישור של מתחמי הגביש השונים מתכנסים בדרך כלל (~300 Å3, טבלה S1), המהווה עדות נוספת ליציבות קונפורמציה של הפעלת חלבון STING.

איור 3. השוואה בין מבני גבישי STING הקשורים ל-apo ולתרכובת. חלבון mSTING הוא חיטה (המרחק נבדק עם קו אדום), קוד PDB:4KC0 (apo), 4LOJ (bound-cGAMP), 4LOL (bound-DMXAA) ו-4JC5 (bound-CMA)
שנית, בהתבסס על הממצאים לעיל של יציבות קונפורמציה של הפעלה, העלינו מבנים משותפים גבישיים של cGAMP, DMXAA, CMA, SR717 ו-MSA02, שהם אגוניסטים STING-קונפורמציוניים סגורים, כדי לחקור את מיקומם של האגוניסטים המבניים השונים ב- אתרי קשירת חלבון STING. ניתן לחלק את כיס החלבון לשני אזורים: הכיס התחתון והכיס העליון, בעקבות הפצה של אגוניסטים STING בכיס החלבון (איור 4א). פרט לכך שאגוניסטים של mSTING DMXAA ו-CMA נמצאים לגמרי בכיס התחתון, האגוניסטים האחרים יכולים להפעיל את מסלול ה-hSTING ולשכב באזור העליון. לאחר מכן מיפינו את האינטראקציות של חמשת אגוניסטים STING עם שאריות חומצות אמינו הקשורות לחלבון STING (בתוך 5 Å מהליגנד; איור S1), והראנו שחומצות האמינו הראשוניות כללו R238, Y167, R232, S162, T263 ו-T267 (מספר הרצף של השרידים המקבילים ל-mSTING מינוס אחד). התאמת השאריות ברצף לכיסים הראתה ש-T267, T263 ו-S162 נמצאים בכיס התחתון; הכיס העליון מכיל R238, R232 ו-Y167 (איור 4b). כפי שדווח, R238, Y167 ו-R232 חיוניים לקשירת אגוניסט ל-STING, במיוחד R238 (חלבון mSTING מתאים ל-R237), שהמוטציה שלו תגרום לאובדן מוחלט של ייצוב (קישור ליגנד) [28-30]. Che et al. גם חשף ששארית המפתח R238 שולטת בקישור של DMXAA, והמוטציות הנקודתיות (S162A/E260I) יכולות לשפר את האינטראקציה של R238 עם DMXAA על ידי סימולציות MD [31].

cistanche tubulosa- לשפר את המערכת החיסונית
לחץ כאן לצפייה במוצרי Cistanche Enhance Immunity
【בקש עוד】 דוא"ל:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
כדי לכבוש את כיס החלבון של mSTING, DMXAA או CMA אימצו מצב קישור ייחודי שבו שני אגוניסטים בעלי מולקולה קטנה נקשרים להומודימר אחד של mSTING. ה-DMXAAs מתנוססים בחוזקה בכיס התחתון על ידי קשרי מימן בין קבוצת הקטו לשרשרת הצדדית T266 (hSTING תואמת ל-267), בעוד שקבוצת הקרבוקסילטים מקיימת אינטראקציה עם שרשראות הצד R237 ו-T262 (איור 5a). האינטראקציה של DMXAA עם R237 (חומצת האמינו המרכזית היחידה בכיס העליון) היא קריטית לפעילות mSTING. פרט שמתעלמים ממנו לעתים קרובות הוא ש-DMXAA יכול לפעול רק על R237 של חלבונים מונומריים סימטריים, למשל, DMXAA (מולקולה A) המשפיעה על R237B (איור 5a). מכיוון ש-DMXAA יושב בתחתית, המרחק בין מולקולה A ל-R237B הוא 3.06 Å, בעוד שהמרחק ל-R237A גדול מ-5 Å (איור 5b). נהנה מהכיס הקומפקטי יותר של חלבון mSTING, DMXAA מקיים אינטראקציה ללא מאמץ עם R237 של המונומר mSTING הסימטרי, אך אין דרך ל-DMXAA לקשר עם כל אחד מה-R238 בחלבון apo-hSTING הפתוח מבחינה קונפורמטיבית (איור 3). לפיכך, מיקום הכיס של DMXAA פוגע בגירוי של מסלול hSTING. לאחרונה, Merck, בהשראת יחס הקישור של DMXAA 2:1, גילתה אנטגוניסטים של STING המסוגלים לכבוש את כיס הקישור [21]. קומפלקס הגבישים של Merck 18 וחלבון hSTING מראה שהתרכובת ממוקמת בעיקר מתחת לכיס החלבון ומקיימת אינטראקציה עם S162, T263 ו-T267, שכולם תואמים את המאפיינים של DMXAA (איור 5c). מכאן נוצרו השערות: הכיס העליון הוא חלל מצוין לעיצוב אגוניסטים של STING; הכיס התחתון הוא קן מתאים יותר למעכבים, והמבנה של DMXAA או CMA מותאם לפוטנציאל להפוך לאנטגוניסט STING.

איור 4. חלוקה של אתרי הקישור של STING והפצה עם חומצות אמינו מפתח. (א) מיקום שני אזורים במונומר STING. הכיס התחתון בצבע מגנטה והכיס העליון ירוק. קודי PDB עבור מתחמי הגביש החופפים הם כדלקמן: 4LOH (cGAMP, ירוק), 6UKV (MSA-02, צהוב), 6XNP (SR717, כתום), 4LOL (DMXAA, מגנטה) ו-4JC5 (CMA, סָגוֹל). (ב) התפלגות של חומצות אמינו מרכזיות באזור העליון והתחתון. השאריות בכיס התחתון מוצגות במגנטה, והירוקים נמצאים באזור העליון.

איור 5. קומפלקסים קריסטליים של DMXAA ו-Merck 18. (א) מגעים בין-מולקולריים בקומפלקס של DMXAA ו-mSTING. ה-DMXAA המחובר מוצג בצבע אפור, עם תת-יחידות STING בודדות בדימר הסימטרי מוצגות בירוק ובסגול. הכתבים העיליים של A ו-B מציינים מונומר חלבון או זהות ליגנד בודדת. (ב) מרחקים בין שיירי מפתח R237A ו-R237B, בהתאמה, לבין DMXAA (מולקולה A). R237A לקרבוקסיל של DMXAA הוא 6.02 Å, R237B לקרבוקסיל של DMXAA הוא 3.06 Å. (ג) מבנה גבישי של Merck 18 הקשור לחלבון hSTING (PDB 6MXE) ופרטים על המגעים הבין-מולקולריים שלו. הליגנד הקשור מוצג בצבע אפור, עם יחידות משנה STING בודדות בדימר הסימטרי מוצגות בירוק ובסגול. הכתבים העיליים של A ו-B מציינים מונומר חלבון או זהות ליגנד בודדת

איור 6. בסיס מחקר והנקודות החמות המוטבות שלנו עבור נגזרות DMXAA ו-CMA. (א) סופרפוזיציה של המבנה של DMXAA קשור ל-mSTING (PDB: 4LOL, מוצג כחול כהה) עם המבנה של DMXAA קשור ל-hSTING S162A/G230I/Q266I (PDB: 4QXR, מוצג כתום). (ב) פרטים של DMXAA קשור ל-hSTING שעבר מוטציה (PDB: 4QXR). תיבות הקו המקווקו מייצגות את אתרי השינוי הפוטנציאליים. שאריות אמינו המוצגות בירוק הן שאריות מוטציות (S162A/Q266I).
מצאנו שחוסר היכולת של DMXAA להפעיל את מסלול האירוח היה קשור למיקום של DMXAA בכיס התחתון (לפי סעיף 2.1.1), מה שגם סיפק לנו את הרעיון העיצובי של מעכבי STING: הגדלת המגעים של נגזרות DMXAA עם האזור התחתון באמצעות שינויים מבניים כדי לשמור על STING במבנה שאינו מופעל. S162 ו-Q266 נמצאים כראוי בתחתית אתר הקישור, כך שניתן למקם DMXAAs היטב במגע ישיר עם שניהם, מה שמקל על חקירת ההשפעה של חומצות אמינו בכיס התחתון על ליגנדים. ניתוח קשרי המבנה-פעילות (SARs) גילה שחלק 5,6-דימתיל ומתוקסי מיקום C7- היו קריטיים לפעילות הביולוגית של 3 ו-4. כפי שמוצג באיור 6b, ה-5 ,6-קבוצת דימתיל יצרה אינטראקציות הידרופוביות עם חומצות אמינו מרובות בכיס התחתון; עקב הקרבה של מיקום C7 של DMXAA לחומצת אמינו Q266, השינוי המתוקסי המתאים אפשר ל-3 ול-4 להיקשר לאירוח. לכן, העיבודים המבניים שלנו הניחו את הנעילה של 5,6-דימתיל ומתוקסי C7, והתכנון של נגזרות חדשות התמקד בשינוי הקבוצה הקוטבית במיקום C1/C2 (המשפיע על S162) ושינוי קבוצת החומצות הקרבוקסילית ( הרחבת המגוון המבני). תכננו וסינתזנו סדרה של נגזרות תוך שימוש בתרכובות 3 ו-4 כפיגומים, ובכך אימתנו את השערת המעכבים המוצעת שלנו.
2.2. כִּימִיָה
ההכנה של כל תרכובות הביניים והמטרה מתוארת בסכימה 1. 1-מתוקסי-2,3-דימתיל-4-ניטרובנזן (5) וחומצה 2-ברומובנזואית ( 7) היו זמינים מסחרית. בתחילה, 1-מתוקסי-2,3-דימתיל-4-ניטרובנזן הומר ל4-מתוקסי- 2,3-דימתילאנילין (6) באמצעות הפחתה עם אבקת ברזל. לאחר מכן, 6 ו-7 היו נתונים לתגובת אולמן עם אשלגן קרבונט עם קטליזה על ידי תחמוצת נחושת ונחושת (I) ב-N, N-דימתילפורמיד כדי לספק את תוצר הביניים המקביל 8. תגובת העיבוי התוך מולקולרית של 8 בוצעה עם ריאגנט של Eaton כדי להעניק תוצר ביניים 2-methoxy-3,4-dimethylacridin-9(10H)-one (9). ההחלפה שלאחר מכן של 9 בוצעה באתיל ברומואצטט, והאובדן של 1 אקוויו של HBr העניק אתיל 2-(2-methoxy-3,4-dimethyl-9- אוקסואקרידין-10(9H)-איל)אצטט (10). לבסוף, אתיל אצטט ב-10 עבר הידרוליזה לחומצה קרבוקסילית על ידי נתרן הידרוקסיד והניב 2-(2-methoxy-3,4- dimethyl-9-oxoacridin-10 (9H)-יל) חומצה אצטית (11).

תכנית 1. א. EtOH, Fe, NH4Cl; ב. DMF, Cu, Cu2O, K2CO3; ג. מגיב של איטון; ד. BrCH2COOC2H5 , NaH; ה. NaOH; ו. CCl3CH(OH)2, NH2OH; ז. H2SO4; ח. EtOH, H2O2, NaOH.
לסינתזה שלאחר מכן של תרכובות מטרה נוספות, עלינו לסנתז תחילה את התרכובת 2-אמינו-5-מתוקסי-3,4-חומצה דימתיל-בנזואית (14). 6 הגיב עם הידראט כלור והידרוקסילאמין, ויצר אצטאמיד והידרוקסיאמינו, עם תוצר הביניים (E)-2-(hydroxylamine)-N-(4-methoxy-2,3-dimethylphenyl )אצטמיד (12). תגובת הסידור מחדש של בקמן שלאחר מכן של ההידרוקסיאמינו של 12 בוצעה עם חומצה גופרתית כדי להעניק נגזרת לקטם 13. לבסוף, תוצר ביניים 13 עבר הידרוליזה עם מי חמצן ונתרן הידרוקסיד בתמיסת אתנול והניב 14. באמצעות 14 כחומר המוצא לתגובה, סינתזה עוד סדרה של 8-מתוקסי-9,10-דימתיל-6הפירולו[3,2,1-דה]אקרידין-1,6( נגזרות 2H)-דיון עם תחליפים ב-R1 ו-R2. בתחילה, 14 ו-15-19 היו נתונים לתגובת אולמן עם אשלגן קרבונט עם קטליזה על ידי תחמוצת נחושת ונחושת(I) ב-N, N-דימתילפורמאמיד כדי לספק תוצרי ביניים מתאימים 20-24. תגובות העיבוי התוך-מולקולריות של 20-24 בוצעו עם ריאגנט של Eaton כדי להעניק 8-מתוקסי-9,10-דימתיל-6H-pyrrolo[3,2,{{46} }דה]אקרידין-1,6(2H)- דיון נגזרות (25-29). באופן דומה, תוך שימוש ב-14 כחומר המוצא לתגובה, סינתזנו עוד סדרה של 7-מתוקסי-5,6-דימתיל-9-אוקסו-9,{{ 59}}דיהידרו-אקרידין-4- נגזרות חומצה קרבוקסיליות עם תחליפים ב-R. בתחילה, 14 ו-7 או 30 היו נתונים לתגובת אולמן עם אשלגן קרבונט עם קטליזה על ידי תחמוצת נחושת ונחושת(I) ב-N, N-דימתיל-פורמאמיד כדי לספק תוצרי הביניים המתאימים 31 ו-32. תגובות העיבוי התוך-מולקולריות של 31 ו-32 בוצעו עם ריאגנט של Eaton כדי להעניק 7-מתוקסי-5,6-דימתיל-9-אוקסו-9 ,10-דיהידרו-אקרידין-4-נגזרות של חומצה קרבוקסילית (33,34). לפיכך, תכננו, סיננתזנו והקרנו 16 אנלוגים של אקרידון, שהמבנים שלהם מסוכמים בטבלה 1.
טבלה 1. מבנים של האנלוגים החדשים של המחקר הנוכחי.

2.3. עוצמת הקישור של תרכובות חדשות ל-STING ול-SARs שלהן
עוצמת הקישור של תרכובות חדשות ל-STING ול-SARs שלהן כדי לאשר ישירות את יעילות השינוי המבני, בדקנו תחילה את כל התרכובות המסונתזות על ידי מבחני עקירה של cGAMP. בנוסף לסלקטיביות המינים, ישנן חמש גרסאות של STING שהן פולימורפיות בבני אדם, R232 (WT, 58% מהאוכלוסייה), HAQ (20%), H232 (13%), AQ (7%) ו-Q ( 2%) [32]. לפיכך, השתמשנו בערכות בדיקת התחרות המסחריות על ידי טכנולוגיית פלואורסצנציה הומוגנית בזמן (HTRF) כדי לבדוק את העוצמה הביוכימית של תרכובות חדשות על mSTING ואיזופורמים שונים של hSTING (WT, H232 ו-AQ) והשווינו אותם לבקרה. כצפוי, תרכובות הבקרה 1-4 היו קשורות כולן ל-mSTING; ממסך hSTING, לתרכובות 3 ו-4 היו ערכי IC50 ברמה המיקרומולרית.
טבלה 2. התוצאות של תרכובות עם איזופורמים שונים של hSTING ומבחני קשירת תחרות mSTING.

ראשית, בהתבסס על תרכובת 3, הוכנס אטום הלוגן או קבוצת מתוקסי באתר C1/C2 (טבלה 1). לתרכובת 27, כנגזרת האופטימלית של תרכובת 3 (מיקום C1 מוחלף ב-F), יש פעילות כוללת טובה יותר מאשר לתרכובת 3 (פעילות מיקרומולרית חד ספרתית בכל המבחנים הביוכימיים, טבלה 2). לתרכובת ה-R1-שונתה 25 יש אפקט קשירה רחב של ספקטרום, אך אינו פעיל כמו הגרסה המוחלפת או הבלתי-מוחלפת. בהשוואה לתרכובת 3, התרכובות (26, 28 ו-29) עם קבוצת C2-אתר שהוצגה הראו כולן דרגות שונות של ירידה באפיניות הקישור, במיוחד תרכובת 29. שנית, שמירה על עמוד השדרה של תרכובת 4 והחלפה אטום ההלוגן כנגד אתר C1/C2, השגנו תרכובות 35-38 (טבלה 1). תרכובות אלו לא היו פעילות בכל ארבעת מבחני העקירה בריכוזים של עד 100 מיקרומטר, מה שמוכיח שהחלפה באטום הלוגן באתר C1/C2 אינה נסבלת. לאחר מכן, הפכנו את קבוצת האצטאט בתרכובת 4 לקבוצת קרבוקסיל (33) והכנסנו מתוקסי באתר C2 (34). למרבה הצער, שינוי זה היה כישלון מכיוון ששתי התרכובות נותרו לא פעילות. למדנו מהכישלון שלנו, חקרנו עוד את ה-SARs של נגזרות התרכובת 4 על ידי העברה של קבוצת האצטט למיקום N והשארת עמדות C1/C2 ללא שינוי. תרכובת 11 מציגה קישור למגוון רחב של גרסאות STING, כולם עם IC50s מתחת ל-20 µM; הפעילות עדיפה על תרכובת 4 ובהשוואה לתרכובת 27. בנוסף, תרכובת 9 (ללא קבוצת קרבוקסיל באתר N) ותרכובת 10 (N-אצטט אתיל) הן מבשרות סינתטיות של תרכובת 11 שאינן יכולות להיקשר ל-STING, מה שמוכיח בעקיפין חשיבותה של קבוצת החומצות הקרבוקסיליות.
2.4. הערכה ביולוגית תאית
2.4.1. הקרנה חוץ גופית של אנלוגים חדשים עם פעילות אגוניסטית של STING
בדקנו באופן שיטתי את כל התרכובות לפעילות אגוניסטית של STING באמצעות שורות 293T hSTING-WT, 293T-mSTING ו-THP1-KO-STING הכתבות (מסופקות על ידי Invivo Gen). באמצעות תאי 293T-hSTING-R232 ותאי 293T-mSTING, הראינו הפעלה של מסלול ה-IRF כמדד עקיף של השראת IFN מסוג I על ידי ניטור פעילות פוספטאז אלקליין עוברי מפריש (SEAP), שתרם למחקר שלנו על סלקטיביות המינים של תרכובות. תאי THP1-KO-STING נוצרו מתאי THP1-כפולים על ידי נוקאאוט יציב של הגן STING, והשתמשנו בתאי THP1-KO-STING כדי לאשר אם התרכובת מציגה את הפונקציה של אינדוקציה של ציטוקינים תלויי STING. השווינו את הפעילות האגוניסטית של STING של כל הנגזרות הממוקדות לאלו של אגוניסטים הייחוסים עבור STING של עכברים (DMXAA) ושל אנושיים (20,30 -cGAMP). באופן מפתיע, אף אחת מהתרכובות המסונתזות לא יכלה להפעיל את מסלולי hSTING או mSTING (ריכוז מקסימלי ב-200 µM), דבר שאינו עולה בקנה אחד עם תוצאות מבחני הקישור. לכן, לסוכני הקישור של STING שנבדקו עשויים להיות דפוסי קישור פוטנציאליים כאנטגוניסטים חדשים של STING.
2.4.2. בדיקה חוץ גופית של קלסרים STING עם פעילות מעכבי STING
ראשית, עשינו ניסויים מקדימים: עם המעכב הקוולנטי H151 של 1 µM כהתייחסות חיובית, חקרנו את הרמות המעכבות שלו בשורות תאים מדווחות mSTING ו-hSTING שתורבו יחד עם ריכוזים שונים של 20 3 0 -cGAMP כדי לקבוע את התנאים האופטימליים לסקר המעכב (ראה סעיף 4.2.3 לפרטי פרוטוקול). שנית, בדקנו תחילה את העוצמה המעכבת של התרכובות החדשות על ידי טיפול בשיטות טרום ניסוי בריכוז של 100 מיקרומטר. מצאנו שהתרכובות קושרות STING רחבות הספקטרום 11 ו-27 הפגינו עיכוב מצוין בתאי כתב STING של עכברים וגם בתאי STING אנושיים, כאשר תרכובות 3 ו-4 והתרכובות האחרות אינן יעילות באותה מידה. שלישית, הגדרנו שיפועים בריכוז עבור תרכובות 11 ו-27 כדי לבדוק את שני ערכי ה-IC50 ולהשוות אותם עם H151. תרכובות 11 ו-27 היו פעילות בריכוזים מיקרומולריים המעכבים ביטוי IFN- המושרה על ידי 20 3 0 -cGAMP הן במסלולי hSTING והן במסלולי mSTING.

cistanche tubulosa- לשפר את המערכת החיסונית
עם ערכי IC50, תרכובת 11 (hSTING 19.93 µM ו-mSTING 15.47 µM) עלתה על תרכובת 27 (hSTING 38.75 µM ו-mSTING 30.81 µM) (איור 7א). לשם השוואה, ערכי ה-IC50 של H-151 בתאי 293T-hSTING ו-293T-mSTING היו 1.04 ו-0.82 µM (איור 7a), מה שמצביע על כך שהמעכב הקוולנטי H-151 מפגין השפעה מעכבת טובה יותר על STING איתות תלוי במבחנים מבוססי תאים. כדי לאשש עוד יותר את התכונה המעכבת של תרכובות 11 ו-27, השתמשנו בשורת תא מדווחת מונוציטים אנושית THP-1 אחר THP1-Dual-hSTING-R232, המשתמשת במערכת דו-מדווחת כדי לדווח על הפעלת IRF כמדד עקיף להשראת IFN מסוג I ועל הפעלת NF-κB כמדד עקיף להשראת ציטוקינים פרו-דלקתיים. לאחר גירוי קו תא הכתב THP-1 עם 20,30 -cGAMP, הוספנו מעכבי STING עם ריכוזים מתאימים לעיכוב האינדוקציות של I IFN וציטוקינים פרו-דלקתיים. כצפוי, תרכובות 11, 27 ו-H151 עיכבו באופן משמעותי את הפעלות של מסלולי IRF ו-NF-KB המופעלים על ידי STING (איור 7b). בנוסף, כדי לשלול את ההשפעה של ציטוטוקסיות של התרכובות על הפעילות המעכבת, השתמשנו בערכת CellTiter-Glo כדי לבחון את הפעילות התאית. למרבה הצער, תרכובות 11 ו-27 לא הראו עדות לציטוטוקסיות לתאי 293T ו-THP-1 על ידי בדיקת כדאיות התא כאשר הוספו בריכוזים (5 עד 100 מיקרומטר) המעכבים STING, בניגוד ל-H151, שכבר הראה ציטוטוקסיות משמעותיות ב- 10 מיקרומטר (איור 7ג). מחקרים אלו זיהו את התרכובות 11 ו-27 כמעכבי STING מתונים, שובר את הרגישות למין ומעכב את המסלולים הכפולים IRF ו-NF-KB ללא ציטוטוקסיות נראית לעין.
2.5. הבסיס המבני של פעילות מתחם 11 נחקר על ידי עגינה
המנגנון של אנטגוניסטים תחרותיים של STING הוא לכבוש את אתר הקישור ולשבש את קונפורמציית ההפעלה של חלבון STING [20,21]. ספציפית ל-hSTING, אנטגוניסטים משאירים את דימר hSTING במבנה "פתוח". השתמשנו ב-Glide docking כדי לקבוע את האינטראקציה בין STING CTD (PDB ID code 6MXE) לבין התרכובת הפעילה הטובה ביותר 11. במבנה העגינה, שתי התרכובות 11 מקבילות בחלקן זו לזו ושוכנות בתחתית השסע של דימר hSTING (איור 8א), נועל את hSTING במבנה פתוח לא פעיל (איור S2). תרכובת 11 מייצרת בעיקר אינטראקציות הידרופוביות, כאשר המבנה הטריציקלי של הליגנד מאפשר מגע רב יותר עם הממשק בכיס התחתון. כמו עם DMXAA או CMA, קבוצת הקרבוקסיל יוצרת קשר מימן עם השרשרת הצדדית של T263, בעוד שקבוצת הקטו יוצרת קשר מימן עם השרשרת הצדדית של T267. המתוקסי בעמדה C2 מקיים אינטראקציה אינטימית עם S162, וכתוצאה מכך קרבת ליגנד-ליגנד אחד כלפי השני. תחליפי הביס-מתיל לא רק יוצרים אינטראקציות ליגנד-ליגנד אלא גם ממוקמים בנוחות בכניסה לכיס העליון, מה שמונע את הקישור של אגוניסטים STING טבעיים לשאריות מפתח (איור 8b).

איור 7. קושרי STING רחבי טווח 11 ו-27 הם אנטגוניסטים של STING. (א) מבנים כימיים של תרכובות 11 ו-27, והפעילות המעכבת של מעכבי STING כנגד מסלולי m- ו- h- STING כאחד. תאי 293T (mSTING או hSTING), שטופלו מראש בריכוזים שונים של תרכובות, עוררו על ידי 20,30 -cGAMP; עיכוב פעילות מסלול ה-IRF נמדד בעקיפין על ידי ערכי צפיפות אופטית (OD). עקומת המעכב התלויה במינון הותאמה כדי לחשב את ה-IC50 של תרכובות. (ב) תרכובות 11 ו-27 יכולות לעכב את ההפעלה של מסלולים כפולים של hSTING. שורות תא מדווחות THP1-hSTING-R232 עוררו עם 20,30 -cGAMP, וטופלו בתרכובות, תוך עיכוב אינדוקציה של IFN (הערכת הפעילות על ידי יחידות האור היחסיות (RLU) של Lucia luciferase ) והשראת ציטוקינים פרו-דלקתיים (ניטור הפעילות של SEAP הנמדדת לפי ערכי OD). (ג) אנלוגים חדשים מפגינים ציטוטוקסיות נמוכה בהשוואה למעכב הקוולנטי. תאי 293T (או THP-1) הודגרו עם הריכוז המצוין של מעכבים לפרקי הזמן המצוינים. כדאיות התא נמדדה על ידי ערכות CellTiter-Glo. הנתונים המוצגים הם הממוצע משלושה ניסויים עצמאיים. NS (לא משמעותי) p > 0.05, *** p < 0.001. ערכי p חושבו על ידי מבחן t דו-זנבתי.

איור 8. מבנה עגינה של תרכובת 11 הקשורה לחלבון STING. (א) אופן הקישור של תרכובת 11. הליגנד המחובר מוצג בצבע אפור, עם יחידות משנה STING בודדות בדימר הסימטרי מוצגות בירוק ובסגול. בכיסי הכריכה של מונומר STING החלק התחתון בצבע מגנטה והחלק העליון ירוק. (ב) המגעים הבין-מולקולריים של תרכובת 11 קשורים ל-STING. תרכובת 11 וחומצות אמינו STING שנקשרו בהן מוצגות כמודל מקל. המגעים הבין-מולקולריים וקשרי המימן מוצגים בקו מקווקו צהוב. הכתבים העיליים של A ו-B מציינים מונומר חלבון או זהות ליגנד בודדת.
3. דיון
לאור הדיווחים הנרחבים על המנגנון והמבנה הגבישי של STING, יש לנו הזדמנות להסביר את הבעיה המדעית מדוע ל-DMXAA אין פעילות אגוניסטית STING אנושית. במחקר זה, בהשוואה של מבני גבישי STING שונים, השגנו כמה ממצאים מעניינים: 1. קונפורמציה של הפעלת STING יציבה; 2. ישנם מנגנוני הפעלה שונים עבור hSTING ו-mSTING; 3. DMXAA ו-CMA נמצאים בתחתית אתר הקישור ומבדילים אותם מאגוניסטים אחרים. בהתחשב במנגנוני ההפעלה השונים של mSTING ו-hSTING, אגוניסטים של mSTING DMXAA או CMA הממוקמים בכיס התחתון אינם יכולים להפעיל הפעלה ב-hSTING מכיוון של-apo-hSTING יש חלל קישור גדול יותר המונע מהליגנד להתחבר ל-R238.
Gao et al. דיווח כי מוטציות בודדות (G230I, S162A ו-Q266I) מקנות ל-hSTING את אותה רגישות DMXAA כמו mSTING [33]. הדמיות MD גילו ששרשרת הצד של אזור המכסה G230I מספיקה כדי ליצור מחסום סטרי למניעת הפרשת DMXAA, בעוד ש-DMXAA יוצא בקלות ב-hSTING WT [27]. בהתבסס על השינוי המבני התואם למוטציות נקודת hSTING (S162A/Q266I) באתר הקישור, אנלוגים משמעותיים של DMXAA ו-CMA היו זמינים אך ללא אגוניסטים חזקים של hSTING. הסיבה מאחורי זה עשויה להיות שהפער המבני העדין בין hSTINGs "טבעיים" ו"מוטטים" עשוי למלא תפקיד מכריע בתהליך הזיהוי. באמצעות סימולציות של MD, Che et al. מצאו שה-hSTINGs שעברו מוטציה לא טבעית מפריעים לתנועות המתואמות של מולקולות מים ומשנים את כמות המים הנפלטת בעת קשירת ליגנד, מה שמתאים יותר לשחזור הפעלת ה-DMXAA של hSTING [31].
מעודדים מגילוי המחקר של מעכבי STING באתר הקישור התחתון [21], אנו מעיזים לחזות כי ל-DMXAA, הממוקם באותו אזור, יש פוטנציאל להפוך למעכבי STING חדשים. במחקר קודם, איחנו את המבנים של DMXAA ו-CMA עם שינויים מבניים עדינים וגילינו בהצלחה 3 ו-4 שיכולים להיקשר ל-hSTING, אך פעילות ה-STING האגוניסטית החלשה שלהם אינה תואמת את עוצמת הקישור שלהם. במאמר זה, רעיון העיצוב הוא לשפר עוד יותר את המגעים של אנלוגי DMXAA עם הכיס התחתון כדי להתנגד באופן תחרותי לקשירה של 20,30 -cGAMP, אז תכננו וסינתזנו מבנים אופטימליים של תרכובות 3 ו-4.

cistanche tubulosa- לשפר את המערכת החיסונית
שלב ההקרנה הראשון היה לבדוק את הפעילות הביוכימית באמצעות ערכות הקישור של וריאנטים מרובים של STING כדי לאפיין את עוצמת הקישור של הנגזרות החדשות. התוצאות של מבחני הכריכה הוכיחו את תקינות כיווני העיצוב שלנו; זיהינו את 11 ו-27 כמקשרי STING רחבי טווח (עדיפים על 3 ו-4) ודנו ב-SARs. עבור האנלוגים של תרכובת 3, השינויים במיקום C1 שיפרו משמעותית את הקישור לגרסאות STING שונות, בעוד שלתרכובות שעברו שינוי ב-C2- לא הייתה השפעה. עם זאת, תרכובת 4 לא נסבלת היטב עבור שינויים מבניים ב-C1/C2. לאחר מיקומו של מיקום החומצה הקרבוקסילית (C4 ל-N), מצאנו את המקשר הטוב יותר STING 11 וקבענו שקבוצת החומצה הקרבוקסילית חיונית לפעילות. לאחר מכן, בדקנו את כל התרכובות לפעילות ברמת התא באמצעות שלוש שורות תאים מדווחות, ואף אחת ממרכיבי המטרה לא הייתה פעילה. לאחר מכן הקמנו שיטת סקר למעכבי STING וסקרנו מחדש את כל האנלוגים החדשים. חומרי הקישור של STING 11 ו-27 הציגו פעילות מעכבת מיקרומולרית, עם נתונים דומים למבחן הקישור התחרותי. המעכב הקוולנטי H151 הראה פעילות מעכבת STING מעט טובה יותר מאשר 11 ו-27 במבחנה. בנוסף, אימתנו עוד ש-11 ו-27 יכולים לעכב ביעילות 20,30 -הפעלה הנגרמת על ידי cGAMP של מסלולים כפולים של STING. באופן המרשים ביותר, 11 ו-27 שומרים על רמה גבוהה של כדאיות תאים בריכוזים גבוהים, מה שלא אפשרי עם H151. ציטוטוקסיות היא בעיה שכיחה עם מעכבים קוולנטיים ומגבילה את היישום של H151.
על ידי ניתוח עגינה, רכשנו תובנה לגבי הבסיס המבני של פעילות התרכובת הפעילה הטובה ביותר 11. תרכובת 11 תופסת את הכיס התחתון בצורה מושלמת, מחזיקה את hSTING במבנה פתוח לא פעיל ובכך מעכבת באופן תחרותי את הקישור של 20,30 -cGAMP. המבנה של הטבעת הטריציקלית של אקרידין הוא המפתח ליצירת אינטראקציות הידרופוביות, כאשר קבוצת החומצות הקרבוקסיליות וחלק הקטון מעגנים את התרכובת בתחתית הכיס. אנו משערים שהמתוקסי מייצר אסוציאציות אינטימיות עם ה-S162, מושך את מבנה החלבון סגור באופן שולי אך לא מספיק כדי להפוך אותו לקונפורמציה אגוניסטית. מבנה הביס-מתיל יוצר חסימת אתר מרחבית המשפרת אינטראקציות ליגנד-ליגנד ופוגעת בכניסה אגוניסט לכיס העליון. נכון לעכשיו, אין מבנים משותפים גבישיים של אנטגוניסטים של mSTING ו-STING, כך שאיננו יכולים להסביר את מנגנון הפעולה של תרכובת 11 עם mSTING באמצעות גישת עגינה. עם זאת, אנו משערים כי קיימות שתי אפשרויות: האחת היא שעיקרון הפעולה זהה לזה של hSTING; השני הוא שתרכובת 11 שומרת את mSTING בקונפורמציה אפו מצטברת יותר ו-20,30 -cGAMP לא יכול להיכנס לכיס כדי להפעיל את האפקט האגוניסטי. לסיכום, האופטימיזציות המבניות העדינות שלנו של אגוניסטים חלשים של STING הפכו בהצלחה את התפקוד הביולוגי לגילוי מעכבי STING. ממצאים אלה ממחישים את המורכבות של כיסי הקישור של STING ומספקים תובנות מחקריות חדשות לפיתוח תרופות של אגוניסטים או מעכבי STING.
4. חומרים ושיטות
4.1. כִּימִיָה
ממיסים וריאגנטים המשמשים בסינתזה התקבלו מ-Beijing Innochem Science and Technology Co., Ltd (בייג'ינג, סין). המבנים של המוצרים זוהו על ידי ספקטרוסקופיה של 1H ו-13C-NMR (JNM-ECA-400, יפן). המשקלים המולקולריים של המוצרים נמדדו באמצעות ספקטרומטריית מסה ברזולוציה גבוהה (HRMS) עם יינון אלקטרוספריי (ESI) כמצב היינון (Agilent 1260-G6230A, גרמניה). NMR וספקטרום מסה של התרכובות מסופקים בחומרים המשלימים. תרכובות 35-38 סונתזו וזוהו על ידינו; אנא עיין במאמר שדווח בעבר לפרטים [23].
אתיל {{0}}(2-מתוקסי-3,4-דימתיל-9-אוקסואקרידין-10 (9H)-איל)אצטט (1{ {25}}): לתמיסה של 4-מתוקסי{{10}},3-דימתילאנילין (6) (0.97 גרם, 6.4 ממול) ו 2-חומצה ברום-בנזואית (7) (1.29 גרם, 6.4 ממול) ב-DMF (6 מ"ל) בטמפרטורת החדר, הוספנו לאחר מכן אבקת Cu (0.05 גרם), Cu2O ({{60}}.05 גרם) ו-K2CO3 ({{186}}.71 גרם, 5.1 ממול). תערובת התגובה חוממת ל-110 ◦C למשך 12 שעות. לאחר הסרת הממסים תחת ואקום, השארית הומסה בתמיסת 1 N NaOH (25 מ"ל). התוצר הגולמי הושג על ידי משקעים עם החמצה של התסנין עם קונצרן. HCl. לאחר הייבוש, התוצר הגולמי הוסף לריאגנט של Eaton (5 מ"ל) בטמפרטורת החדר, ואז התערובת חוממה ל-90 מעלות צלזיוס למשך שעה אחת. תערובת התגובה המקוררת הושלכה לתמיסת NaHCO3 מימית רוויה. המשקע סונן כדי לאסוף את המוצר הגס. טיהור של השאריות על ידי כרומטוגרפיה של עמודת סיליקה ג'ל סיפק 9, מוצק צהוב חיוור (0.61 גרם, 37.7% תשואה). תמיסה של NaH (1.43 מ"ל) ו-9 (0.33 גרם, 1.3 מ"ל) ב-DMF (5 מ"ל) בטמפרטורת החדר עורבה במשך שעה אחת ולאחר מכן מקוררה ל-5-7 מעלות צלזיוס. האתיל ברומואצטט (0.43 גרם, 2.6 מילימול) הוסף לתערובת שהתקבלה ונערבב ללא הרף בטמפרטורת החדר במשך 20 שעות. לאחר השלמת התגובה (TLC), תערובת התגובה נשפכה למי קרח (15 מ"ל). המשקעים שהתקבלו סוננו, יובשו ולאחר מכן חולצו עם כלורופורם. אידוי של הממס נתן אסטר גולמי שטוהר על ידי התגבשות מחדש כדי לספק 10, מוצק צהוב (0.33 גרם, 76% תשואה). 1H NMR (400 MHz, DMSO-D6) δ 8.30 (d, J=8.4 Hz, 1H), 8.08 (d, J=8.6 Hz, 1H), 7.75–7.67 (m , 1H), 7.57–7.50 (מ', 1H), 7.48 (s, 1H), 5.02 (s, 2H), 4.22 (q, J=7.1 Hz, 2H), 3.96 (s, 3H) , 2.77 (s, 3H), 2.34 (s, 3H), 1.21 (t, J=7.1 Hz, 3H). 13C NMR (101 MHz, DMSO-D6) δ (ppm): 169.25, 157.87, 155.96, 147.46, 146.72, 135.46, 132.15, 130.17, 129.1218, 8. 19.46, 95.26, 72.06, 61.28, 56.06, 14.59 , 14.34, 13.77. HRMS (ESI) m/z [M+H]+ מחושב עבור C20H21NO4: 339.3910 נמצא: 340.1546. 2-(2-מתוקסי-3,4-דימתיל-9-אוקסואקרידין-10(9H)-איל) חומצה אצטית (11): תמיסה של 10 (0.37 גרם, 1.1 מ"ל) ו-NaOH (0.05 גרם, 1.3 מ"ל) באתנול (20 מ"ל) ובמים (2 מ"ל) חוממו ל-60 מעלות צלזיוס למשך שעה אחת. לאחר הסרת הממיסים, השאריות שנוצרו הומסו במים וסוננו. לאחר נטרול התסנין עם קונקרטי. HCl, התערובת סוננה כדי לקבל את המוצק הגולמי, לאחר מכן התגבשה מחדש על ידי מתנול כדי לתת 11, אבקה צהובה חיוורת (0.29 גרם, 85.7% תשואה). 1H NMR (400 MHz, DMSO-D6) δ 10.51 (s, 1H), 8.33 (d, J=6.9 Hz, 1H), 8.04 (d, J=8.5 Hz, 1H ), 7.69 (s, 1H), 7.67-7.62 (m, 1H), 7.45 (t, J=6.8 Hz, 1H), 4.52 (s, 2H), 3.90 (s, 3H), 2.75 (s, 3H), 2.31 (s, 3H). 13C NMR (101 MHz, DMSO-D6) δ (ppm): 159.04, 155.63, 147.47, 146.64, 134.86, 131.52, 129.56, 128.98, 125.63, 5.91215, 5. 01.77, 96.02, 74.81, 55.69, 14.42, 13.33 . HRMS (ESI) m/z [M+H]+ מחושב עבור C18H17NO4: 311.3370 נמצא: 312.1229.
{{0}}כלורו-8-מתוקסי-9,10-דימתיל-6H-פירולו [3,2,1-דה]אקרידין{ {9}},6(2H)-דיון (25): לתמיסה של 6-קרבוקסי-4-מתוקסי-2,3-דימתיל-בנזנמיניום (14) (1.3 גרם, 6.4 ממול) ו-2-(2-ברומו-4-כלורופניל) חומצה אצטית (15) (1.6 גרם, 6.4 ממול) ב-DMF (6 מ"ל) בטמפרטורת החדר, הוספנו לאחר מכן אבקת Cu (0.05 גרם), Cu2O (0.05 גרם) ו-K2CO3 (0.71 גרם, 5.1 ממול). תערובת התגובה חוממת ל-110 מעלות צלזיוס למשך 12 שעות. לאחר הסרת הממסים תחת ואקום, השארית הומסה בתמיסת 1 N NaOH (25 מ"ל). התוצר הגולמי הושג על ידי משקעים עם החמצה של התסנין עם קונצרן. HCl. לאחר הייבוש, התוצר הגולמי הוסף לריאגנט של Eaton (5 מ"ל) בטמפרטורת החדר, ואז התערובת חוממה ל-90 מעלות צלזיוס למשך שעה אחת. תערובת התגובה המקוררת הושלכה לתמיסת NaHCO3 מימית רוויה. המשקע סונן כדי לאסוף את המוצר הגס. טיהור של השאריות על ידי כרומטוגרפיה של עמודת סיליקה ג'ל סיפק 25, מוצק צהוב (0.80 גרם, 38.6% תשואה). 1H NMR (400 MHz, DMSO-D6) δ 8.17 (d, J =8.1, 1.5 Hz, 1H), 7.86 (d, J=6.9 Hz, 1H), 7.51 (s, 1H), 3.84 (s, 3H), 3.78 (s, 2H), 2.49 (s, 3H), 2.27 (s, 3H); HRMS (ESI) m/z [M+H]+ מחושב עבור C18H14ClNO3: 327.7640 נמצא: 328.0734. 4-כלורו-8-מתוקסי-9,10-דימתיל-6H-פירולו[3,2,1-דה]אקרידין-1 ,6(2H)-dion (26): הסינתזה של תרכובת זו הייתה דומה ל-25. 15 הוחלף ב-2-(2-ברומו-5-כלורופניל) חומצה אצטית (16). קיבלנו 0.82 גרם 26 כמוצק צהוב חיוור עם תשואה של 38.7%. 1H NMR (400 מגה-הרץ, DMSO-D6) δ 7.73 (s, 1H), 7.52 (s, 1H), 7.38 (s, 1H), 3.71 (s, 3H), 3.64 (s,2H), 2.36 (s, 3H), 2.13 (s, 3H); HRMS (ESI) m/z [M+H]+ מחושב עבור C18H14ClNO3: 327.7640 נמצא: 328.0734.
{{0}}פלואורו-8-מתוקסי-9,10-דימתיל-6H-פירולו[3,2,1-דה]אקרידין{ {9}},6(2H)-dion (27): הסינתזה של תרכובת זו הייתה דומה ל-25. 15 הוחלף ב-2-(2-ברומו-4-פלואורופניל) חומצה אצטית (17). השגנו מוצק צהוב עמוק 27 עם 0.84 גרם (42.1% תשואה). 1H NMR (400 MHz, DMSO-D6) δ 8.21 (d, J=8.0 Hz, 1H), 7.68 (s, 1H), 7.23 (d, J {{39} }.5 הרץ, 1H), 3.88 (s, 3H), 3.81 (s, 2H), 2.53 (s, 3H), 2.30 (s, 3H); HRMS (ESI) m/z [M+H]+ מחושב עבור C18H14FNO3: 311.3124 נמצא: 312.1030. 4-פלואורו-8-מתוקסי-9,10-דימתיל-6H-פירולו[3,2,1-דה]אקרידין-1 ,6(2H)-dion (28): הסינתזה של תרכובת זו הייתה דומה ל-25. 15 הוחלף ב-2-(2-ברומו-5-פלואורופניל) חומצה אצטית (18). התקבל 0.81 גרם מוצק צהוב עמוק (תשואה של 40.5%). 1H NMR (400 מגה-הרץ, DMSOD6) δ 7.86 (s, 1H), 7.64 (s, 1H), 7.51 (s, 1H), 3.83 (s, 3H), 3.77 (s, 2H), 2.49 (s, 3H), 2.26 (s, 3H); HRMS (ESI) m/z [M+H]+ מחושב עבור C18H14FNO3: 311.3124 נמצא: 312.1030.
4,8-דימתוקסי-9,10-דימתיל-6H-פירולו[3,2,1-דה]אקרידין-1,6(2H )-דיון (29): הסינתזה של תרכובת זו הייתה דומה ל-25. 15 הוחלף ב-2-(2-bromo-5-methoxyphenyl)חומצה אצטית (19). {{20}}.73 גרם מוצק צהוב סופק עם תשואה של 35.2%. 1H NMR (400 MHz, DMSO D6) δ 7.93 (s, 1H), 7.61 (s, 1H), 7.47 (s, 1H), 3.84 (s, 3H), 3.81 ( s, 3H), 3.67 (s, 2H), 2.44 (s, 3H), 2.28 (s, 3H); HRMS (ESI) m/z [M+H]+ מחושב עבור C19H17NO4: 323.3480 נמצא: 324.1230. 7-מתוקסי-5,6-דימתיל-9-אוקסו-9,10-דיהידרואקרידין-4-חומצה קרבוקסילית (33): לפתרון של 6-קרבוקסי-4-מתוקסי-2,3-דימתיל-בנזנמיניום (14) (1.30 גרם, 6.4 ממול) ו-2-חומצה ברום-בנזואית (7) (1.29 גרם, 6.4 מילימול) ב-DMF (6 מ"ל) בטמפרטורת החדר, הוספנו לאחר מכן אבקת Cu (0.05 גרם), Cu2O (0.05 גרם) ו-K2CO3 (0.71 גרם, 5.1 ממול). תערובת התגובה חוממת ל-110 מעלות צלזיוס למשך 12 שעות. לאחר הסרת הממסים תחת ואקום, השארית הומסה בתמיסת 1 N NaOH (25 מ"ל). התוצר הגולמי הושג על ידי משקעים עם החמצה של התסנין עם קונצרן. HCl. לאחר הייבוש, התוצר הגולמי הוסף לריאגנט של Eaton (5 מ"ל) בטמפרטורת החדר, ואז התערובת חוממה ל-90 מעלות צלזיוס למשך שעה אחת. תערובת התגובה המקוררת הושלכה לתמיסת NaHCO3 מימית רוויה. המשקע סונן כדי לאסוף את המוצר הגס. טיהור של השאריות על ידי כרומטוגרפיה של עמודת סיליקה ג'ל סיפק 33, מוצק צהוב חיוור (1.00 גרם, 52.7% תשואה). 1H NMR (400 MHz, DMSO-D6) δ 13.00 (s, 1H), 10.28 (s, 1H), 8.01 (d, J=9.7 Hz, 1H), 7.69 (d , J=8.5 הרץ, 1H), 7.48 (t, J=9.0 הרץ, 1H), 7.34 (s, 1H), 3.67 (s, 3H), 2.32 (s, 3H ), 2.10 (s, 3H); HRMS (ESI) m/z [M+H]+ מחושב עבור C17H15NO4: 297.3100 נמצא: 298.1073. 2,7-דימתוקסי-5,6-דימתיל-9-אוקסו-9,10-דיהידרואקרידין-4-חומצה קרבוקסילית (34): סינתזה של תרכובת זו הייתה דומה ל-33. ה-7 הוחלף ב-2-ברומו-5- חומצה מתוקסיבנזואית (30). המוצק הצהוב נתן 1.05 גרם עם תשואה של 50.2%. 1H NMR (400 מגה-הרץ, DMSO-D6) δ 12.96 (s, 1H), 10.45 (s, 1H), 7.84 (s, 1H), 7.54 (s, 1H), 7.50 (s, 1H), 3.84 (s, 3H), 3.81 (s, 3H), 2.48 (s, 3H), 2.27 (s, 3H); HRMS (ESI) m/z [M+H]+ מחושב עבור C18H17NO5: 327.3360 נמצא: 328.1179.
4.2. בדיקה ביולוגית
ערכות קשירה STING לעכבר, ערכות קשירה STING WT אנושית, ערכות קשירה אנושית AQ STING וערכות קשירה אנושית H232 STING נרכשו מ-Cisbio. תאי 293T mSTING (ISG/KI-IFNb), תאי 293T hSTING-R232 (ISG/KI-IFNb), תאי THP1-KI-hSTING-R232, תאי THP1-KO-STING נרכשו מ אינובוגן. תאי 293T mSTING ו-293T hSTING-R232 תורבו באמצעות DMEM (Gibco, Waltham, MA, ארה"ב), 2 מ"מ L-גלוטמין (Sigma-Aldrich, St. Louis, MO, ארה"ב), 4.5 גרם/ליטר גלוקוז (Sigma- Aldrich), 10% FBS (Gibco), Pen-Strep (100 U/mL-100 µM) (Gibco), 100 µM normocin (Invivogen, סן דייגו, קליפורניה, ארה"ב), ובתוספת אנטיביוטיקה סלקטיבית (Invivogen ) בלסטיצידין (10 מיקרומטר), היגרומיצין (100 מיקרומטר) וזאוצין (100 מיקרומטר). תאי THP1-KO-STING ותאי THP1-KI-hSTING-R232 תורבו באמצעות RPMI-1640 (Gibco), 2 מ"ל L-גלוטמין (Sigma-Aldrich), 25 מ"מ HEPES (Sigma-Aldrich), FBS 10% מושבתת חום (Gibco), PenStrep (100 U/mL-100 µM) (Gibco), 100 µM normocin (Invivogen), ובתוספת אנטיביוטיקה סלקטיבית (Invivogen) blasticidin ( 10 µM) וזאוצין (100 µM). הפתרון QUANTI-Blue, QUANTI-Luc, 20,30 -cGAMP נרכשו מ-Invivogen. H151 הושג מ-Beijing Innochem Science and Technology Co., Ltd. (בייג'ינג, סין). ערכת בדיקת כדאיות תאים זוהרת CellTiter-Glo התקבלה מ-Promega.
4.2.1. HTRF STING Binding Competitive Assay
בהתאם להוראות של ערכות הקישור של STING, הפתרונות הבאים נוספו ברציפות לכל באר בצלחת 384-הבאר: 5 µL של תרכובות הזיהוי או 2 0,30 -cGAMP (בקרה חיובית ) עם ריכוזים שונים או מדלל (שליטה שלילית); 5 μL חלבון אנושי מתויג STING 6His (באר בקרה שלילית נוספה למאגר הזיהוי); 10 µL של ליגנד STING d2 ו-Anti 6His-Tb3+ תמיסת עבודה מעורבת מראש. לאחר איטום הצלחת ודגירה בטמפרטורת החדר למשך 3 שעות, נקראו ערכי הקרינה ב-665 ננומטר ו-620 ננומטר. היחס בין שתי עוצמות הקרינה (665 ננומטר/620 ננומטר) שימש להערכת עוצמת הקישור של תרכובות. ערכי ה-IC50 (50% ריכוז מעכב) חושבו באמצעות התוכנה GraphPad Prism.
4.2.2. בדיקת תאי להקרנה של תרכובות לפעילות האגוניסטית
כמויות של 180 µL של תאי mSTING 293T, תאי 293T hSTING-R232 ותליית תאי THP1-KOSTING הופצו ב96-צלחות עם תחתית שטוחה היטב עם צפיפות של ~50,000 תאים /well (293T) או ~100,000 תאים/באר (THP1). נוספה כמות של 20 μL של תמיסת מלח או תמיסת מלח של תרכובת בדיקה, או 20,30 -cGAMP כהתייחסות חיובית, והתאים הודגרו ב-37 ◦C עם 5% CO2 למשך 48 שעות. לאחר מכן, כמות של 20 µL של supernatant נוספה לתוך צלחת 96-באר עם תחתית שטוחה, ואחריה 180 µL של תמיסה QUANTI-Blue לכל באר. הצלחת הודגרה ב-37 מעלות צלזיוס למשך 3 שעות, ורמות SEAP (פעילות מסלול ה-IRF) נקבעו באמצעות ספקטרופוטומטר ב-620-655 ננומטר.
4.2.3. בדיקת תאי לבדיקת תרכובות לפעילות מעכבת
ניסוי מקדים: 180 µL של תאי mSTING 293T, תאי 293T hSTING-R232 (~50,000 תאים/באר) עוררו במשך 48 שעות ב-37 ◦C ב- חממת CO2 5% עם 10 µL 20,30 -cGAMP (3.125 µM, 6.25 µM) ו-10 µL H151 (1.0 µM ). לאחר מכן, כמות של 20 µL של supernatant נוספה לתוך צלחת 96-בתחתית שטוחה, ואחריה 180 µL של תמיסה QUANTI-Blue לכל באר. הצלחת הודגרה ב-37 מעלות צלזיוס למשך 3 שעות, ורמות SEAP (פעילות מסלול ה-IRF) נקבעו באמצעות ספקטרופוטומטר ב-620-655 ננומטר. 180 µL של תאי 293T mSTING, תרחיף 293T hSTING-R232 הופצו ב96-צלחות בעלות תחתית שטוחה עם צפיפות של ~50,000 תאים/באר. כמות של 10 µL 2 0,30 -cGAMP (3.125 µM) ותרכובת 11 או תרכובת 27 (0.78 µM, 1.56 µM, 3.13 µM, 6.25 µM, 12.5 µM, 5µM, 5µM, 5µM, µM) או H151 (0.08 µM, 0.16 µM, 0.31 µM, 0.63 µM, 1.25 µM, 2.5 µM, 5 µM) נוספו, והתאים הודגרו ב-37 ◦C CO2 עם 58% CO2. לאחר מכן, כמות של 20 µL של supernatant נוספה לתוך צלחת 96-בתחתית שטוחה, ואחריה 180 µL של תמיסה QUANTI-Blue לכל באר. הצלחת הודגרה ב-37 מעלות צלזיוס למשך 3 שעות, ורמות SEAP (פעילות מסלול ה-IRF) נקבעו באמצעות ספקטרופוטומטר ב-620-655 ננומטר. ערכי IC50 חושבו על ידי תוכנת GraphPad.
4.2.4. מבחן סלולרי לעיכוב של מסלולים כפולים STING
180 µL של תרחיף תאי THP1-KI-hSTING-R232 הופצו ב96-צלחות שטוחות היטב עם צפיפות של ~100,000 תאים/באר. נוספה כמות של 10 µL 20,30 -cGAMP ו-10 µL תרכובת 11 (20 µM) או תרכובת 27 (33 µM) או H151 (2 µM), והתאים הודגרו ב-37 ◦C עם 5% CO2 למשך 24 שעות. לאחר מכן, הוספה כמות של סופרנטנט לצלחת 96-לבנה (אטומה), ולאחריה תמיסת QUANTI-Luc או QUANTI-Blue לכל באר, ורמות הארה או רמות SEAP נקראו בהתאם להוראות היצרן. זה מאפשר מחקר סימולטני של מסלול ה-IFN regulatory factor (IRF), על ידי הערכת הפעילות של Lucia luciferase ומסלול NF-κB, על ידי ניטור הפעילות של SEAP.
4.2.5. Assay CellTiter-Glo Luminescent Cell Viability Cell
כדאיות התא נמדדה על ידי ערכת בדיקת כדאיות תאים זוהרת CellTiter-Glo לפי הוראות היצרן. בקצרה, תאים הודגרו עם שלושה ריכוזים שונים (5 מיקרומטר, 10 מיקרומטר, 100 מיקרומטר) של תרכובת 11 תרכובת 27, או H-151 למשך 48 שעות. ריאגנט CellTiter-Glo של 100 μL נוספה לצלחת 96-לבדיקת באר למשך 10 דקות, ולאחר מכן תועדה זוהר.
4.3. עגינה מולקולרית של תרכובת 11
המבנה הגבישי של קומפלקס STING (PDB ID: 6MXE) נלקח מהערך של Protein Data Bank ושימש כנקודת ההתחלה. חלבון הוכן באמצעות הכנת חלבון של Maestro ופוצל לשרשרת A ושרשרת B. יצרנו אתר קישור ב-LBD של מונומר STING המבוסס על הליגנד המקורי (Merck-18) באמצעות Receptor Grid Generation. השתמשנו בדיוק ה-SP של גלייד עגינה עבור חלק העגינה המולקולרית, מה שאפשר לתרכובת 11 ליצור לכל היותר 20 תנוחות. בסופו של דבר הפקנו 16 קונפורמציות קשורות (כולם בכיס התחתון) ובדקנו את האנרגיה החופשית של הקומפלקסים באמצעות מודול Prime MM-GBSA בתוכנה של שרדינגר. יתר על כן, בהתבסס על ציון העגינה, ציון מודל הגלישה וציון MMGBSA dG Bind, בחרנו את המבנה האופטימלי שקיבל ציון ראשון בשני ודורג שלישי באחד (נראה בטבלה S2). לבסוף, מיזגנו את הקונפורמציות הטובות ביותר של שרשראות A ו-B כדי להשיג את מבנה העגינה השלם.
הפניות
1. אייב, ט.; חרשימה, א; שיה, ט.; קונו, ה.; קונו, ק.; מוראלס, א.; אהן, ג'; גוטמן, ד.; ברבר, GN STING זיהוי של DNA ציטופלזמי מעורר הגנה סלולרית. מול. תא 2013, 50, 5–15. [CrossRef]
2. Wu, J.; שמש, ל. חן, X.; דו, פ.; שי, ח; חן, ג; Chen, ZJ Cyclic GMP-AMP הוא שליח שני אנדוגני באיתות חיסוני מולד על ידי DNA ציטוזולי. מדע 2013, 339, 826–830. [CrossRef]
3. אייב, ט.; Barber, GN Cytosolic-DNA-Mediated, STING-Dependent Gene Proinflammatory Induction מחייב הפעלה קנונית של NF-κB באמצעות TBK1. J. Virol. 2014, 88, 5328–5341. [CrossRef]
4. Cai, X.; Chiu, Y.-H.; Chen, ZJ מסלול ה-cGAS-cGAMP-STING של חישה ואיתות DNA ציטוסוליים. מול. תא 2014, 54, 289–296. [CrossRef] [PubMed]
5. גאו, ד.; לי, ט.; לי, X.-D.; חן, X.; לי, ק.-ז.; וייט-קרטר, מ.; Chen, ZJ הפעלה של סינתאז GMP-AMP מחזורי על ידי DNA עצמי גורמת למחלות אוטואימוניות. פרוק. נאטל. Acad. Sci. ארה"ב 2015, 112, E5699–E5705. [CrossRef] [PubMed]
6. לי, טי ג'יי; צ'נג, ה.; יואן, ה.; שו, QM; שו, ג; Zhang, YF; שו, פ.; טאן, ג'; רואי, י.; Li, PJSR פעילות אנטי-גידולית של cGAMP באמצעות גירוי של תגובה חיסונית מולדת בתיווך cGAS-cGAMP-STING-IRF3. Sci. נציג 2016, 6, 19049. [CrossRef] [PubMed]
7. מוטואני, מ.; פסירידיס, ש.; פיצג'רלד, KA חישת DNA על ידי מסלול cGAS-STING בבריאות ומחלות. נאט. הכומר ג'נט. 2019, 20, 657–674. [CrossRef]
8. ג'אנג, ה.; אתה, QD; Xu, XL ממריץ מיקוד של גנים אינטרפרון (STING): פרספקטיבה של כימיה רפואית. J. Med. Chem. 2020, 63, 3785–3816. [CrossRef]
9. גאו, ג'; טאו, ג'; ליאנג, ו.; זאו, מ.; דו, X.; Cui, S.; דואן, ה.; קאן, ב.; סו, X.; Jiang, Z. זיהוי ואפיון של פוספודיאסטראזים המפירים באופן ספציפי 30 3 0 -GMP-AMP מחזורי. Cell Res. 2015, 25, 539–550. [CrossRef] [PubMed]
10. Corrales, L.; McWhirter, SM; דובנסקי, TW; Gajewski, TF מסלול STING המארח בממשק של סרטן וחסינות. ג'יי קלין. תחקור. 2016, 126, 2404–2411. [CrossRef] [PubMed]
11. באגולי, לפני הספירה; Ching, LM DMXAA: חומר אנטי-וסקולרי עם מספר תגובות מארח. Int. ג'יי רדיאט. אונקול. ביול. פיזי. 2002, 54, 1503–1511. [CrossRef]
12. לארה, PN; דוילארד, J.-Y.; Nakagawa, K.; פון פאבל, י. McKeage, MJ; אלברט, I.; Losonczy, G.; רק, מ.; היו, ד.-ס.; מניפה, X.; et al. ניסוי אקראי שלב III מבוקר פלצבו של Carboplatin ו-Paclitaxel עם או בלי הגורם משבש כלי הדם Vadimezan (ASA404) בסרטן ריאות מתקדם לא-לא-קטן. ג'יי קלין. אונקול. 2011, 29, 2965–2971. [CrossRef]
13. Conlon, J.; Burdette, DL; שארמה, ש; בהט, נ.; תומפסון, מ.; ג'יאנג, ז'; Rathinam, VAK; נזירים, ב.; ג'ין, ט.; Xiao, TS; et al. עכבר, אך לא STING אנושי, קושרים ואותות בתגובה לחומר משבש כלי הדם 5,6-Dimethylxanthenone-4-Acetic Acid. J. Immunol. 2013, 190, 5216–5225. [CrossRef] [PubMed]
14. קים, ש.; לי, ל.; מאליגה, ז; יין, ש; וו, ה.; Mitchison, TJ פלבנואידים אנטי סרטניים הם אגוניסטים של STING סלקטיביים לעכברים. ACS Chem. ביול. 2013, 8, 1396–1401. [CrossRef] [PubMed]
15. קאבלר, ט.; דיימלינג, ט.; אבלסר, א.; הופנר, ק.-פ.; Hornung, V. זיהוי ספציפי למין של תרכובת מולקולה קטנה אנטי-ויראלית CMA על ידי STING. EMBO J. 2013, 32, 1440–1450. [CrossRef]
16. Ramanjulu, JM; Pesiridis, GS; יאנג, ג'; קונצ'ה, נ.; סינגהאוס, ר.; ג'אנג, ש.-י.; טראן, י.-ל.; מור, פ.; להמן, ש.; Eberl, HC; et al. עיצוב אגוניסטים לקולטן STING של אמידו בנזימידאזול עם פעילות מערכתית. טבע 2018, 564, 439–443. [CrossRef] [PubMed]
17. סנטר, EN; יו, ג; Vartabedian, VF; ג'יה, י.; קומאר, מ.; גאמו, AM; Vernier, W.; עלי, ש; קיסאי, מ.; לזר, DC; et al. פעילות אנטי-גידולית של חיקוי cGAMP סיסטמי המפעיל STING שאינו נוקלאוטיד. מדע 2020, 369, 993–999.
18. פאן, ב"ש; Perera, SA; Piesvaux, JA; Presland, JP; שרדר, GK; קאמינג, JN; Trotter, BW; אלטמן, ד"ר; Buevich, AV; מזומן, ב.; et al. אגוניסט STING שאינו נוקלאוטיד זמין דרך הפה עם פעילות אנטי-גידולית. Science 2020, 369, eaba6098. [CrossRef] [PubMed]
19. סאלי, TM; Pryke, KM; ג'ינו, א.; אנדרו, ל.; איריס, א.; רבקה, ב.; Staverosky, JA; Smith, JL; אחמד, א.ס.; Lisi, AJPP אפיון של אגוניסט STING חדשני ספציפי לאדם המעורר פעילות אנטי-ויראלית נגד נגיפי אלפא מתעוררים. PloS Pathog. 2015, 11, e1005324. [CrossRef] [PubMed]
20. הונג, ז; מיי, ג'; לי, ג; באי, ג.; מיימיטי, מ.; הא.; יו, ו.; שמש, ל. ג'אנג, ל.; צ'נג, ד'; et al. מעכבי STING מכוונים לכיס הקישור המחזורי של הדינוקלאוטידים. פרוק. נאטל. Acad. Sci. ארה"ב 2021, 118, e2105465118. [CrossRef] [PubMed]
21. Siu, T.; אלטמן, ד"ר; Baltus, GA; צ'ילדרס, מ.; אליס, JM; Gunaydin, H.; האץ', ח; הו, ט.; Jewell, J.; לייסי, ב.מ.; et al. גילוי של ליגנד תחרותי חדש של cGAMP מהצורה הלא פעילה של STING. ACS Med. Chem. Lett. 2019, 10, 92–97. [CrossRef] [PubMed]
22. האג, SM; גולן, MF; ריימונד, ל.; גיבלין, א.; אברמי, ל. דקווט, א.; היימן, מ.; ואן דר גוט, FG; טורקאטי, ג'; בהרנדט, ר.; et al. מיקוד STING עם מעכבי מולקולות קטנות קוולנטיות. טבע 2018, 559, 269–273. [CrossRef]
23. הו, ש; לאן, X.-J.; לי, ו.; יאן, X.-L.; Chang, J.-J.; יאנג, X.-H.; Sun, W.; Xiao, J.-H.; Li, S. עיצוב, סינתזה והערכה ביולוגית של אנלוגים לאקרידון כאגוניסטים חדשים לקולטן STING. ביוורג. Chem. 2020, 95, 103556. [CrossRef] [PubMed]
24. Ouyang, S.; שיר, X.; וואנג, י.; רו, ה.; שו, נ.; ג'יאנג, י.; ניו, פ.; ז'ו, י.; Qiu, W.; פרוואטיאר, ק.; et al. ניתוח מבני של חלבון מתאם STING חושף ממשק דימר הידרופובי ומצב של כריכת di-GMP מחזורית. חסינות 2012, 36, 1073–1086. [CrossRef] [PubMed]
25. שו, ג; יי, ג.; ווטס, ט.; קאו, CC; Li, P. מבנה STING הקשור ל-di-GMP מחזורי חושף את המנגנון של זיהוי דינוקלאוטידים מחזוריים על ידי מערכת החיסון. נאט. מבנה. מול. ביול. 2012, 19, 722–724. [CrossRef]
26. Huang, Y.-H.; ליו, X.-Y.; דו, X.-X.; Jiang, Z.-F.; סו, X.-D. הבסיס המבני לחישה וקשירה של di-GMP מחזורית על ידי STING. נאט. מבנה. מול. ביול. 2012, 19, 728–730. [CrossRef]
27. שי, א"י; דאם-גנמט, ק"ל; Mirzadegan, T. הבדלים מבניים דינמיים בין STING של אדם ועכבר מובילים לרגישות שונה ל-DMXAA. ביופיס. י' 2018, 114, 32–39. [CrossRef]
28. גאו, פ.; אסכנו, מ.; זילינגר, ט.; וואנג, ו.; דאי, פ.; סרגנוב, א.א.; גפני, BL; שומאן, ש; ג'ונס, ר"א; דנג, ל.; et al. ניתוח מבנה-פונקציה של הפעלת STING על ידי c[G(20,50 )pA(30,50 )p] ומיקוד על ידי DMXAA אנטי ויראלי. תא 2013, 154, 748–762. [CrossRef] [PubMed]
29. ג'אנג, סי; שאנג, ג.; Gui, X.; ג'אנג, X.; באי, X.; Chen, ZJN בסיס מבני של קשירת STING עם וזרחון על ידי TBK1. טבע 2019, 567, 394–398. [CrossRef]
30. Vavˇrina, Z.; גוטן, או.; סמולה, מ.; Zavˇrel, M.; אליאקבר טהרני, ז; Charvát, V.; קוז'יסק, מ.; בורה, ע.; בירקוש, ג.; Rulíšek, L. אינטראקציות חלבון-ליגנד באתר הקישור של STING שנבדקו על ידי מוטציות נקודתיות מעוצבות רציונליות: ניסוי ותיאוריה. ביוכימיה 2021, 60, 607–620. [CrossRef] [PubMed]
31. צ'ה, X.; דו, X.-X.; קאי, X.; ג'אנג, ג'; Xie, WJ; ארוך, ז"ר; יא, ז'-י'; ג'אנג, ה.; יאנג, ל.; סו, X.-D.; et al. מוטציות בודדות מעצבות מחדש את רשת המתאם המבנית של קומפלקס DMXAA-Human STING. J. Phys. Chem. B 2017, 121, 2073–2082. [CrossRef] [PubMed]
32. דינר, EJ; Burdette, DL; וילסון, SC; מונרו, קמ; קלנברגר, קליפורניה; Hyodo, M.; הייאקווה, י.; האמונד, MC; Vance, RE חיישן ה-DNA החיסוני המולד cGAS מייצר דינוקלאוטיד מחזורי לא קנוני המפעיל STING אנושי. נציג תא 2013, 3, 1355–1361. [CrossRef] [PubMed]
33. גאו, פ.; זילינגר, ט.; וואנג, ו.; אסכנו, מ.; דאי, פ.; הרטמן, ג.; טושל, ט.; דנג, ל.; ברכט, ו.; תחליפי פאטל, דיג'יי כריכה בכיס ומכסה באזור הופכים את ה-STING האנושי לרגיש לתרופה הספציפית למין DMXAA. נציג תא 2014, 8, 1668–1676. [CrossRef] [PubMed]
34. Hwang, J.; קאנג, ט.; לי, ג'; צ'וי, ב'-ש'; Han, S. עיצוב, סינתזה והערכה ביולוגית של נגזרות DMXAA מתפקדות ב-C7-כאגוניסטים פוטנציאליים ל-STING. Org. ביומול. Chem. 2019, 17, 1869–1874. [CrossRef] [PubMed]
