מעבר אקטיבי של שלב זיכרון הפחד מגיבוש מחדש להכחדה באמצעות מניעת קונסולידציה בתיווך ERK
Mar 19, 2022
איש קשר: Audrey Hu Whatsapp/hp: 0086 13880143964 דוא"ל:audrey.hu@wecistanche.com
השליפה שלפַּחַדזיכרוןגורם לשני תהליכי זיכרון הפוכים, כלומר, איחוד מחדש והכחדה. שליפה קצרה גורמת לגיבוש מחדש כדי לשמור או לשפר את הפחדזיכרון, בעוד שליפה ממושכת מכבה את הזיכרון הזה. למרות שהמנגנונים של איחוד מחדש והכחדה נחקרו, עדיין לא ידוע כיצד שלבי זיכרון הפחד עוברים מאיחוד מחדש להכחדה במהלך אחזור הזיכרון. כאן, אנו מראים שתהליך מעבר זיכרון תלוי קינאז חוץ-תאי (ERK) לאחר אחזור מווסת את המעבר של שלבי זיכרון מאיחוד מחדש להכחדה על ידי מניעת השראת איחוד מחדש במשימת הימנעות מעכבת (IA) בעכברים זכרים. ראשית, שלב זיכרון המעבר, המבטל את השראת הגיבוש מחדש, אך אינו מספיק לרכישת הכחדה, זוהה לאחר קונסולידציה מחדש, אך לפני שלבי הכחדה. שנית, שלבי הגיבוש מחדש, המעבר וההכחדה לאחר מכןאחזור זיכרוןהראו חתימות מולקולריות ותאיות מובהקות באמצעות חלבון קשירת אלמנטים מגיב ל-CAMP (CREB) וזרחון ERK באמיגדלה, בהיפוקמפוס ובקליפת המוח הקדם-מצחית (mPFC). שלב הגיבוש מחדש הראה זרחון מוגבר של CREB, בעוד ששלב ההכחדה הציג מספר אוכלוסיות עצביות עם שילובים שונים של זרחון CREB ו/או ERK, באזורי מוח אלו. מעניין לציין ששלושת שלבי הזיכרון, כולל שלב המעבר, הראו הפעלת ERK חולפת מיד לאחר השליפה. והכי חשוב, החסימה של ERK באמיגדלה, בהיפוקמפוס או ב-mPFC בשלב זיכרון המעבר ביטלה חיזוק שנגרם מקונסולידציה מחדש של זיכרון IA. תצפיות אלו מצביעות על כך שמסלול האותות ERK מווסת באופן פעיל את המעבר של שלב הזיכרון מגיבוש מחדש להכחדה ותהליך זה מתפקד כמתג המבטל גיבוש מחדש של פחדזיכרון.
מילות מפתח: ERK; הַכחָדָה; זיכרון פחד; איחוד מחדש; מַעֲבָר
1המחלקה למדעי הביולוגי, הפקולטה למדעי החיים, אוניברסיטת טוקיו לחקלאות, טוקיו 156-8502, יפן, ו
2בית הספר לתואר שני לחקלאות ומדעי החיים, אוניברסיטת טוקיו, טוקיו 113-8657, יפן
הצהרת משמעות
שליפה של זיכרון פחדגורם לשני תהליכי זיכרון הפוכים; איחוד מחדש והכחדה. איחוד מחדש שומר/משפרזיכרון פחד, בעוד הכחדה מחלישה את זיכרון הפחד. עדיין לא ידוע כיצד שלבי זיכרון עוברים מאיחוד מחדש להכחדה במהלך השליפה. כאן, זיהינו תהליך מעבר זיכרון פעיל המתפקד כמתג המעכב איחוד מחדש. שלב מעבר זיכרון זה הראה עלייה חולפת של זרחון קינאז חוץ-תאי (ERK) באמיגדלה, בהיפוקמפוס ובקליפת המוח הקדם-פרונטלית המדיאלית (mPFC). באופן מעניין, עיכוב של ERK באזורים אלה בשלב המעבר ביטלה את השיפור בתיווך מחדש של זיכרון הימנעות מעכבת (IA). ממצאים אלו מצביעים על כך שתהליך זיכרון המעבר מווסת באופן פעיל את המעבר של שלבי זיכרון הפחד של זיכרון הפחד על ידי מניעת השראת קונסולידציה מחדש באמצעות הפעלת מסלול האותות ERK.
מבוא
זיכרוןאחזור אינו תהליך פסיבי אלא הוא תהליך דינמי המאפשר תחזוקה, חיזוק, החלשה או שינוי/עדכון של זיכרון מקורי (Misanin et al., 1968; Schneider and Sherman, 1968; Lewis, 1979; Mactutus et al. ., 1979; Gordon, 1981; Nader et al., 2000; Nader and Hardt, 2009; Dudai, 2012; Fukushima et al., 2014). חשוב לציין, זיכרון פחד מותנה שאוחזר על ידי חשיפה חוזרת קצרה לגירוי המותנה (CS) הופך לאבילי ודורש איחוד מחדש תלוי ביטוי גנים לצורך תחזוקתו או שיפורו (Nader et al., 2000; Dudai, 2002; Kida et al., 2002; Suzuki et al., 2004; Tronel et al., 2005; Fukushima et al., 2014). לעומת זאת, חשיפה חוזרת מתמשכת או חוזרת ל-CS גורמת להכחדת זיכרון, אשר מחלישה את זיכרון הפחד (Pavlov, 1927; Rescorla, 2001; Myers and Davis, 2002). לפיכך, שליפת זיכרון הפחד גורמת לשני תהליכי זיכרון הפוכים, כלומר, איחוד מחדש והכחדה, למרות ששני התהליכים נגרמים על ידי חשיפה מחדש ל-CS זהה, אך שונים בהתאם למשך החשיפה מחדש ל-CS.
המאפיין הביוכימי המשותף והקריטי של איחוד מחדש והכחדה הוא הדרישה לביטוי גנים המתווך ל-cAMP-element-binder חלבון (CREB) (Mamiya et al., 2009). באופן מעניין, הראינו חתימות מולקולריות, אנטומיות והתנהגותיות מנוגדות בין שלבי הגיבוש מחדש וההכחדה של זיכרון פחד הקשרי (Suzuki et al., 2004; Mamiya et al., 2009). חסימת סינתזת חלבון במהלך שלב הגיבוש מחדש משבשת את הפחד המקוריזיכרון, בעוד שחסימת סינתזת חלבון במהלך שלב ההכחדה לא מצליחה לעשות זאת, למרות שזיכרון הפחד ההקשרי הופעל מחדש. הדרישה של אזורי מוח המציגים את ההפעלה של ביטוי גנים בתיווך CREB שונה בין איחוד מחדש והכחדה; קונסולידציה מחדש תלויה באמיגדלה ובהיפוקמפוס, בעוד שההכחדה מסתמכת על האמיגדלה וקליפת המוח הקדם-מצחית (mPFC). עם זאת, מהלך הזמן של הפעלת CREB של אמיגדלואיד שונה בין שלבי הגיבוש מחדש וההכחדה. תצפיות אלו העלו כי שלבי הגיבוש מחדש וההכחדה אינם עצמאיים, אלא מקיימים אינטראקציה זה עם זה. מעניין לציין שמחקרים עדכניים זיהו חלון זמן (שלב המעבר) שלא מראה הפעלה של קינאז חוץ-תאי (ERK) באמיגדלה לאחר קונסולידציה מחדש, אלא לפני שלבי ההכחדה לאחר שליפת זיכרון פחד שמיעתי (Merlo et al., 2018) ). ביחד, ממצאים אלה מציעים את המנגנונים האפשריים שבאמצעותם שלבי זיכרון עוברים מגיבוש מחדש להכחדה במהלך שליפת זיכרון הפחד. במילים אחרות, ייתכן שתהליך מעבר הזיכרון מווסת באופן פעיל את המתג הזה.
במשימת הימנעות מעכבת (IA), עכברים מקבלים הלם רגל חשמלי לאחר שהם נכנסים לתא חשוך מתא בהיר ויוצריםזיכרוןכדי להימנע מהתא האפל. בעבר, על ידי שימוש במשימה זו, הראינו שניתן להבחין בשלבי הגיבוש מחדש וההכחדה בנקודת הזמן שבה עכבר נכנס לתא חשוך מתא בהיר במהלך פגישת חשיפה חוזרת (Fukushima et al., 2014). לכן, משימה זו מאפשרת לנו לאפיין את החתימות המולקולריות הפרספקטיביות של שלבי הקונסולידציה וההכחדה, בניגוד לפרדיגמת התניית הפחד ההקשרית הקלאסית שבה ההפעלה מחדש של זיכרון פחד מותנה על ידי חשיפה מחדש ל-CS יוזמת הן קונסולידציה והכחדה; חשיפה חוזרת קצרה (3 דקות) להקשר המותנה גורמת לגיבוש מחדש, בעוד שחשיפה ארוכה (30 דקות) או חוזרת להקשר זה גורמת להכחדה (Eisenberg et al., 2003; Pedreira and Maldonado, 2003; Suzuki et al., 2004; Lee et al., 2008; Mamiya et al., 2009). יתר על כן, מצאנו שזיכרון ה-IA שאוחזר מוגבר באמצעות איחוד זיכרון מחדש במשימה זו (Fukushima et al., 2014).
להבין את מנגנון המעבר מגיבוש מחדש להכחדה במהלך שליפה של פחדזיכרון, שאפנו לזהות ולאפיין את החתימות המולקולריות, הסלולריות וההתנהגותיות של שלבי הגיבוש מחדש, המעבר וההכחדה של זיכרון IA. ניתחנו את ההפעלה של CREB ו-ERK באמיגדלה, בהיפוקמפוס וב-mPFC בשלבי הגיבוש מחדש, המעבר וההכחדה ובחנו את התפקידים של הפעלת ERK בתהליכי זיכרון אלו.

חומרים ושיטות
עכברים כל הניסויים נערכו על פי המדריך לטיפול ושימוש בחיות מעבדה (אגודה למדעי המוח של יפן ואוניברסיטת טוקיו לחקלאות). כל הניסויים בבעלי חיים שבוצעו במחקר זה אושרו על ידי ועדת הטיפול והשימוש בבעלי חיים של אוניברסיטת טוקיו לחקלאות (אישור מס' 280037). כל ההליכים הניתוחיים בוצעו בהרדמה נמבוטלית ונעשה כל מאמץ למזער את הסבל. עכברי זכר C57BL/6N התקבלו מ-Charles River. העכברים שוכנו בכלובים של חמישה או שישה, נשמרו על מחזור אור/חושך של 12/12 שעות, ואפשרו גישה למזון ולמים באופן חופשי. העכברים היו בני שמונה שבועות לפחות כאשר נבדקו. הבדיקה בוצעה בשלב הקל של המחזור. כל הניסויים נערכו עיוור למצב הטיפול של העכברים.
בדיקת IA מכשיר ה-IA המעבר (OHARA Pharmaceutical) כלל קופסה עם תאים בהירים וכהים נפרדים (שניהם 15.5 12.5 11.5 ס"מ). תא האור הואר באור ניאון (2500 לוקס; Fukushima et al., 2008, 2014; Zhang et al., 2011; Ishikawa et al., 2016). לפני תחילת אימוני ה-IA, העכברים טופלו בנפרד במשך 2 דקות בכל יום במשך שבוע. במהלך האימונים, כל עכבר הורשה להתרגל לתא האור למשך 30 שניות, ודלת הגיליוטינה הוגבהה כדי לאפשר גישה לתא האפל. השהיה לכניסה לתא האפל נחשב כמדד לרכישה. ברגע שהעכבר נכנס לתא החשוך, דלת הגיליוטינה נסגרה. לאחר 5 שניות, הלם רגל (0.2 mA) נמסר לתקופה כוללת של 2 שניות (אימון). ב-24 שעות לאחר האימון, העכבר הונח בחזרה בתא האור עד שנכנס לתא החשוך (ממוצע 459 6 15.49 שניות). מיד לאחר שהעכבר נכנס לתא החשוך, דלת הגיליוטינה נסגרה והעכבר שהה בתא החשוך למשך זמן משתנה (0, 1 או 10 דקות) ללא הלם רגל (הפעלה מחדש). הזיכרון הוערך 48 שעות מאוחר יותר [מבחן זיכרון ארוך טווח לאחר הפעלה מחדש (PR-LTM)] כזמן ההצלבה של העכבר להיכנס לתא האפל כשהוחלף בתא האור, כמו בהפעלה מחדש.
עבור הניסוי הראשון, בחנו את ההשפעה של עיכוב סינתזת חלבון לאחר הפעלה מחדש (חשיפה מחדש לתא האפל למשך 0, 1 או 10 דקות; איור 1). מעכב סינתזת החלבון anisomycin (ANI; Wako) הומס במלח (pH מותאם ל-7.0-7.4 עם NaOH). העכברים אומנו כמתואר לעיל, וכעבור 24 שעות, הם קיבלו כלי רכב (VEH) או ANI (150 מ"ג/ק"ג, ip) מיד לאחר חשיפה מחדש לתא החשוך למשך 0, 1 או 10 דקות ללא הלם רגל. (הפעלה מחדש). במינון זה, ANI מעכב .90 אחוז מסינתזת חלבון במוח במהלך שעתיים הראשונות (Flood et al., 1973). ב-48 שעות לאחר הפעלת ההפעלה מחדש, עכברים בודדים שוב הושמו בתא האור והשהיית ההצלבה הוערכה.
עבור הניסוי השני [אימונוהיסטוכימיה מזורחת CREB (pCREB) ו-ERK מזורחת (pERK); תאנים. 2–5], בדקנו את אזורי המוח שהופעלו לאחר חשיפה חוזרת לאור (עד שהעכברים נכנסו לתא החשוך, חשיפה מחדש לתא האפל למשך 0 דקות) או תא חשוך (מחדש- חשיפה לתא החשוך למשך 1 או 10 דקה). העכברים חולקו לארבעה Fukushima et al. · Transition of Fear Memory Phases after Retrieval J. Neurosci., 10 בפברואר 2021, • 41(6):1288–1300 • 1289groups. ב-24 שעות לאחר האימון, עכברים בודדים נחשפו מחדש לתא הבהיר ולאחר מכן נשארו בתא האפל לאחר כניסתם מהתא האפל [הפעלה מחדש: 0 דקות בתא האפל, קבוצת איחוד מחדש (Recon); 1 דקה, קבוצת מעבר (טראן); 10 דקות, קבוצת הכחדה (Ext)]. קבוצה אחרת של עכברים לא הוחזרה לתא הבהיר/כהה [קבוצת הלא-מופעל מחדש (NR)]. לאחר מכן העכברים הורדמו עם Nembutal (750 מ"ג/ק"ג, ip) ב-5, 15 או 30 דקות לאחר ההפעלה מחדש.
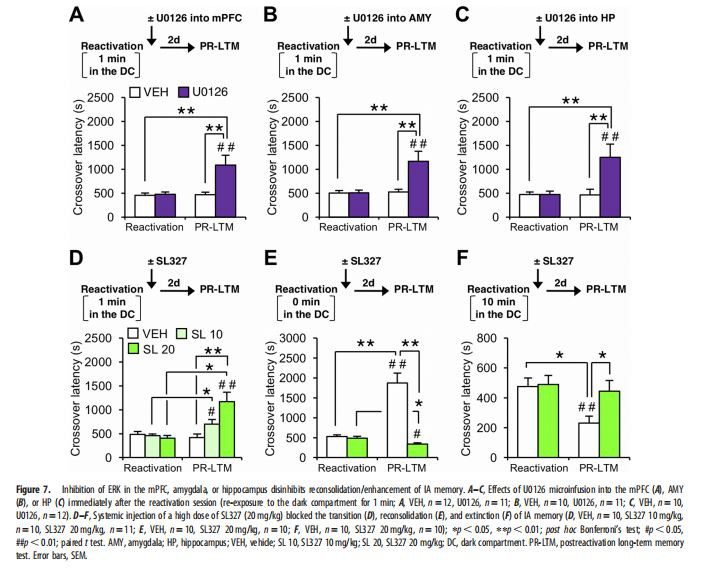
עבור הניסוי השלישי (מיקרואינפוזיה של U0126; איורים 6,7), בחנו את ההשפעות של עיכוב ERK באמיגדלה, בהיפוקמפוס או ב-mPFC עלזיכרוןאיחוד מחדש / שיפור, מעבר והכחדה. מעכב MEK U0126 (Sigma-Aldrich) הומס בנוזל מוחי מלאכותי המכיל שלוש טיפות של Tween 80 (Sigma) ב-2.5 מ"ל של 7.5 אחוז דימתיל סולפוקסיד (Wako) והותאם ל-pH 7.4 עם NaOH. העכברים אומנו כמתואר לעיל, וכעבור 24 שעות, הם הוצבו בחזרה בתא האור (הפעלה מחדש). העכברים הועברו מיקרואינפוזיה עם U0126 (1 מ"ג) או VEH לאזורי המוח השונים מיד לאחר מכן (איורים 6A, C, E–H, 7A–C) או ב-30 דקות לאחר מכן (איור 6B, D) הפעלה מחדש. ב-48 שעות לאחר ההפעלה מחדש, עכברים בודדים שוב הושמו בתא האור וההתנהלות ההצלבה הוערכה (PR LTM). מיקרו אינפוזיות לתוך ההיפוקמפוס ו-mPFC (0.5 מ"ל) נעשו בקצב של 0.25 מ"ל לדקה. מיקרו אינפוזיות לאמיגדלה (0.2 מ"ל) נעשו בקצב של 0.1 מ"ל לדקה. צינורית ההזרקה הושארה במקומה למשך 2 דקות לאחר מיקרואינפוזיה ולאחר מכן העכברים הוחזרו לכלובים הביתיים שלהם. מעכב MEK SL327 (Santa Cruz Biotechnology) הומס ב-dimethyl sulfoxide ומדולל במלח. העכברים אומנו כמתואר לעיל, ו-24 שעות לאחר מכן, עכברים בודדים הוצבו בחזרה בתא האור (הפעלה מחדש). העכברים הוזרקו באופן מערכתי עם SL327 (10 או 20 מ"ג/ק"ג) או VEH מיד לאחר ההפעלה מחדש (איור 7D-F). ב-48 שעות לאחר ההפעלה מחדש, עכברים בודדים שוב הושמו בתא האור וזמן ההצלבה הוערך (PR-LTM).
אימונוהיסטוכימיה בוצעה כמתואר קודם (Mamiya et al., 2009; Suzuki et al., 2011; Zhang et al., 2011; Fukushima et al., 2014; Ishikawa et al., 2016; Hasegawa et al., 2019). לאחר ההרדמה, כל העכברים חולפו ב-4 אחוז פרפורמלדהיד. המוח הוסר, תוקן למשך הלילה, הועברו ל-30 אחוז סוכרוז, ואוחסנו ב-4 מעלות. חתכים קורונליים (30 מ"מ) נחתכו בקריוסטט.
עבור צביעת pCREB ו-pERK, קטעים צפים חופשיים טופלו ב-1 אחוז H2O2 והודגרו למשך הלילה עם נוגדן פוליקלונלי אנטי-פוספו-CREB של ארנב (סרין 133; S133) (1:1000; #{{10 }}, Millipore) ו/או נוגדן אנטי-פוספו-ERK1/2 (T202/Y204) חד-שבטי של ארנב (1:300; #4370; Cell Signaling Technology) בתמיסה חוסמת (מלח מבוצר בפוספט בתוספת 1 אחוז אלבומין בסרום עיזים, 1 מ"ג/מ"ל אלבומין בסרום בקר ו-0.05 אחוז Triton X-100). המקטעים נשטפו עם תמיסת מלח מוגברת בפוספט והודגרו עם IgG של חמור אנטי ארנבת מצומד חזרת פרוקסידאז (1:500; Jackson ImmunoResearch) עבור pCREB או IgG עז נגד ארנבת מצומדת של חזרת פרוקסידאז עבור pERK למשך שעה אחת בטמפרטורת החדר. אותות pCREB הוגברו על ידי ביוטין טירמיד והוצגו באמצעות Alexa Fluor-מצומד streptavidin (Invitrogen). אותות pERK הוגברו עם TSA-FCM (Invitrogen). החלקים הורכבו על שקופיות וכיסויים באמצעות מצע הרכבה (Millipore).
הכימות בוצע כמתואר קודם (Frankland et al., 2006; Fukushima et al., 2014; Mamiya et al., 2009; Zhang et al., 2011; Suzuki et al., 2008). מבנים הוגדרו מבחינה אנטומית על פי האטלס של פרנקלין ופקסינוס (1997). כל הנוירונים החיסוניים נספרו על ידי נסיין עיוור למצב הטיפול

תוצאות
אפיון שלבי זיכרון לאחר שליפה במשימת IA
משימת ה-IA מאפשרת לנו להבחין בין שלבי הגיבוש מחדש וההכחדה בנקודת הזמן שבה עכבר נכנס לתא חשוך מתא בהיר (Fukushima et al., 2014). כדי להבין את המנגנון העומד בבסיס המעבר של שלבי זיכרון מגיבוש מחדש להכחדה, אפיינו את שלבי זיכרון ה-IA בעקבות אחזור הזיכרון על ידי בחינת ההשפעות של עיכוב סינתזת החלבון הנדרשת לאיחוד מחדש והכחדה של זיכרון IA (Fukushima et al., 2014). העכברים הונחו תחילה בתא האור. ב-5 שניות לאחר שנכנסו לתא החשוך, נערך שוק חשמלי קצר (אימון). העכברים נחשפו מחדש לתא האור 24 שעות לאחר האימון (מפגש הפעלה מחדש; איור 1A) וזמן ההצלבה שלהם להיכנס לתא האפל הוערך (איור 1B). העכברים הוחזרו לכלובים הביתיים שלהם מיד לאחר שנכנסו לתא החשוך מהתא האור (0-מינימום חשיפה חוזרת לתא האפל; שלב איחוד מחדש) או שהו בתא החשוך למשך 1, 3, או 10 דקות מבלי לקבל הלם רגל (שלב הכחדה; איור 1C-E). מיד לאחר ההפעלה מחדש, העכברים קיבלו זריקה מערכתית של VEH או מעכב סינתזת החלבון ANI. לאחר 48 שעות, חביון ההצלבה הוערך PR-LTM.
בהתאם למחקר הקודם שלנו (Fukushima et al., 2014), חשיפה מחדש לתא האור (קבוצת 0 דקות) גרמה לגיבוש מחדש ושיפור של זיכרון IA. ANOVA דו-כיווני חשפה השפעות משמעותיות של זמן (F(1,24)=10.433, p=0.{{20}}036), תרופה (F(1) ,24)=23.197, p , 0.0001) ואינטראקציה בין תרופות בזמן (F(1,24)=25.022, p , 0.0001; איור 1B). הבדיקה של Bonferroni שלאחר ההוצאה ומבחן ה-t המזווג גילו כי קבוצות VEH ו-ANI, הציגו חביון מוצלב מוגבר או מופחת באופן משמעותי, בהתאמה, ב-PR-LTM בהשוואה להפעלת ההפעלה מחדש (ps , 0.05; VEH, t(6) {{28 }} 5.134, p=0.0021, ANI, t(6)=4.804, p=0.003; איור 1B). תצפיות אלו מצביעות על כך ששליפת זיכרון IA בתא האור שיפרה את הזיכרון, בעוד שעיכוב סינתזת חלבון שיבש את הזיכרון שאוחזר, ומאשר את התצפית הקודמת כי אחזור זיכרון IA משפר את הזיכרון באמצעות איחוד מחדש באופן תלוי סינתזת חלבון.

לעומת זאת, החשיפה המחודשת לתא האפל גרמה להכחדה ארוכת טווח [ANOVA דו כיווני, זמן (איור 1C, F(1,28)=9.575, p=0.{ {50}}04; איור 1D, F(1,36)=11.699, p=0.0016), תרופה (איור 1C, F(1,28)=4.674, p=0.039; איור 1D, F(1,36)=12.285, p {{29 }}.0012), זמן אינטראקציה בין תרופות (איור 1C, F(1,28)=7.916, p=0.009; איור 1D, F(1,36) {{41 }}.915, p=0.0079)], כפי שנצפה בעבר (Fukushima et al., 2014). קבוצות ה-VEH ששהו בתא החשוך למשך 3 או 10 דקות הראו ירידה משמעותית ב-Cross-over-latency ב-PR-LTM בהשוואה לסשן ההפעלה מחדש, בעוד שקבוצות ה-ANI הציגו זמן השהיית הצלבה דומה ב-PR-LTM בהשוואה לסשן ההפעלה מחדש ול- קבוצות VEH (הבדיקה של בונפרוני, ps , 0.05; מבחן t מזווג, איור 1C, VEH, t(7)=4.976, p=0.0016, ANI, t(7) { {59}}.796, p . 0.05; איור 1D, VEH, t(9)=10.211, p , 0.0001, ANI, t(9)=1.02, p . 0.05 ). תצפיות אלו מצביעות על כך שהחשיפה המחודשת לתא האפל למשך 3 או 10 דקות כיבה את זיכרון ה-IA וכי עיכוב סינתזת החלבון חסם הכחדה ארוכת טווח. לפיכך, שליפת זיכרון IA בתא האפל מכבה זיכרון IA באופן תלוי ביטוי גנים.
חשוב לציין, קבוצת VEH הראתה חביון הצלבה דומה ב-PR-LTM בהשוואה לסשן ההפעלה מחדש ולקבוצת ה-ANI כאשר הם שהו בתא החשוך במשך דקה אחת [ANOVA דו-כיווני, זמן (F(1,36) {{ 5}}.03, p. 0.05), drug (F(1,36)=0.019, p. 0.05), זמן אינטראקציה בין תרופות (F(1,36)=0.011, p . 0.05); מבחן פוסט הוק בונפרוני, נ.ב. 0.05; מבחן t מצמד, VEH, t(9)=0.091, p . 0.05, ANI, t(9)=0.328, p . 0.05; איור 1ה]. תצפיות אלו מצביעות על כך שקבוצת VEH לא הראתה שיפור או הכחדה של זיכרון IA וכי קבוצת ANI לא הראתה הפרעה בזיכרון IA. לכן, חשיפה חוזרת לתא האפל למשך דקה אחת חסמה גם את השיפור וגם את ההפרעה הנגרמת על ידי ANI של זיכרון ה-IA שהופעל מחדש, אך לא כיבויה את זיכרון ה-IA, מה שמרמז שחשיפה מחודשת זו 1-מבטלת את השראת הגיבוש מחדש. , אך אינו מספיק כדי לכבות זיכרון IA.
לסיכום, תוצאות אלו הצביעו על כך שחשיפה חוזרת לתא האור גורמת לשלב הגיבוש מחדש, בעוד שחשיפה ממושכת יותר לתא החשוך (3 או 10 דקות) גורמת לשלב ההכחדה. חשוב מכך, שהייה של דקה אחת בתא החשוך גורמת לשלב המעבר מגיבוש מחדש להכחדה, אשר מעכב איחוד מחדש של זיכרון הפחד מבלי לגרום להכחדה.
חתימות מולקולריות של שלבי הגיבוש מחדש, המעבר וההכחדה באמיגדלה, בהיפוקמפוס וב-mPFC לאחר אחזור זיכרון IA
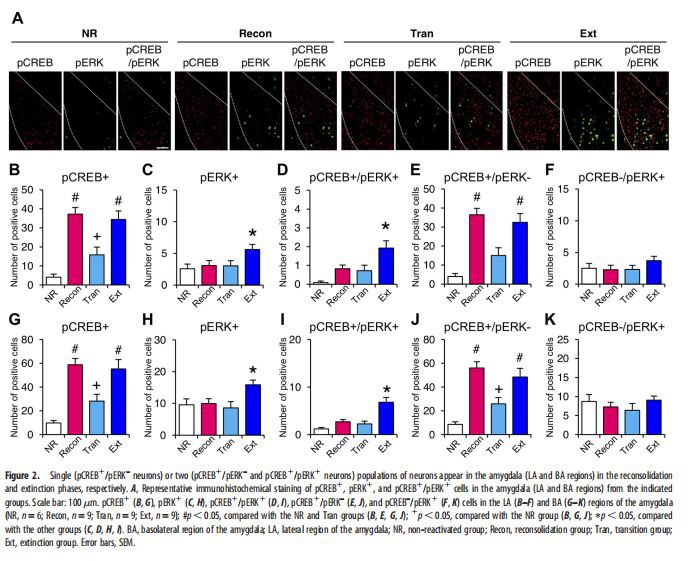
איחוד מחדש והכחדה של זיכרון פחד הקשרי מראים עליות בזרחן CREB ב-S133, סמן של הפעלת ביטוי גנים הנדרש לאיחוד מחדש והכחדה ארוכת טווח, אך מראים דינמיקה ברורה של זרחון CREB (Mamiya et al., 2009 ). מעניין שמחקרים עדכניים הראו שאין עלייה בזרחון של ERK, מווסת במעלה הזרם של CREB (Impey et al., 1998; Wu et al., 2001), באזור הבזולטרלי של האמיגדלה במעבר מגיבוש מחדש להכחדה של זיכרון פחד רמז, אם כי זרחון זה מוגבר באזור הבזולטרלי כאשר זיכרון פחד רמז מתגבש מחדש ומכבה (Merlo et al., 2014, 2018). מחקר אחר הצביע על כך ש-ERK בהיפוקמפוס מופעל רק כאשר זיכרון הפחד ההקשרי נכבה, אך לא מאוחד מחדש (Tronson et al., 2009). ממצאים אלה מצביעים על כך ששלבי גיבוש מחדש, מעבר והכחדה מראים חתימות מולקולריות ותאיות ברורות. לכן, מדדנו והשווינו את הרמות של pCREB ו-pERK בשלבי הגיבוש מחדש, המעבר וההכחדה באמצעות אימונוהיסטוכימיה. ביצענו לוחות זמנים ניסויים דומים כמו באיור 1B, D, E באמצעות ארבע קבוצות ניסוי. העכברים נחשפו מחדש לתא האור ב-24 שעות לאחר האימון ולאחר מכן נשארו בתא האפל [הפעלה מחדש: 0 דקות בתא האפל, קבוצת איחוד מחדש (Recon); 1 דקה, קבוצת מעבר (טראן); 10 דקות, קבוצת הכחדה (Ext)]. קבוצה אחרת של עכברים לא הוחזרה לתא הבהיר/כהה (לא הופעל מחדש, קבוצת NR). ספרנו נוירונים חיוביים ל-pCREB (pCREB1), נוירונים חיוביים ל-pERK (pERK1) ונוירונים כפולים חיוביים (pCREB1/pERK1) באמיגדלה, בהיפוקמפוס וב-mPFC ב-30 דקות לאחר הפעלת ההפעלה מחדש.
אמיגדלה (אזור רוחבי) CREB הופעל בשלבי ההכחדה והגיבוש מחדש, ואילו ERK הופעל רק בשלב ההכחדה (איור 2A-C). ANOVA חד כיווני חשפה השפעה משמעותית של הקבוצה (איור 2B, F(3,29)=14.85, p , 0.0001). בדומה לממצאים קודמים (Mamiya et al., 2009), מבחן Newman-Keuls לאחר ההוצאה גילה כי קבוצות Recon ו-Ext הראו באופן משמעותי יותר נוירונים pCREB1 מאשר הקבוצות האחרות (עמ' 0.05). תצפיות אלו הצביעו על כך שבדומה לתצפיות ברמות ההתנהגות (איור 1), חשיפה לתא האפל למשך דקה אחת (שלב המעבר) מבטלת את ה"הדלקה" של זרחון CREB שתוגבר בשלב הגיבוש מחדש. לעומת זאת, נצפו באופן משמעותי יותר נוירונים pERK1 בקבוצת ה-Ext מאשר בקבוצות האחרות, אם כי היו הרבה פחות נוירונים pERK1 מאשר נוירונים pCREB1 בקבוצת ה-Ext (F(3,29)=3.793, p { {23}}.0207; איור 2C).

באופן עקבי, נצפו באופן משמעותי יותר נוירונים חיוביים כפולים (pCREB1/pERK1) בקבוצת Ext (F(3,29)=6.698, p=0.00 14; איור 2D), בעוד שנצפתו באופן משמעותי יותר נוירונים מסוג pCREB1/pERK– (pCREB יחיד חיובי) בקבוצות Recon ו-Ext (F(3,29)=13.689, p , 0 .0001; איור 2E). לפיכך, שלב האיחוד מחדש הראה רק אוכלוסייה בודדת של נוירונים pCREB1/pERK–. לעומת זאת, שלב ההכחדה הראה שתי אוכלוסיות של נוירונים pCREB1/pERK– ו-pCREB1/pERK1, מה שמצביע על כך ש-ERK מופעל רק בתת-קבוצה של נוירונים pCREB1. חשוב לציין, תוצאות דומות נצפו באזור הבזולטרלי של האמיגדלה (איור 2G, F(3,29)=13.042, p , 0.0001; איור 2H, F(3,29) {{32} }.824, p=0.0201; איור 2I, F(3,29)=12.633, p , 0.0001; איור 2J, F(3,29)=12 .505, p , 0.0001).
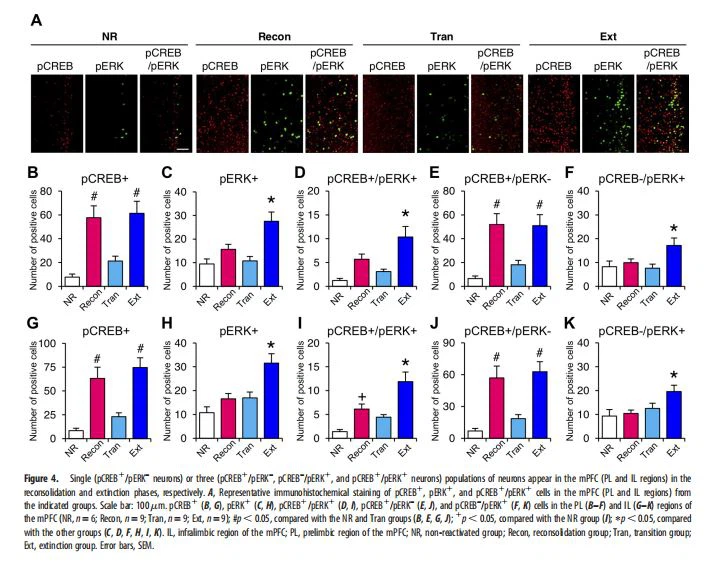
הפעלה דו-פאזית של ERK בשלב ההכחדה ERK היא מפעיל במעלה הזרם של CREB ולפיכך נדרשת הפעלת ERK לגיבוש וגיבוש מחדש של זיכרון הפחד (Schafe et al., 200{{31 }}; Duvarci et al., 2005). עם זאת, באופן לא עקבי, לא נצפתה הפעלת ERK באמיגדלה, בהיפוקמפוס או ב-mPFC בשלב הגיבוש מחדש כאשר pERK נמדד ב-30 דקות לאחר הפעלת ההפעלה מחדש (איורים 2-4). לכן, בדקנו את מהלכי הזמן של זרחון ERK ו-CREB. ביצענו ניסוי דומה כמו באיורים 2-4, מלבד שרמות pCREB ו-pERK נמדדו ב-5, 15 ו-30 דקות לאחר סשן ההפעלה מחדש (חשיפה מחדש לתא החשוך למשך {{ 66}}, 1 או 10 דקות; איור 5A). בהתאם לנתונים המוצגים באיורים 2-4, עליות משמעותיות בנוירונים pCREB1 נצפו ב-30 דקות, אך לא ב-5 דקות, לאחר סשן ההפעלה מחדש ב-Recon (אמיגדלה,mPFC והיפוקמפוס) וב-Ext (אמיגדלה ו-mPFC ) קבוצות, אך לא קבוצת טראן (איור 5E, ANOVA חד כיווני, אמיגדלה, 5 דקות, F(3,23)=0.346, p . 0.05, 30 min, F(3,23)=15.272, p , 0.0001; mPFC, 5 min, F(3,23)=1.169, p . 0.05, 30 min, F(3,23)=32. 346, p , 0.0001; היפוקמפוס, 5 דקות, F(3,23)=0.154, p. 0.05, 30 min, F(3,23)=16.197, p , 0.0001; בדיקת t לא מזווגת, אמיגדלה, קונסולידציה מחדש, 5 לעומת 30 דקות, t(12)=7.807, p , 0.0001, הכחדה, 5 לעומת 30 דקות, t(12)=5.405, p { {73}}.0002; mPFC, איחוד מחדש, 5 לעומת 30 דקות, t(12)=5.727, p , 0.0001, הכחדה, 5 לעומת 30 דקות, t(12)=4.188 , p=0.0013; אזור ההיפוקמפוס CA1, איחוד מחדש, 5 לעומת 30 דקות, t(12)=2.339, p=0.0374).
מעניין לציין, עליות משמעותיות בנוירונים pERK1 נצפו באמיגדלה, mPFC והיפוקמפוס של קבוצות Recon, Tran ו-Ext ב-5 דקות לאחר הפעלת ההפעלה מחדש בהשוואה לקבוצת NR (איור 5F, אמיגדלה, F(3,23)=10.961, p=0.0001; mPFC, F(3,23)=7.525, p { {13}}.0011; hippocampus, F(3,23)=6.924, p=0.0017). תצפיות אלו הצביעו על כך ש-ERK מופעל מיד לאחר סשן ההפעלה מחדש בכל שלבי הזיכרון. עם זאת, העליות הללו במספר הנוירונים pERK1 חזרו לרמות הבסיס (בהשוואה לקבוצת ה-NR) ב-15 דקות לאחר הפעלת ההפעלה מחדש (איור 5F, אמיגדלה, F(3,20)=2.676, p. .0.05; mPFC, F(3,23)=0.683, p . 0.05; hippocampus, F(3,20)=0.74, p. 0.05). יתרה מזאת, בהתאם לממצאים המוצגים באיורים 2-4, נצפו משמעותית יותר נוירונים של pERK1 באמיגדלה, mPFC והיפוקמפוס ב-30 דקות לאחר הפעלת ההפעלה מחדש רק בקבוצת Ext (איור 5F, אמיגדלה, F( 3,23)=6.616, p=0.022; mPFC, F(3,23)=8.012, p=0.0008; hippocampus, F( 3,23)=6.206, עמ'=0.003). לפיכך, שלבי האיחוד מחדש והמעבר מראים הפעלה חולפת של ERK רק בנקודת הזמן המוקדמת (5 דקות), בעוד ששלב ההכחדה מראה הפעלה דו-פאזית של ERK בנקודות הזמן המוקדמות (5 דקות) ומאוחרות (30 דקות) לאחר ההפעלה מחדש מוֹשָׁב. תצפיות אלו הצביעו על כך שהמנגנונים לוויסות הפעלת ERK שונים בשלבי הגיבוש/המעבר וההכחדה. באופן קולקטיבי, התצפיות שלנו הוכיחו ששלבי הגיבוש מחדש, המעבר וההכחדה מראים חתימות מולקולריות ברורות.
תפקידים של הפעלת ERK בשלבי איחוד מחדש והכחדה של זיכרון IA
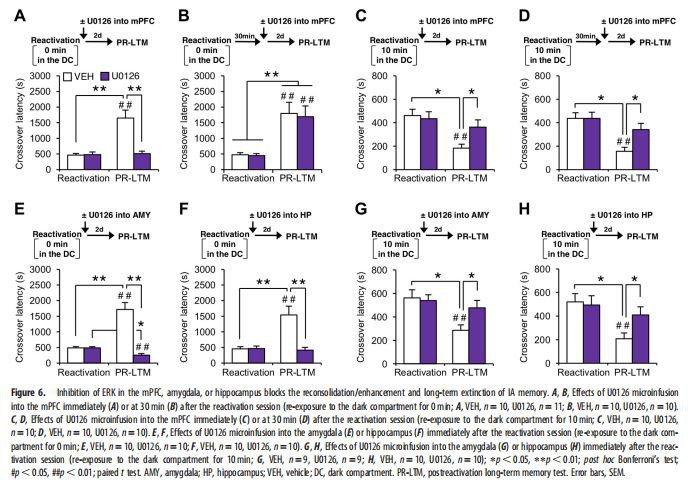
שלבי הקונסולידציה/המעבר וההכחדה הראו הפעלת ERK מונופאזית וביפאזית, בהתאמה. לאחר מכן חקרנו והשווינו את התפקידים של הפעלת ERK מוקדמת (5 דקות) ומאוחרת (30 דקות) ב-mPFC בשלבי הגיבוש מחדש וההכחדה על ידי בחינת ההשפעות של עיכוב ERK (איור 6).


דִיוּן
במחקר זה, חקרנו את המנגנונים למעבר זיכרון משלבי הגיבוש מחדש להכחדה לאחר שליפה של זיכרון IA. תחילה אפינו את החתימות ההתנהגותיות של שלבי זיכרון IA לאחר השליפה. בהתאם למחקר הקודם שלנו (Fukushima et al., 2014), אחזור זיכרון IA הנגרמת קונסולידציה והכחדה מחדש על ידי חשיפה מחדש לאור (0 דקות בתא החשוך) ולחושך ( תאים של 3 או 10 דקות), בהתאמה. מעניין לציין שזיכרון IA לא השתפר ולא כבה והראה עמידות לעיכוב סינתזת חלבון כאשר העכברים נחשפו מחדש לתא האפל למשך דקה אחת בלבד. לכן, תצפיות אלו מצביעות על כך שחשיפה חוזרת של 1-דקה לתא האפל מבטלת את השראת הגיבוש מחדש, אך אינה מספיקה כדי לכבות את זיכרון ה-IA. יתר על כן, מצאנו ש-ERK הופעל באמיגדלה, בהיפוקמפוס וב-mPFC בנקודת זמן מוקדמת (5 דקות) לאחר חשיפה חוזרת לתא האפל למשך 0, 1 או 10 דקות. באופן עקבי, העיכוב של ERK באזורי מוח אלה חסם את הגיבוש/השבחה מחדש והכחדה של זיכרון IA. והכי חשוב, עיכוב ERK באמיגדלה, בהיפוקמפוס וב-mPFC לאחר 1-דקות חשיפה חוזרת לתא האפל ביטלו את השיפור בתיווך איחוד מחדש של זיכרון IA, מה שמרמז על הפעלת ERK לאחר חשיפה חוזרת קצרה (דקה אחת) לתא האפל נדרש לעיכוב איחוד זיכרון IA מחדש. לעומת זאת, חשיפה חוזרת של 1-דקות לתא האפל לא הספיקה כדי לכבות את זיכרון ה-IA, אם כי חשיפה ממושכת לתא האפל (3 או 10 דקות) כיבתה את הזיכרון הזה. לכן, התוצאות שלנו מצביעות על כך שחשיפה מחודשת של 1-דקות לתא האפל גורמת לתהליך מעבר זיכרון שמבטל איחוד מחדש/שיפור אך אינו מתחיל למידת הכחדה. באופן קולקטיבי, אנו מציעים שתהליך מעבר הזיכרון תורם למעבר של שלבי זיכרון מאיחוד מחדש להכחדה באמצעות מניעת איחוד מחדש בתיווך ERK.
בדומה לתצפיות הנוכחיות שלנו, מחקר שנערך לאחרונה באמצעות התניה של פחד שמיעתי הראה שמצגות CS בודדות (1) או ממושכות (10) גורמות לחיזוק זיכרון והכחדה מחדש, בהתאמה, באמצעות עלייה של רמות pERK באזור הבזולטרלי של האמיגדלה. לעומת זאת, מצגות CS ביניים (4-7) אינן משנות את רמות pERK באזור הבזולטרלי של האמיגדלה. חשוב לציין, עיכוב ERK במצגות CS הביניים לא השפיע על זיכרון הפחד. מחקר זה הציע כי קיים מעבר של שלב הזיכרון מגיבוש מחדש להכחדה לאחר אחזור זיכרון פחד (Merlo et al., 2018). במחקר הנוכחי, הרחבנו את הממצא הזה והצענו ששלב המעבר מחליף באופן אקטיבי שלבי זיכרון מאיחוד מחדש להכחדה באמצעות הפעלת מסלול העברת האות ERK. בניגוד לממצאים קודמים (Merlo et al., 2018), מצאנו ששלב המעבר כולל זרחון ERK באמיגדלה, בהיפוקמפוס וב-mPFC. אי-התאמות אלו אולי בגלל ההבדל בין נקודות הזמן הבודקות זרחון ERK; במחקר הקודם נמדדו רמות pERK ב-;12 דקות לאחר הצגת CS (Merlo et al., 2018), בעוד שהמחקר שלנו הראה שרמות pERK מוגברות חזרו לרמה הבסיסית בערך בנקודת זמן זו (15 דקות לאחר החשיפה החוזרת). בנוסף, חשוב לציין שמשימת ה-IA מאפשרת צפייה בשיפור זיכרון ה-IA באמצעות קונסולידציה מחדש, ובכך מובילה לממצא שלנו שעיכוב של ERK בשלב המעבר מונע את שיפור זיכרון ה-IA.
מחקרים קודמים הראו שזרחון ERK מוגבר באזור הבזולטרלי של האמיגדלה ב-20-60 דקות לאחר למידת הכחדה של זיכרון פחד רמז (Herry et al., 2006; Merlo et al., 2014, 2018), בעוד שההיפוקמפוס מראה הפעלה זו בשעה אחת לאחר לימוד ההכחדה של זיכרון פחד הקשרי (Fischer et al., 2007; Tronson et al., 2009). במחקר הנוכחי, השגנו תצפיות דומות לפיהן ה-pERK גדל ב-30 דקות לאחר סשן ההפעלה מחדש בשלב ההכחדה. ממצאים אלה מצביעים על כך שזרחון ERK הוא חתימה מולקולרית נפוצה של שלב ההכחדה המאוחר (20-60 דקות).
יתר על כן, ראינו שהפעלת ERK מתרחשת באופן דו-פאזי בנקודות זמן מוקדמות ומאוחרות (5 ו-30 דקות) לאחר הפעלת ההפעלה מחדש בשלב ההכחדה, בעוד שהפעלה זו מתרחשת חד פאזית בנקודת הזמן המוקדמת בשלב הגיבוש מחדש (איור 5). . באופן עקבי, עיכוב של ERK באזורי מוח בנקודות זמן אלו של שלבי הגיבוש מחדש וההכחדה חסם איחוד מחדש/שיפור והכחדה לטווח ארוך, בהתאמה (איור 6A, C-H). תצפיות אלו מצביעות על כך שהפעלת ERK מונופאזית ודו-פאזית נדרשת לשיפור והכחדה בתיווך של איחוד מחדש של זיכרון IA, בהתאמה. חשוב לציין כי ERK מתפקד כמווסת במעלה הזרם של זרחון CREB. לכן, ההפעלה החולפת של ERK בשלב הזיכרון המוקדם עשויה, לפחות חלקית, לתרום לזרחון זה של CREB, אשר מפעיל את ביטוי הגנים הנדרשים לגיבוש מחדש ולהכחדה ארוכת טווח.

בדומה לממצאים הקודמים שלנו באמצעות התניית פחד קונטקסטואלית (Mamiya et al., 2009), CREB הופעל בשלבי הגיבוש מחדש (אמיגדלה/היפוקמפוס/mPFC) והכחדה (אמיגדלה/mPFC), בעוד ERK הופעל רק בשלב ההכחדה ב-30 דקות לאחר סשן ההפעלה מחדש. באופן עקבי, רק אוכלוסייה בודדת של נוירונים pCREB1/pERK– נצפתה בשלב הקונסולידציה, בעוד שאוכלוסיות נוירונים מובחנות נצפו בשלב ההכחדה: נוירונים pCREB1/pERK– ו-pCREB1/pERK1 באמיגדלה (איור 2); נוירונים pCREB– /pERK1 בהיפוקמפוס (איור 3); ונוירונים pCREB1/pERK–, pCREB–/pERK1 ו-pCREB1/pERK1 ב-mPFC (איור 4). תצפיות אלו, במיוחד התצפית המנוגדת של נוירונים pCREB–/pERK1 ו-pCREB1/pERK–, מצביעות על כך שההפעלה של CREB ו-ERK מווסתת באופן שונה בכל אזור מוח כאשר הזיכרון כבוי וכי ההפעלה בשלב מאוחר של ERK משחקת ספציפית ומובחנת. תפקידים להכחדת זיכרון הפחד בהשוואה לתהליכי זיכרון אחרים כגון קונסולידציה וגיבוש מחדש כפי שנדון להלן. מעניין לציין כי נוירוני pERK1 היו נפוצים יותר ב-mPFC בהשוואה להיפוקמפוס והאמיגדלה, מכיוון שה-mPFC הראה יחס גבוה יותר של נוירונים pERK1 (שלב ההכחדה) ונוירונים pCREB1 (שלב איחוד מחדש) בהשוואה להיפוקמפוס והאמיגדלה, מה שמרמז כי ההפעלה של ERK ב-mPFC משחקת תפקיד ספציפי יותר בהכחדת הזיכרון.
עדיין לא ברור אם אוכלוסיות זהות או שונות של נוירונים מופעלות בשלבי הגיבוש מחדש, המעבר וההכחדה. מחקר קודם זיהה את ההפעלה של "נוירוני פחד" ו"נוירוני הכחדה" באמיגדלה כאשר זיכרון פחד רמז מופעל מחדש או כבוי, בהתאמה (Herry et al., 2008). לכן, ייתכן ש-ERK ו-CREB מופעלים באוכלוסיות השונות של נוירונים עם פרופילים זמניים שונים (כלומר, "נוירוני קונסולידציה מחדש" ונוירוני הכחדה). כפי שנדון לעיל, נוירוני pCREB1, כולל נוירוני pCREB1/pERK1, עשויים לווסת את הגיבוש מחדש וההכחדה לטווח ארוך של זיכרון IA באמצעות הפעלת ביטוי גנים כנוירוני קונסולידציה והכחדה, בהתאמה. לעומת זאת, הפעלת ERK בנוירונים pCREB- /pERK1 עשויה לתרום לביטול של הפעלת תעתיק בתיווך CREB שתידרש לאיחוד מחדש מכיוון שהפעלת ERK זו נצפית במיוחד בשלב ההכחדה המאוחר; ERK הפעיל בנוירונים של קונסולידציה מחדש כדי לבטל את ההפעלה של ביטוי גנים בשלב ההכחדה. מעניין לציין שמחקר קודם הראה שהפעלת ERK בהיפוקמפוס חוסמת את האינדוקציה של c-fos כאשר זיכרון הפחד ההקשרי נכבה (Guedea et al., 2011), מה שהעלה את האפשרות שהפעלת ERK זו נוגדת את מסלול האותות של CREB. חשוב לזהות את האוכלוסיות הנוירונים המווסתות את הגיבוש מחדש, המעבר וההכחדה ולחקור את החתימות המולקולריות ואת המשמעות התפקודית של אותם נוירונים. בנוסף, אינטראקציות בין אוכלוסיות עצביות שזוהו במחקר זה נותרו לא ידועות. ייתכן ש"נוירוני הכחדה (מעבר)" מווסתים את תפקודם של נוירוני קונסולידציה מחדש כדי לבטל מניעת קונסולידציה מחדש באמצעות אינטראקציות ביניהם (Eisenberg et al., 2003; Merlo et al., 2014). לכן, חשוב גם לבחון אינטראקציות אלו באמיגדלה, mPFC והיפוקמפוס ובין האמיגדלה.
בעבר, הראינו שההיפוקמפוס לא מציג שום שינוי בזרחן CREB ובביטוי Arc בעקבות למידה של הכחדה של פחד הקשרי, ובאופן עקבי, עיכוב סינתזת החלבון בהיפוקמפוס בשלב ההכחדה לא מצליח לחסום הכחדה לטווח ארוך (Mamiya et al. , 2009). תצפיות אלו העלו את האפשרות שההיפוקמפוס אינו נדרש להכחדה ארוכת טווח. עם זאת, הראינו ש-ERK מופעל בהיפוקמפוס לאחר למידה של הכחדה של זיכרון IA, ובאופן עקבי, חסימת הפעלת ERK בהיפוקמפוס פוגעת בהכחדה ארוכת טווח. לכן, התצפיות הנוכחיות שלנו מצביעות על תפקידים חיוניים להיפוקמפוס בהכחדת הזיכרון. יחד עם הממצאים הקודמים שלנו, אנו מציעים כי ההיפוקמפוס נדרש להכחדת זיכרון אך לא לתהליך דמוי קונסולידציה לייצוב "זיכרון הכחדה" באמצעות הפעלת ביטוי גנים.


